Clear Sky Science · nl
Een celcyclus-afhankelijke overgang van acetylatie naar fosforylatie reguleert tijdige centrosoomrijping
Ons genetische vracht op het spoor houden
Elke keer dat een cel in ons lichaam deelt, moet ze haar DNA met uiterste precisie verdelen. Als dit proces misgaat, kunnen cellen chromosomen winnen of verliezen, een gevaarlijke toestand die in verband wordt gebracht met kanker en andere ziekten. Deze studie onthult een moleculair tijdmeetinstrument dat cellen helpt de kleine structuren op te bouwen die nodig zijn om chromosomen correct te scheiden, en toont een potentiële zwakke plek die toekomstige kankertherapieën zouden kunnen benutten.
De kleine verkeersknooppunten van de cel
In het hart van elke delende cel bevinden zich centrosomen, kleine structuren die fungeren als verkeersknooppunten voor de vezels die chromosomen uit elkaar trekken. Voordat een cel in de deling gaat, moeten deze knooppunten "rijpen": ze vullen zich met hulp-eiwitten en worden krachtige organisatoren van microtubuli, de dynamische vezels die de delingsspoel vormen. Als deze rijping te vroeg, te laat of helemaal niet plaatsvindt, kunnen chromosomen verkeerd verdeeld raken, wat leidt tot cellen met abnormale aantallen chromosomen. Begrijpen hoe cellen centrosomen op precies het juiste moment inschakelen is een langlopend vraagstuk in de celbiologie.
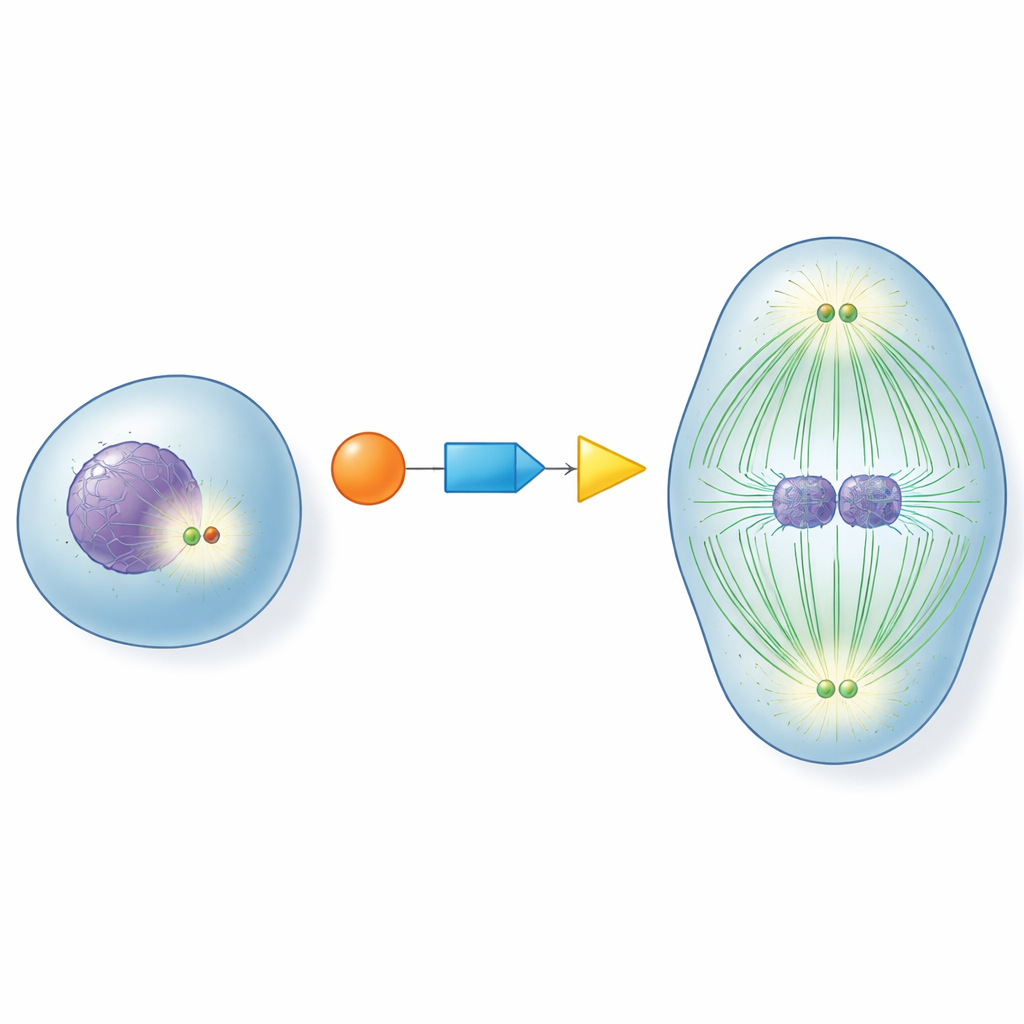
Een moleculaire estafette voor perfecte timing
De auteurs richtten zich op drie sleuteleiwitten die samenwerken als een estafette: CDK1, een meesterregelaar van de celcyclus; RNF40, voorheen vooral bekend om het wijzigen van DNA-verpakkende eiwitten; en PLK1, een belangrijke aanjager van celdeling. Ze ontdekten dat RNF40 fysiek aanwezig is bij centrosomen gedurende de hele celcyclus en direct aan PLK1 bindt. Naarmate cellen de deling naderen, markeert CDK1 RNF40 chemisch op twee specifieke punten, wat RNF40 op zijn beurt een betere aanlegplaats voor PLK1 maakt. Deze CDK1–RNF40–PLK1-keten zorgt ervoor dat PLK1 tijdens de late voorbereidingsfase van de deling precies op het juiste moment bij centrosomen arriveert, waardoor krachtige centrosoomrijping, microtubulusgroei en de assemblage van een goed gevormde bipolaire spoel worden geactiveerd.
Een vormveranderende eiwitschakelaar
Opmerkelijk genoeg accepteert RNF40 deze activerende tags niet altijd. In niet-delende en DNA-kopieerfasen draagt RNF40 een andere chemische versiering—acetylgroepen—op twee nabijgelegen posities. Deze acetylmerken worden toegevoegd door een enzym genaamd PCAF en later verwijderd door een deacetylaserende partner, HDAC1. De geacetyleerde versie van RNF40 is resistent tegen modificatie door CDK1 en blokkeert zo effectief de volgende stap in de estafette. Terwijl cellen naar de laatste pre-delingsfase gaan, wist HDAC1 geleidelijk de acetylmerken uit, waardoor CDK1 in plaats daarvan fosfaatgroepen kan toevoegen. Deze zorgvuldig getimede switch van acetylatie naar fosforylatie verandert RNF40 van een "stand-by"-toestand in een "aan"-toestand, klaar om PLK1 te recruteren en het centrosoom op te starten.
Wat gebeurt er als de timing faalt
Om te onderzoeken hoe cruciaal deze schakeling is, maakten de onderzoekers cellen waarbij RNF40 niet langer gefosforyleerd kon worden, of waarin het geforceerd in een acetylatie-imiterende staat bleef. In beide gevallen slaagde PLK1 er niet in zich goed bij centrosomen op te hopen. Deze cellen toonden verzwakte microtubulusgroei vanuit centrosomen, verkeerd gevormde spoelen en misgeplaatste chromosomen. Velen eindigden met extra of ontbrekende chromosomen—een abnormale toestand bekend als aneuploidie—en sommige werden binucleair, tekenen van catastrofale delingsfouten. In kankermodellen vormden cellen die vastzaten in de "geacetyleerde" RNF40-toestand kleinere tumoren in muizen en waren ze gevoeliger voor gangbare chemotherapieën die worden gebruikt bij de behandeling van dikkedarmkanker, wat suggereert dat het verstoren van deze schakeling de tumorgroei kan vertragen.
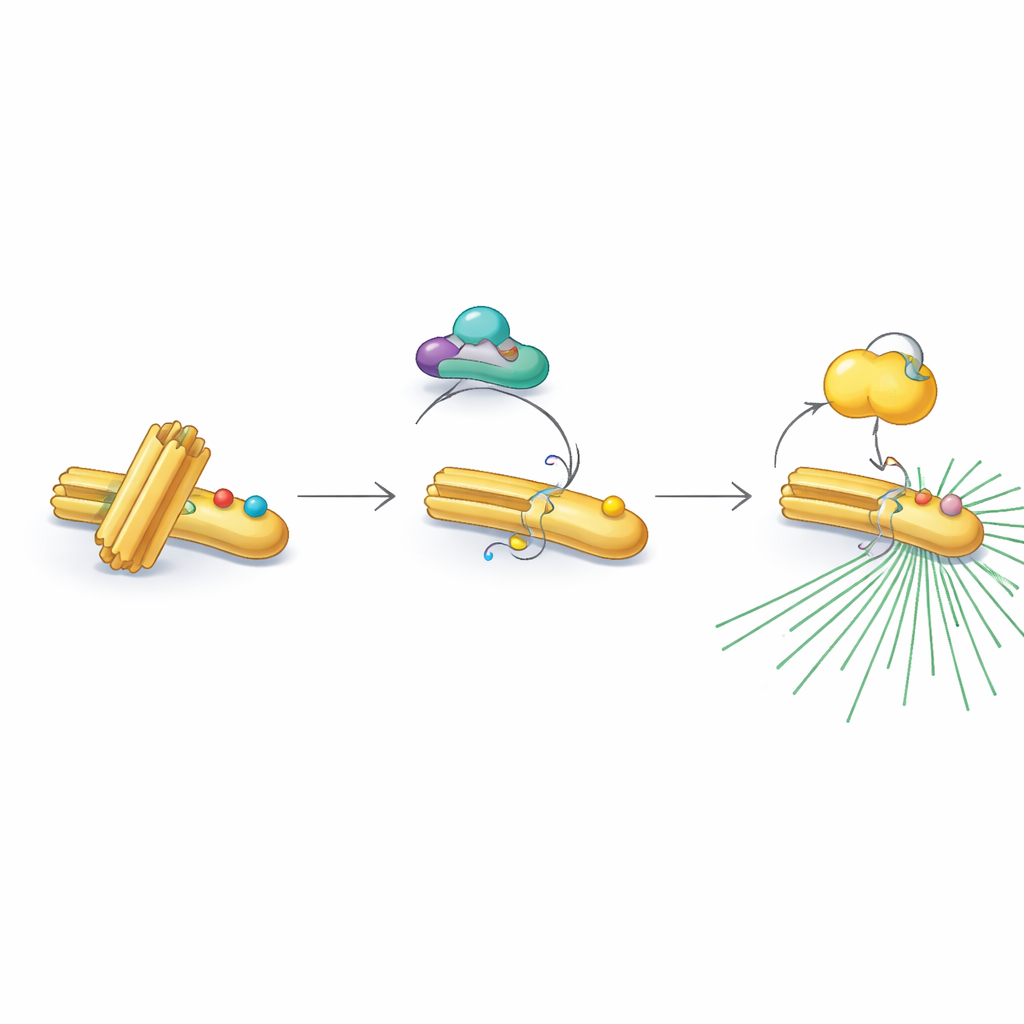
Verbanden met menselijke kanker en toekomstige mogelijkheden
Het team onderzocht ook patiëntgegevens en tumormonsters. Ze vonden dat RNF40 vaak abnormaal overvloedig is bij dikkedarmkankers en dat bepaalde kanker-geassocieerde mutaties in de buurt van zijn modificatieplaatsen de fosforylatie verstoren, waardoor de juiste centrosoomfunctie wordt ondermijnd. Deze observaties koppelen het nieuw beschreven tijdmechanisme rechtstreeks aan menselijke ziekte. Door een specifiek eiwit aan te wijzen dat coördineert wanneer centrosomen rijpen en hoe chromosomen worden gescheiden, benadrukt de studie een signalerings"knoop" die mogelijk gericht kan worden om snel delende kankercellen in dodelijke delingsfouten te duwen, terwijl gezonde cellen minder worden getroffen.
Een nieuw handvat voor betrouwbare celdeling
Voor niet-specialisten is de kernboodschap dat cellen vertrouwen op een fijn afgestelde chemische schakel op één eiwit, RNF40, om precies te bepalen wanneer de machinerie die chromosomen scheidt moet worden geactiveerd. Deze overgang van acetylatie naar fosforylatie werkt als een verkeerslicht op een druk kruispunt en springt pas op groen als de cel echt klaar is om te delen. Als het licht niet werkt, struikelen cellen tijdens de deling, hopen zich genetische fouten op en kunnen ze kankerachtig worden. Het begrijpen en beheersen van deze schakel kan nieuwe wegen openen naar behandelingen die selectief kankercellen destabiliseren door hun vermogen om schoon te delen te ondermijnen.
Bronvermelding: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Trefwoorden: rijping van centrosomen, celdeling, chromosoominstabiliteit, PLK1-signaaltransductie, dikke darmkanker