Clear Sky Science · nl
Keuze van reactiepaden tussen click- en acyloverdrachtsreacties aangedreven door aminoacylfosfaten
Waarom timing ertoe doet in alledaagse chemie
In elke cel worden belangrijke moleculen in een zeer precieze volgorde opgebouwd en aangepast, vergelijkbaar met stappen in een recept. Die timing bepaalt of een eiwit aan of uit gaat, of zelfs van vorm verandert. Chemici willen dit soort ingebouwde schema nabootsen met eenvoudige, niet-levende moleculen in water, zonder enzymen of externe prikkels zoals licht- of pH-veranderingen. Dit artikel beschrijft een kunstmatig reactiesysteem dat precies dat doet: het gebruikt de structuur van kleine peptiden en een veelgebruikte bindingvormende reactie uit de "clickchemie" om te bepalen welke chemische stap eerst plaatsvindt en welke op zijn beurt moet wachten.
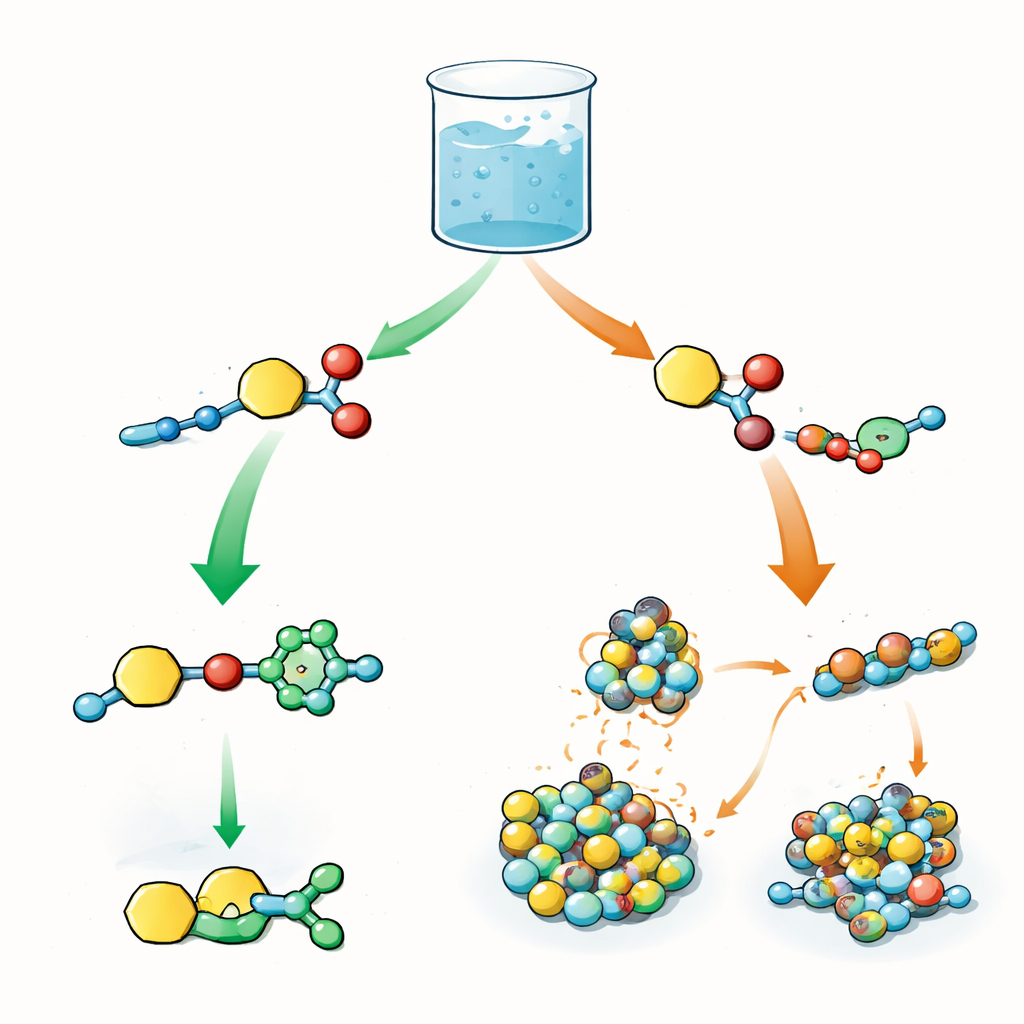
Twee rivaliserende reacties in één vat
De auteurs ontwerpen een centraal bouwblok dat twee reagerende elementen draagt: één die een "acyl"-groep kan overdragen (een klein chemisch fragment dat vaak wordt gebruikt om eiwitten te modificeren) en een ander dat een clickreactie kan ondergaan, de kopercatalyserende azide–alkyn cycloadditie. In hetzelfde bekerglas wordt dit bouwblok gemengd met aziden en korte peptiden die fungeren als nucleofielen, dat wil zeggen dat ze de acylgroep opnemen. In de biologie bepaalt de volgorde van zulke stappen—activering, overdracht en latere modificaties—hoe eiwitten zich gedragen. Hier is de vraag vergelijkbaar: wanneer beide reacties tegelijk mogelijk zijn, kiest het systeem dan eerst de clickreactie, eerst de acyloverdracht, of een menging van beide?
Trage zuurstof, snelle zwavel
Het team bestudeert eerst peptiden die tyrosine bevatten, een aminozuur met een zuurstofhoudende zijgroep. Onder licht basische omstandigheden gaat de clickreactie het snelst: de alkyn en azide binden snel, terwijl de acyloverdracht naar de tyrosine-zijgroep traag is en nauwelijks detecteerbare tussenproducten vormt. Verschillende click-afgeleide producten coëxisteren en er is weinig duidelijke tijdsafstand tussen de stappen. Wanneer de onderzoekers overschakelen naar cysteïne, een aminozuur met een zwavelhoudende zijgroep, keert het beeld zich om. Cysteïne vormt snel thioesters—zwavelgebonden acylproducten—die in hoge opbrengst verschijnen, ver voor er clickproducten zijn. Pas na vele uren beginnen clickproducten te ontstaan. Deze verschuiving komt doordat zwavel niet alleen reactiever is, maar ook koperionen vastzet, waardoor de katalysator tijdelijk bezet raakt en het clickpad als het ware "pauzeert".
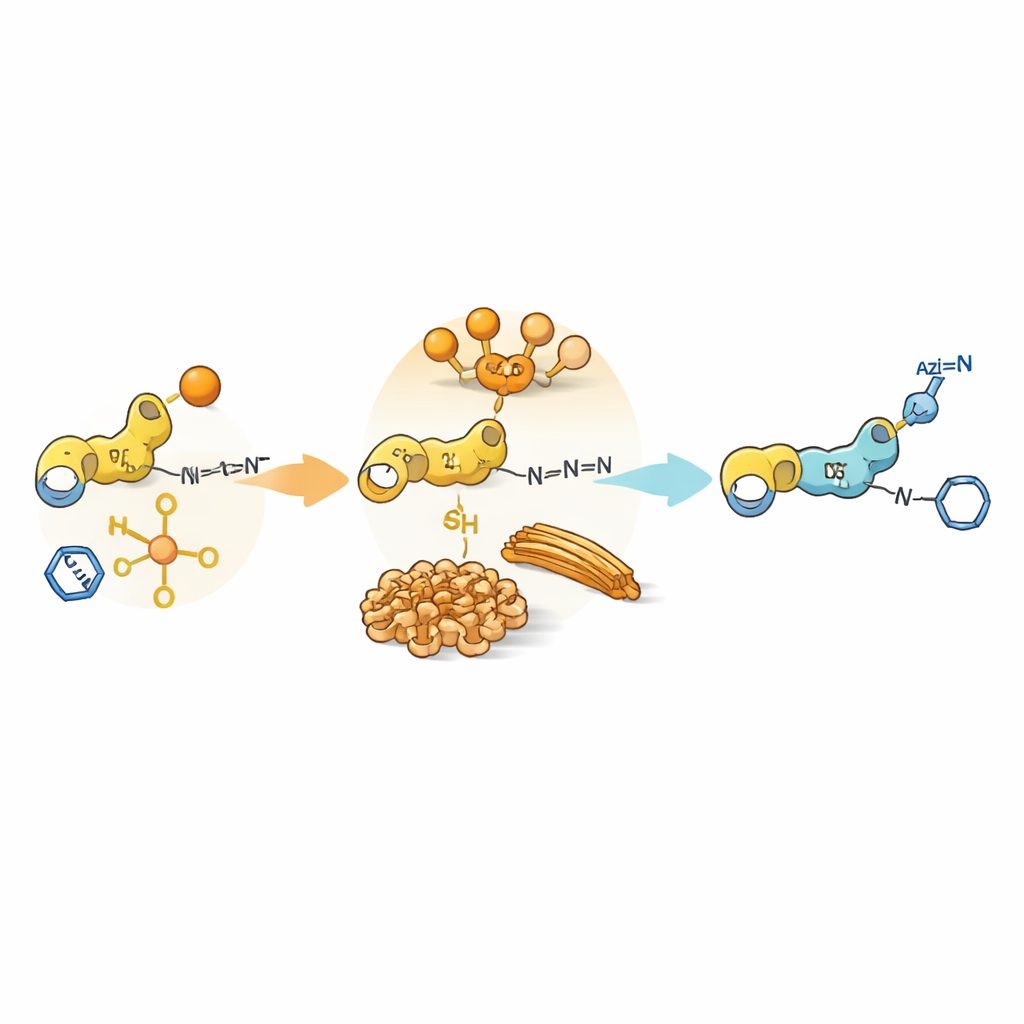
Zelfassemblage als een chemische poort
Buiten eenvoudige reactiviteit kunnen de peptiden zelf samenklonteren tot grotere structuren en zachte gels of vezels in water vormen. Deze assemblages creëren kleine domeinen waar sommige partners geconcentreerd zijn en anderen worden uitgesloten. Voor bepaalde dipeptiden met tyrosine of cysteïne die extra aromatische groepen dragen, verzamelen de tussenproducten zich tot fibrillen of dichte deeltjes. Binnen deze compacte regio’s wordt acyloverdracht bevoordeeld omdat nucleofiel en acyldonor naast elkaar zitten, terwijl de azide en kopercatalysator grotendeels in de omringende oplossing blijven. Hierdoor, hoewel de clickreactie intrinsiek snel is in vrije oplossing, wordt ze vertraagd doordat de katalysator de ingesloten reactieve sites moet bereiken. Deze "fase-mismatch" tussen waar de katalysator aanwezig is en waar de substraten zich bevinden verlengt de levensduur van geacyleerde tussenproducten en vertraagt het begin van de clickchemie.
Cascades en keuzemogelijkheden programmeren
Om te onderzoeken hoe ver ze deze ingebouwde planning kunnen sturen, ontwerpen de auteurs complexere situaties. In één geval bevat een enkel peptide zowel cysteïne als tyrosine, en biedt daarmee twee verschillende locaties voor acyloverdracht. De reactie verloopt als een drie-stappen cascade: eerst vormt zich een thioester op cysteïne, vervolgens verschuift een tweede acylgroep naar tyrosine, en pas na deze stappen verschijnen clickproducten. In een andere reeks experimenten concurreren twee verschillende aziden—één flexibel en alifatisch, de ander star en aromatisch—om hetzelfde reactieve centrum. Verrassend genoeg geeft het systeem consequent de voorkeur aan de alifatische azide, wat aantoont dat zelfs de vorm en elektronische eigenschappen van de azide kunnen bepalen welke producten domineren, terwijl de timing van de acyloverdracht onder peptidencontrole blijft.
Wat dit betekent voor toekomstige slimme materialen
In gewone bewoordingen laat dit werk zien hoe je meerdere, mogelijk concurrerende reacties in hetzelfde eenvoudige waterige mengsel kunt stoppen en toch kunt laten verlopen in een vooraf bepaalde volgorde—zonder enzymen, pompen of externe schakelaars. Door te kiezen of een peptide zuurstof of zwavel draagt, door zijn neiging tot zelfassemblage af te stemmen en door de aard van de azidepartner aan te passen, coderen de auteurs een soort interne klok in een klein chemisch netwerk. Vroege, omkeerbare acyloverdrachten scheppen kortlevende tussenproducten die bepalen wanneer en hoe de robuuste, bijna onomkeerbare clickstap plaatsvindt. Dergelijke geprogrammeerde reeksen kunnen de basis vormen voor slimme materialen en synthetische reactienetwerken die na verloop van tijd hun eigen paden "besluiten", vergelijkbaar met de nauwkeurig getimede chemie in levende cellen.
Bronvermelding: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Trefwoorden: clickchemie, acyloverdracht, supramoleculaire assemblage, reactienetwerken, peptidechemie