Clear Sky Science · nl
Single-cell multiomics onthult een endotheliale mechanogevoelige PIEZO1-IL-33-as die longfibrose aandrijft
Waarom stijve longen ertoe doen
Longfibrose is een verwoestende longaandoening waarbij ooit veerkrachtige luchtzakjes langzaam veranderen in stug littekenweefsel, waardoor elke ademhaling moeite kost. Artsen kunnen de ziekte momenteel alleen vertragen, niet stoppen of omkeren. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: hoe voelen de cellen die de bloedvaten in de longen bekleden dat het omliggende weefsel abnormaal stijf is, en hoe wordt die gewaarwording omgezet in meer littekenvorming? Door deze keten van gebeurtenissen terug te traceren tot op enkele cellen en individuele genen, ontdekken de onderzoekers een mechanische “schakelaar” in bloedvaten die mogelijk met geneesmiddelen te beïnvloeden is.
Van longfunctietests naar enkele cellen
Het team begon met longweefsel van mensen met idiopathische longfibrose, de meest voorkomende vorm van de ziekte, en van donoren met normale longen. Ze combineerden standaard longfunctiemetingen (hoeveel lucht iemand krachtig kan uitademen) met krachtige single-cell RNA-sequencing, waarmee wordt uitgelezen welke genen in duizenden individuele cellen actief zijn. Met een computationeel hulpmiddel dat bulk klinische gegevens koppelt aan single-cell profielen, bepaalden ze welke celtypen het sterkst geassocieerd waren met ernstig verminderde longfunctie. Vaat-endotheelcellen—de cellen die de binnenkant van bloedvaten vormen—staken er vooral uit bij patiënten met een longcapaciteit die minder dan de helft van normaal was. In deze endotheelcellen waren genprogramma’s gerelateerd aan "mechanische stress" consequent opgevoerd, wat suggereert dat abnormale fysieke krachten een deel van het probleem zijn.
Mechanische stress als een verborgen aanjager
Om te testen of deze link tussen stress‑waarneming en ziekte algemeen is, keerden de onderzoekers zich tot twee muismodellen van longlittekening: één geïnduceerd door het chemotherapeuticum bleomycine, de andere door langdurige blootstelling aan silicastof, een beroepsrisico. Met single‑cell methoden op deze experimentele longen vonden ze opnieuw dat endotheelcellen duidelijke signaturen van verhoogde mechanische stress droegen. In beide modellen, naarmate het omliggende longweefsel dikker en stijver werd, leek de bekleding van de bloedvaten over te schakelen naar een maladaptieve toestand. Deze convergentie tussen menselijke monsters en diermodellen versterkte het idee dat verstoorde fysieke krachten in de long, en niet alleen ontsteking of immuunactiviteit, centraal staan in hoe fibrose ontstaat en vordert.
Een druksensor met een cruciale rol
Dieper gravend zocht het team naar specifieke “mechanosensoren”—eiwitten die fysieke uitrekking omzetten in biochemische signalen—die omhooggereguleerd waren in gestresste endotheelcellen. Eén kanaaleiwit, genaamd PIEZO1, kwam herhaaldelijk naar voren als hoofdverdachte. Zowel bij muizen als bij mensen met fibrose waren PIEZO1-niveaus duidelijk hoger in vaat-endotheelcellen dan bij gezonde controles. Toen de onderzoekers muizen creëerden waarin PIEZO1 alleen in het endotheel verwijderd was, bleken deze dieren veel resistenter tegen bleomycine-geïnduceerde longlittekens: ze hadden minder collageenophoping, minder geactiveerde littekenvormende cellen en lagere niveaus van een chemische merker van fibrose. Farmacologisch blokkeren van PIEZO1 met een peptide-remmer verlichtte ook de littekenvorming, terwijl activering ervan fibrose verergerde—tenzij de receptor ontbrak in endotheelcellen. Samen toonden deze experimenten aan dat PIEZO1 in vaatbekledende cellen niet slechts een omstander is, maar een noodzakelijke aanjager van de ziekte.
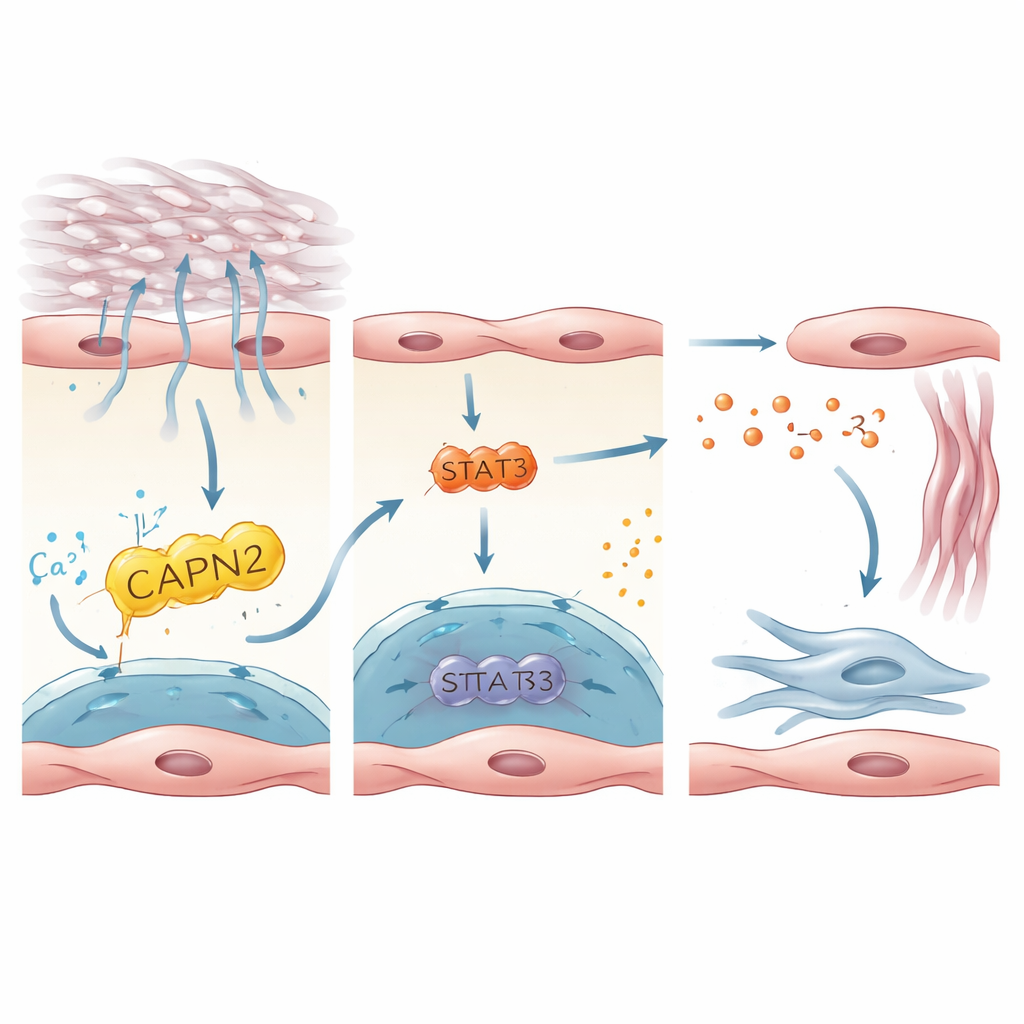
Een signaleringsketen die littekenvormende cellen activeert
De studie volgde vervolgens hoe PIEZO1‑activatie binnen endotheelcellen wordt vertaald naar signalen die fibroblasten wakker maken, de cellen die littekenweefsel aanleggen. Door menselijke en muisdatasets te integreren, richtten de auteurs zich op interleukine‑33 (IL‑33), een klein eiwit dat door gestresste of beschadigde cellen wordt vrijgegeven, als belangrijke boodschapper. IL‑33 werd sterk tot expressie gebracht in PIEZO1‑positieve endotheelcellen en was verhoogd in longen van patiënten en muizen met fibrose. In gekweekte menselijke endotheelcellen die op stijve substraten waren gekweekt of uitgerekt om ademhalen tegen een stijve long na te bootsen, verhoogde PIEZO1‑activatie de productie van IL‑33. Dit hing af van een downstream enzym, CAPN2, en een transcriptiefactor, STAT3, die samen de IL‑33-genactiviteit afstemden. Bij muizen beschermde het specifiek verwijderen van IL‑33 in endotheelcellen tegen fibrose, terwijl het geforceerd laten overproduceren van IL‑33 door endotheelcellen het beschermende effect van het verlies van PIEZO1 teniet deed. Deze resultaten schetsen een lineaire as: mechanische stress → PIEZO1 → CAPN2/STAT3 → IL‑33 → activatie van fibroblasten en littekenvorming.
Wat dit betekent voor toekomstige behandelingen
Voor niet‑specialisten is de boodschap dat longfibrose niet alleen wordt aangedreven door opstandige immuuncellen; het is ook een ziekte van foutieve “tastzin” in de bloedvaten. Endotheelcellen voelen dat hun omgeving te stijf is geworden, schakelen de PIEZO1‑schakelaar aan en geven als reactie IL‑33 vrij, een alarmsignaal dat nabijgelegen fibroblasten aanspoort om doorgaan met het aanleggen van littekenweefsel. Door deze keten van mechanische kracht tot genexpressie te ontleden, belicht het werk meerdere veelbelovende doelwitten—PIEZO1 zelf, het CAPN2‑STAT3‑relais en IL‑33—voor therapieën gericht op het onderbreken van de zelfversterkende cyclus van stijfheid en littekenvorming. Hoewel meer onderzoek nodig is om deze routes veilig bij mensen te moduleren, biedt deze mechanogevoelige endotheliale as een nieuw, fysiek gegrond perspectief om een ziekte aan te pakken die zich lange tijd aan doeltreffende behandeling heeft onttrokken.
Bronvermelding: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Trefwoorden: longfibrose, endotheelcellen, mechanotransductie, PIEZO1, IL-33