Clear Sky Science · nl
Aanpassingen in Plasmodium-tubuline bepalen verschillende microtubulusarchitecturen, mechanica en geneesmiddelfgevoeligheid
Waarom het skelet van malaria ertoe doet
Malariaparasieten overleven binnen menselijke bloedcellen, maar moeten zich ook kunnen persen door muggen en verschillende weefsels. Hiervoor vertrouwen ze op een interne steigerconstructie van microscopische buisjes, microtubuli genoemd. Deze studie stelt een eenvoudige maar krachtige vraag: hoe kunnen de microtubuli van de parasiet zo gespecialiseerd en stevig zijn terwijl hun basiselementen zo sterk lijken op die in onze eigen cellen? Het antwoord onthult niet alleen hoe de parasiet zijn vorm behoudt, maar ook hoe we mogelijk geneesmiddelen kunnen ontwerpen die zijn skelet aanvallen zonder dat die van ons wordt beschadigd. 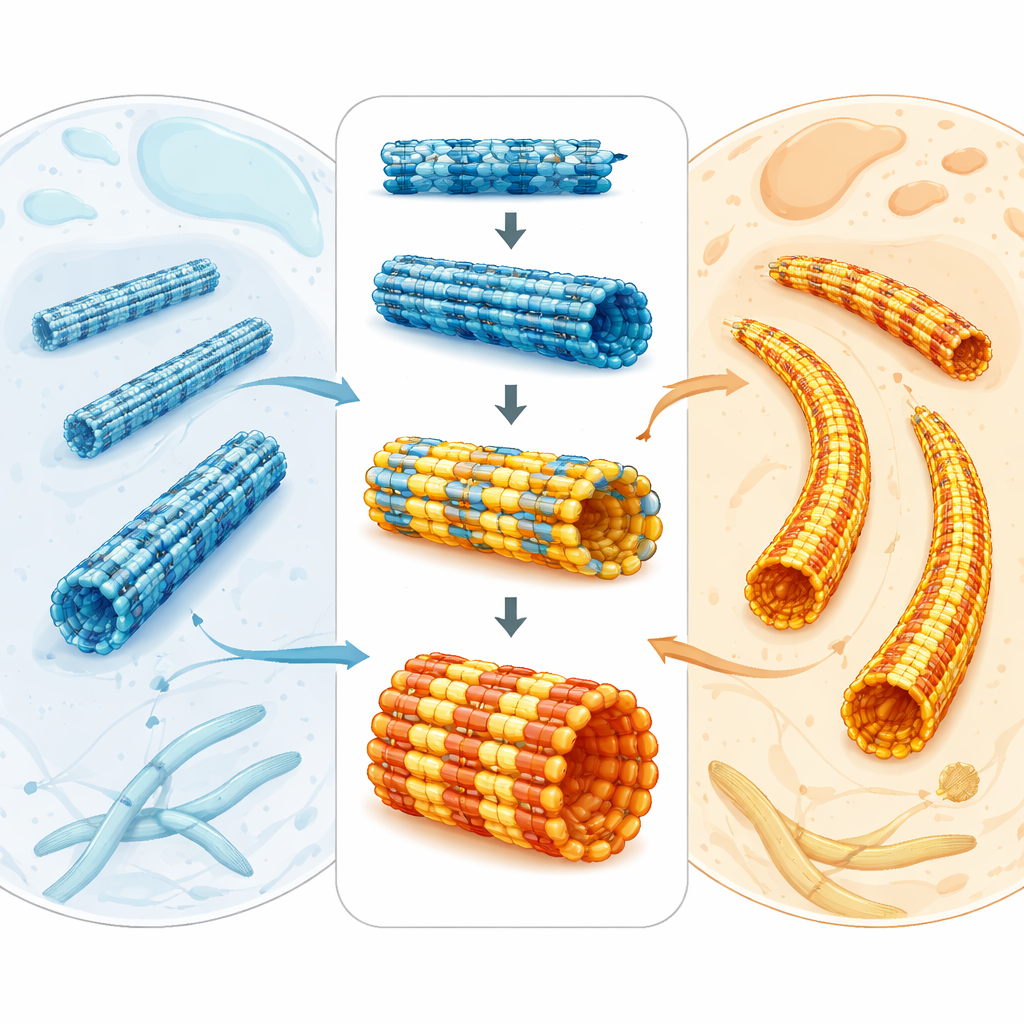
De piepkleine buisjes die een dodelijke parasiet vormgeven
Microtubuli zijn holle eiwitbuizen die cellen helpen delen, bewegen en hun vorm behouden. Ze zijn opgebouwd uit gepaarde eiwiteenheden, tubuline genoemd. Over dieren, planten en parasieten heen is tubuline verrassend gelijk, wat het moeilijk maakt te verklaren waarom microtubuli er in verschillende organismen zo verschillend uit kunnen zien en zich zo verschillend kunnen gedragen. In de malariaparasiet Plasmodium falciparum vormen microtubuli uiteenlopende netwerken: sommige zijn dynamisch en helpen bij celdeling, terwijl andere lange, stijve steunen vormen onder het buitenmembraan van de parasiet. Omdat deze structuren essentieel zijn voor groei en transmissie van de parasiet, vormen ze aantrekkelijke doelen voor antimalariamiddelen—zeker nu resistentie tegen bestaande behandelingen toeneemt.
Parasitaire tubuline zien op atomaire schaal
De onderzoekers zuiverden tubuline direct uit P. falciparum-parasieten en gebruikten hoogresolutie kryo-elektronenmicroscopie om te zien hoe het assembleert tot microtubuli. Ze vergeleken deze structuren met de goed bestudeerde microtubuli uit het mammalische brein. In eerste instantie lijkt parasitaire tubuline bijna identiek aan de menselijke versie en neemt het dezelfde algemene vouwing aan. Maar zorgvuldige vergelijking bracht clusters van kleine sequentievariaties aan het licht rond sleutelzakjes waar energiedragende moleculen (GTP en GDP) binden en waar bepaalde geneesmiddelen inwerken. Deze subtiele verschuivingen veranderen de positie van nabijgelegen helices en lussen, vooral aan het oppervlak van het tubulinedimeer waar andere eiwitten en medicijnen zich hechten. Het werk suggereert dat, hoewel het algemene ontwerp behouden blijft, lokale aanpassingen in de parasiet deze belangrijke sites subtiel hervormen.
Stijvere buisjes door sterkere zij-aan-zij verbindingen
Microtubuli zijn polymeren: vele tubulinedimeren stapelen zich eind-aan-eind tot protofilamenten, en meerdere protofilamenten liggen naast elkaar om de buiswand te vormen. Het team ontdekte dat bij parasitaire microtubuli de longitudinale contacten langs elk protofilament erg lijken op die in breinmicrotubuli. Het verschil verschijnt in de zijwaartse, of laterale, contacten tussen naburige protofilamenten. Hoewel het contactoppervlak in de parasiet eigenlijk iets kleiner is, tonen simulaties aan dat deze laterale verbindingen gezamenlijk sterker zijn, waardoor het rooster stijver wordt. Computer¬modellen van stukjes microtubuluswand lieten zien dat parasitaire tubuline minder buigt en draait dan breintubuline. Elektronentomografie van echte microtubuseinden bevestigde dat parasitaire microtubuli kortere, minder uitgespreide protofilamentkrullen hebben—een kenmerk van een steviger buis.
Ongebruikelijke buisgroottes die bij de parasiet passen
Een ander opvallend kenmerk van P. falciparum is dat in sommige levensstadia zijn microtubuli meer bouwstenen rond de omtrek bevatten dan de gebruikelijke 13 die in de meeste dierlijke cellen voorkomen—vaak 15 of zelfs 17 rijen protofilamenten. Het team reproduceerde dit gedrag in vitro door de nucleotide die tijdens assemblage gebruikt werd te veranderen. Met een GTP-achtig molecuul dat de groeiende toestand stabiliseert, gaf parasitaire tubuline van nature de voorkeur aan 15-protofilament-microtubuli. De auteurs bepaalden de structuur van deze dikkere buizen en toonden aan hoe ze de extra protofilamenten accommoderen door een lichte scheefstand van het rooster, maar toch vrijwel perfect cilindrisch blijven. Wanneer ze deze in het lab gemaakte 15-protofilamentbuizen vergeleken met die in parasietcellen, was de overeenkomst in vorm en afmetingen opmerkelijk nauw, wat aangeeft dat intrinsieke eigenschappen van de tubuline zelf—en niet noodzakelijk een menigte hulp-eiwitten—voldoende zijn om de kenmerkende architecturen van de parasiet te genereren.
Aanwijzingen voor toekomstige, parasiet-specifieke geneesmiddelen
De conclusie van de studie is dat evolutie de tubuline van de parasiet heeft fijngeslepen door kleine, verspreide sequentiewijzigingen die samen de mechanica, architectuur en geneesmiddelgevoeligheid van microtubuli veranderen. Deze aanpassingen maken de microtubuli van de parasiet stijver en in staat niet‑standaard buisgroottes te vormen die bij zijn veeleisende levenscyclus passen, terwijl het basale tubulineontwerp herkenbaar blijft. Belangrijk voor de geneeskunde is dat sommige geneesmiddelbindingsplaatsen vrijwel identiek lijken tussen parasiet en gastheer (zoals bij het kankerremmende paclitaxel), wat suggereert dat ze slechte doelen zijn voor selectieve antimalariamiddelen. Andere plekken, zoals het gebied waarvan gedacht wordt dat het het herbicide-achtige verbinding oryzalin bindt, vertonen zowel sequentieverschuivingen als subtiele structurele verplaatsingen die kunnen verklaren waarom parasitaire microtubuli daar gevoeliger zijn dan menselijke. Het in kaart brengen van deze genuanceerde verschillen biedt een routekaart voor het ontwerpen van toekomstige geneesmiddelen die het skelet van de malariaparasiet verstoren terwijl onze eigen cellen grotendeels ongemoeid blijven.
Bronvermelding: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Trefwoorden: malariaparasiet, microtubuli, tubuline-structuur, medicijndoelwitten, kryo-elektronenmicroscopie