Clear Sky Science · nl
Covalente warhead‑assemblage in fostriecin‑biosynthese omvat malonylatie‑lactonisatie door een bifunctionele thioesterase en enzymatische demalonylatie
Hoe de natuur een klein chemisch oorlogswapen bouwt
Kankergeneesmiddelen en antibiotica leunen vaak op een paar atomen die precies zo gerangschikt zijn — een klein “warhead” dat zich aan een eiwit vastzet en het uitschakelt. De natuurlijke verbinding fostriecin is zo’n molecuul en remt krachtig enzymen die betrokken zijn bij celgroei. Maar de complexe structuur maakt het moeilijk om het in het laboratorium te produceren of aan te passen. Deze studie onthult stap voor stap hoe bacteriën het cruciale warhead van fostriecin samenstellen en laat enzymtrucs zien die chemici nu kunnen gebruiken om nieuwe geneesmiddelen te ontwerpen.
De speciale haak in krachtige natuurlijke geneesmiddelen
Veel veelbelovende geneesmiddelen uit bodembacteriën behoren tot een familie die polyketiden heet. Binnen deze familie draagt een subgroep een reactieve ring die chemici kennen als een α,β‑onverzadigde δ‑lacton — die werkt als een moleculaire vis‑haak. Hij kan een permanente binding vormen met bepaalde aminozuren in eiwitten en zo belangrijke biologische schakelaars uitschakelen. In fostriecin en verwante moleculen is deze haak gekoppeld aan een fosfaatgroep die helpt om gericht bepaalde enzymen te vinden die de celdeling regelen. Deze eigenschappen maken ze aantrekkelijke antikankerleidende structuren, maar diezelfde reactiviteit en structurele complexiteit maken ze lastig te synthetiseren en onstabiel bij opslag.
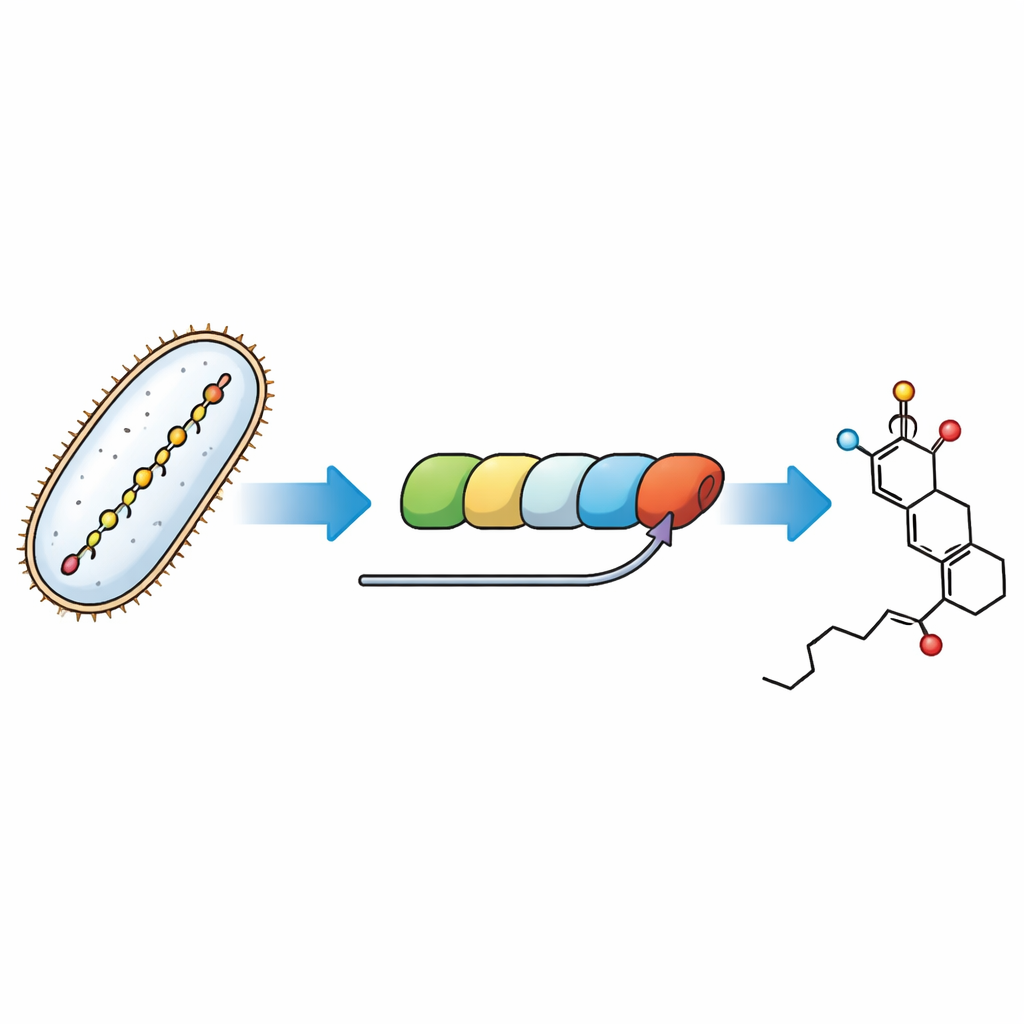
De laatste stappen van een moleculaire assemblagelijn volgen
Bacteriën bouwen fostriecin met een enorme modulaire eiwitmachine, een polyketidesynthase — een assemblagelijn waarbij elk station de groeiende koolstofketen verlengt en vormt. De puzzel die hier wordt aangepakt is hoe het laatste module van deze machine de warhead‑ring smeedt en een tijdelijke “greep”, een malonylgroep, aanbrengt die later verwijderd moet worden. Door de route na te bootsen in reageerbuizen met gezuiverde enzymen en zorgvuldig ontworpen kleine moleculaire stand‑ins voor de natuurlijke tussenproducten, konden de onderzoekers individuele stappen volgen en toewijzen aan specifieke onderdelen van de assemblagelijn.
Een multitaskend enzym met een onverwachte vaardigheid
Het team ontdekte dat het laatste station van de assemblagelijn, een domein genaamd FosTE, zich gedraagt op een manier die eerder niet was gezien. Typische versies van dit domein knippen gewoon afgewerkte producten van de lijn af. FosTE daarentegen pakt eerst een malonylfragment van een veelvoorkomend cellulair bouwblok en heft het over op een precies zuurstof‑atoompunt van de groeiende keten, en helpt vervolgens de keten om te buigen zodat die sluit tot de warhead‑ring. Het muteren van een enkele reactieve serine‑aminozuur in FosTE schakelt beide activiteiten uit. Structurele modellering wijst op twee positief geladen arginine‑resten in het actieve centrum die het malonylfragment omvatten en positioneren voor overdracht — functies die normaal door een ander type enzym worden uitgevoerd. Het veranderen van deze arginines in neutrale residuen wist de malonyl‑overdrachtsstap uit terwijl de basale ringvorming grotendeels intact bleef, wat hun cruciale rol bevestigt.
Het warhead vergrendelen en verspilling voorkomen
Zodra de ring is gevormd en zijn tijdelijke malonylgroep draagt, moet een ander enzym, FosM, deze groep verwijderen om het volledig bewapende warhead bloot te leggen. De studie toont aan dat FosM efficiënt werkt alleen nadat nog een ander enzym, een brede‑specificiteitskinase genaamd FosH, een fosfaat aan een nabijgelegen positie op het molecuul heeft toegevoegd. Wanneer de onderzoekers de gemalonyleerde ring aan FosM alleen aanboden, trad slechts een bescheiden omzetting op. FosH eerst toevoegen leidde tot bijna volledige verwijdering van de malonylgroep en de vorming van de finale reactieve eenheid. Belangrijk is dat FosH ook fosforylering kan uitvoeren op verwante “shunt”‑tussenproducten die ontstaan door nevenreacties, waardoor deze worden gered zodat ze correct kunnen worden verwerkt in plaats van verloren te gaan als doodlopende producten.
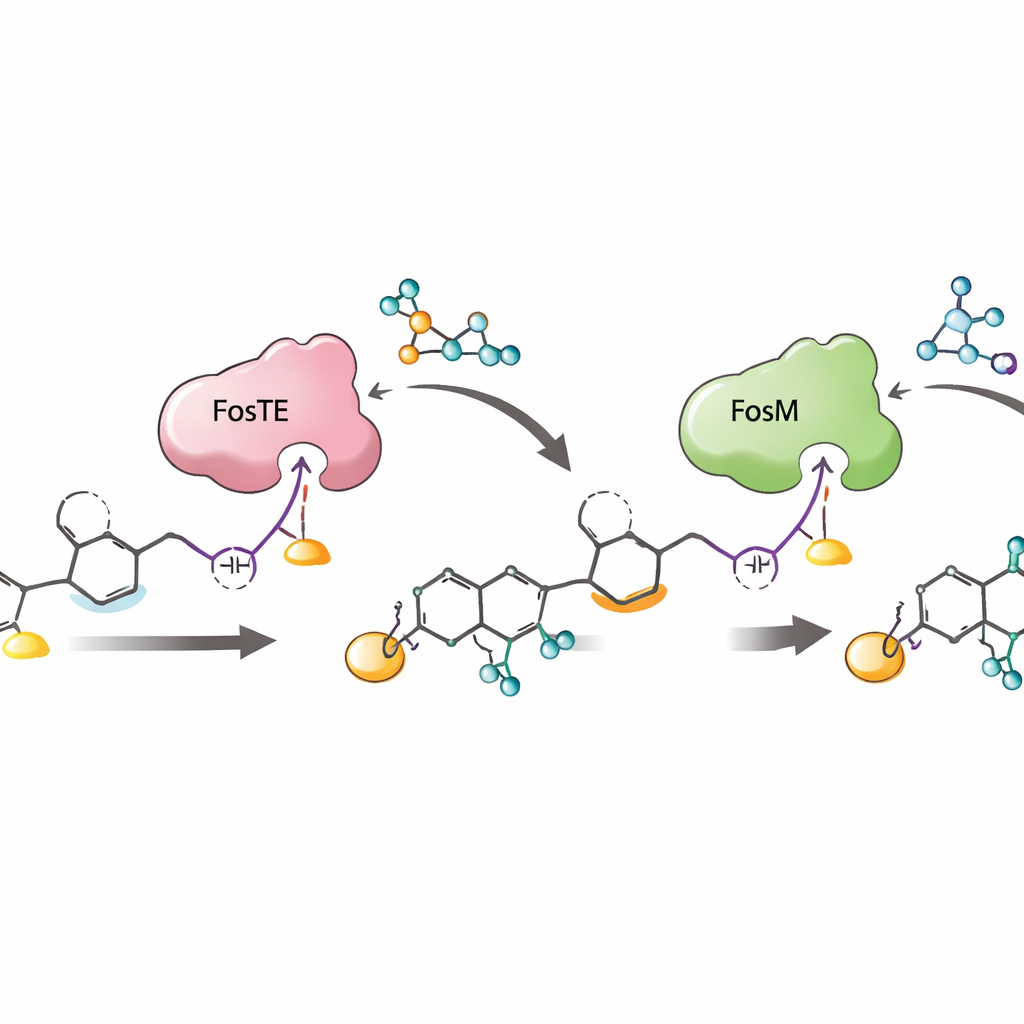
Waarom deze enzymatische choreografie ertoe doet
Gezamenlijk laat het werk een strak georkestreerde volgorde zien: ketenverlenging op de assemblagelijn, FosTE‑gedreven malonyltoevoeging en ringsluiting, FosH‑fosforylering, en tenslotte FosM‑gestuurde demalonylatie. Deze volgorde bouwt het delicate warhead niet alleen efficiënt op, maar beschermt ook instabiele tussenproducten tegen afbraak en maximaliseert de productie van de gewenste gefosforyleerde vorm die het meest actief is als geneesmiddel‑lead. Door te laten zien hoe een enkel enzymdomein zowel een groeiend molecuul kan versieren als vrijmaken — en hoe partnerenzymen reactieve tussenproducten fijnregelen en herstellen — biedt de studie een blauwdruk voor het ontwerpen van nieuwe polyketiden met warheads en voor het bouwen van kortere, efficiëntere synthetische routes naar complexe antikankermiddelen zoals fostriecin.
Bronvermelding: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Trefwoorden: fostriecin, polyketide biosynthese, enzymengineering, natuurlijke product‑warheads, chemo‑enzymatische synthese