Clear Sky Science · nl
Translationele regulatie via oxidatieve desulfuratie van tRNA-modificaties
Hoe cellen de eiwitproductie bijsturen onder stress
Elke cel moet beslissen welke eiwitten worden gemaakt, hoe snel dat gebeurt en wanneer het proces vertraagd moet worden. Deze studie onthult een subtiele chemische schakel op transfer-RNA (tRNA)-moleculen die cellen helpt de eiwitproductie terug te schroeven wanneer de omgeving van de cel meer oxiderend wordt, zoals tijdens ontsteking of metabole stress. Door te volgen hoe deze schakel zich gedraagt in zoogdiercellen en in in vitro-systemen, laten de onderzoekers een nieuwe manier zien waarop schadeachtige veranderingen aan RNA daadwerkelijk als regulatoir signaal kunnen dienen.
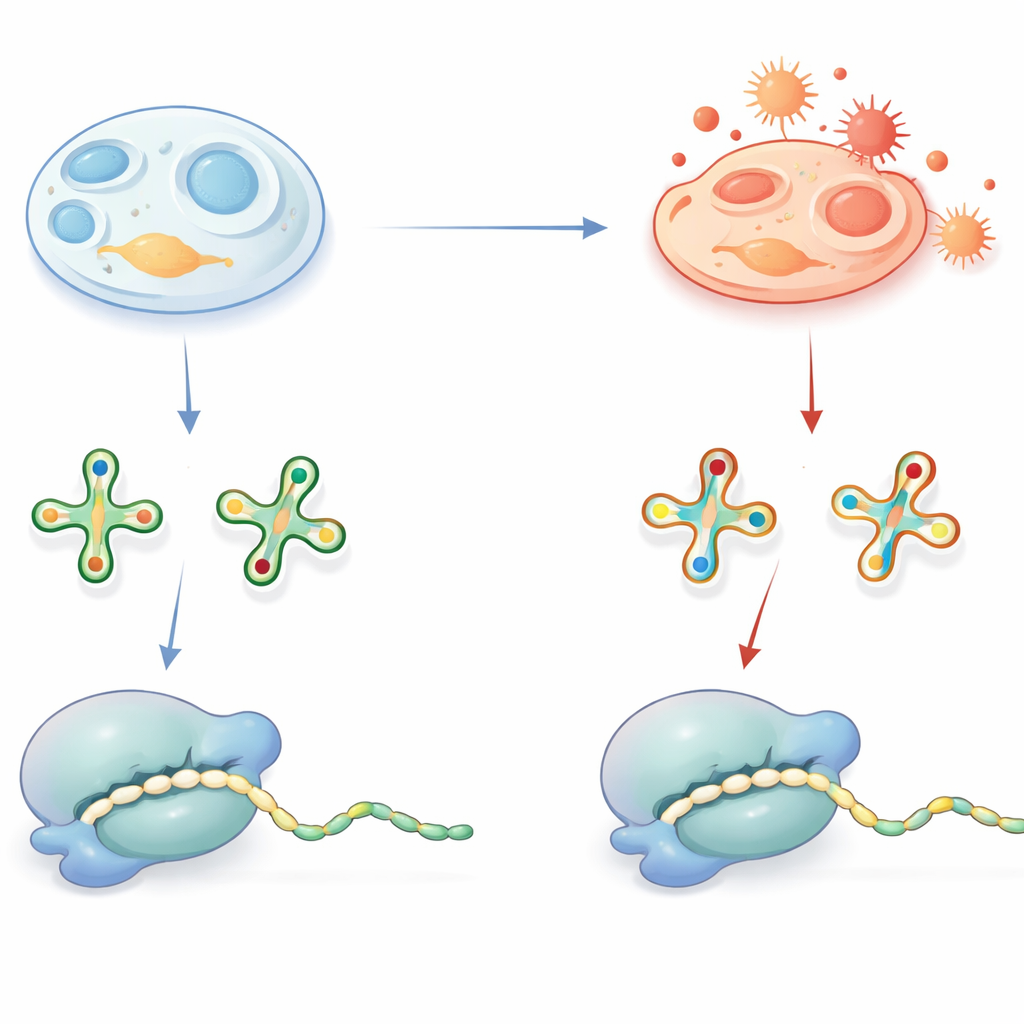
Kleine markeringen op tRNA met grote gevolgen
tRNA’s fungeren als adapters die drie-letterwoorden in boodschapper-RNA lezen en de bijpassende aminozuren aanleveren tijdens eiwitsynthese. Om dit nauwkeurig en efficiënt te doen, dragen veel tRNA’s speciale chemische versieringen, met name op een sleutelpositie die contact maakt met de derde letter van elk codon. Een veelvoorkomende versiering is een zwavelhoudende groep op een uridinebase, vaak aangeduid als een 2-thiouridine-afgeleide. Onder normale omstandigheden helpt deze zwavelgroep tRNA’s de juiste codons die eindigen op A of G te herkennen en ondersteunt zij snelle, foutloze translatie. Defecten in deze versieringen zijn al bekend als oorzaken van menselijke ziekten, wat hun belang onderstreept.
Wanneer oxidatieve stress tRNA herschrijft
De zwavelgroep die het decoderen versterkt heeft ook een keerzijde: ze is chemisch kwetsbaar voor oxidatie. Het team vroeg zich af of deze groep binnen cellen tatsächlich wordt verwijderd onder oxiderende omstandigheden, en wat dat zou betekenen voor de eiwitsynthese. Met gevoelige massaspectrometrie identificeerden zij geoxideerde, zwavelvrije versies van deze tRNA-basen — zogeheten h2U-afgeleiden — in muwweefsel, varkensmitochondriën, bacteriën, gist en verschillende humane cellijnen. Een slimme spike-in-experiment met een bacterieel tRNA-tracer toonde aan dat deze h2U-markeringen geen artefacten van de preparatie zijn, maar binnen levende cellen gevormd worden. Hoewel de geoxideerde versies slechts in een fractie van de tRNA’s voorkwamen, varieerde hun hoeveelheid tussen weefsels en celtypen, wat suggereert dat de intracellulaire redoxtoestand en het antioxidantvermogen bepalen hoe vaak deze conversie optreedt.
Hoe geoxideerde tRNA’s de assemblagelijn vertragen
Vervolgens testten de onderzoekers hoe deze gewijzigde tRNA’s presteren tijdens eiwitsynthese. Ze zetten de zwavelhoudende vorm chemisch om in de geoxideerde h2U-vorm in bulk tRNA en gebruikten een volledig gereconstitueerd humaan translatiesysteem in vitro. Een reporter-eiwit wiens productie sterk afhankelijk is van deze gemodificeerde tRNA’s vertoonde een scherpe afname wanneer de tRNA’s gedesulfureerd waren, terwijl een controle-reporter die de getroffen codons ontwijkt gewoon goed werd vertaald. Biochemische assays verklaarden waarom: geoxideerde tRNA’s voor lysine, glutamine en glutamaat werden veel minder efficiënt opgeladen met hun aminozuren, terwijl de overeenkomstige arginine-tRNA’s grotendeels gespaard bleven. Belangrijk is dat tRNA’s met h2U nog steeds in ribosoomgebonden (polysomale) fracties uit cellen voorkwamen, wat aangeeft dat ze wel deelnemen aan translatie, maar dat ze dat slecht doen.
Een structurele blik op verzwakt decoderen
Om precies te zien hoe oxidatie het decoderen verandert, gebruikte het team hoogresolutie cryo-elektronenmicroscopie om bacteriële ribosomen te imageren geprogrammeerd met humaan lysine-tRNA en specifieke codons. In de normale, zwavelhoudende staat vormt de gemodificeerde base op de tRNA-wobblepositie ofwel een standaard basepaar met een A-eindigend codon of een speciaal wobble-paar met een G-eindigend codon, beide stevig ingebed in het ribosoomdecoderingcentrum. Na desulfuratie kon dieselde base slechts één zwak contact maken met het A-eindigende codon en vormde ze een minder stabiel wobble-paar met het G-eindigende codon. Bindingsexperimenten kwamen overeen met deze structuren: geoxideerd lysine-tRNA verloor praktisch het vermogen het AAA-codon te herkennen en herkende het AAG-codon veel minder efficiënt. Samen tonen deze bevindingen aan dat een ogenschijnlijk kleine chemische wijziging kan leiden tot codon-specifieke vertragingen in eiwitsynthese.
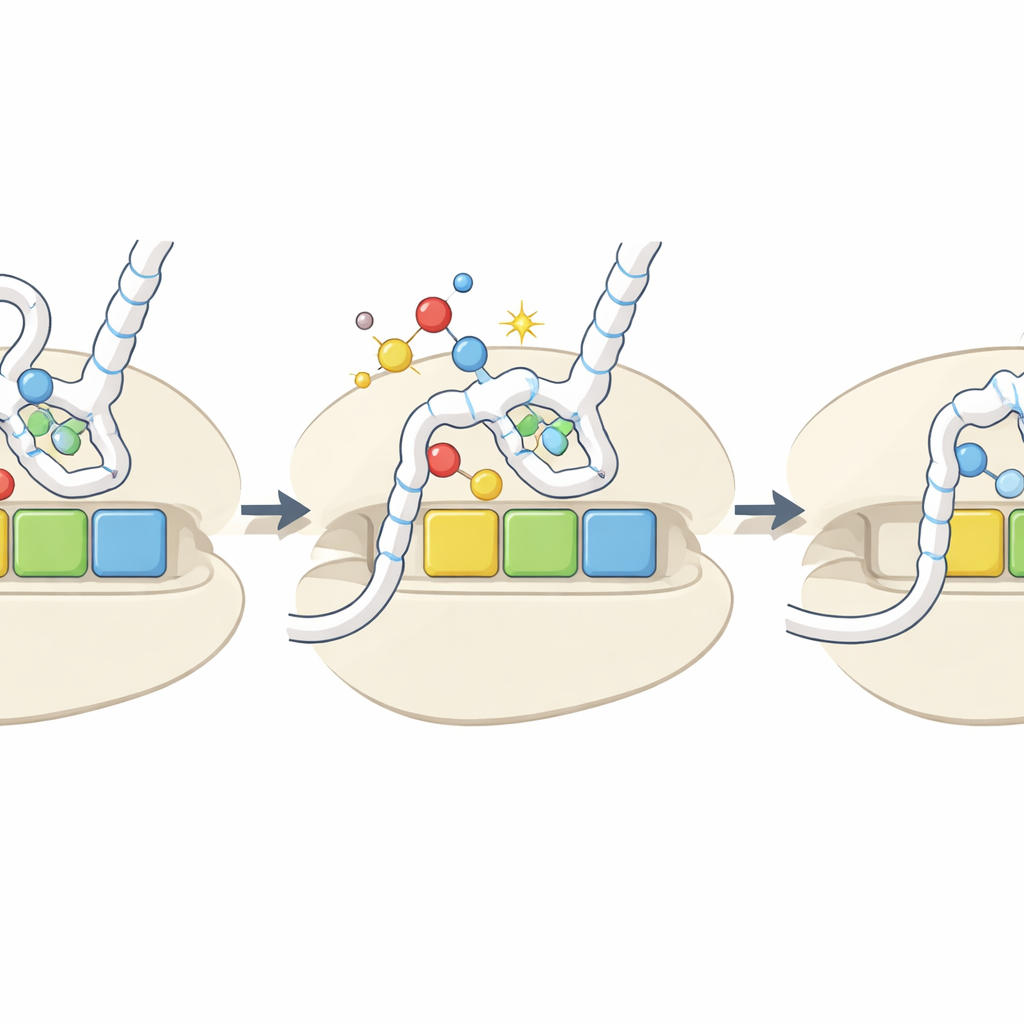
Een schadelijk signaal dat een regelknop wordt
Al met al stellen de auteurs voor dat de oxidatieve verwijdering van zwavel uit sleutelbasen van tRNA functioneert als een ingebouwde sensor voor de redoxomgeving van de cel. Onder oxidatieve stress worden meer tRNA’s omgezet naar de h2U-vorm, die slecht worden opgeladen en zwak binden aan bepaalde codons. Dit vertraagt selectief de translatie bij die codons, wat mogelijk de stabiliteit van de getroffen mRNA’s verandert, de vouwing van eiwitten beïnvloedt en stressresponsroutes triggert wanneer ribosomen vastlopen. Hoewel de geoxideerde markeringen relatief zeldzaam zijn en hun niveaus niet altijd duidelijk stijgen onder experimentele stress, betekenen hun codon- en aminozuurspecifieke effecten dat zelfs bescheiden veranderingen kunnen herverdelen welke eiwitten worden gemaakt, en hoe snel, onder uitdagende omstandigheden.
Bronvermelding: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Trefwoorden: tRNA-modificatie, oxidatieve stress, eiwitsynthese, regulatie van translatie, RNA-schade