Clear Sky Science · nl
Het richten op tRNA-afhankelijke tyrosine-gebruik onthult een metabole kwetsbaarheid in hepatocellulair carcinoom
Kankercellen uithongeren van een algemeen bouwsteen
Leverkankercellen, zoals alle snel delende cellen, hebben een constante aanvoer van aminozuren nodig—de kleine bouwstenen van eiwitten. Deze studie toont aan dat hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker, een onverwachte zwakte bezit: het is sterk afhankelijk van het aminozuur tyrosine voor zowel energieproductie als overleving. Door selectief te beperken hoe kankercellen tyrosine gebruiken, konden de onderzoekers tumorgroei vertragen, de energiecentrales van kankercellen beschadigen en een vorm van celdood activeren die mogelijk kan worden benut voor nieuwe behandelingen.
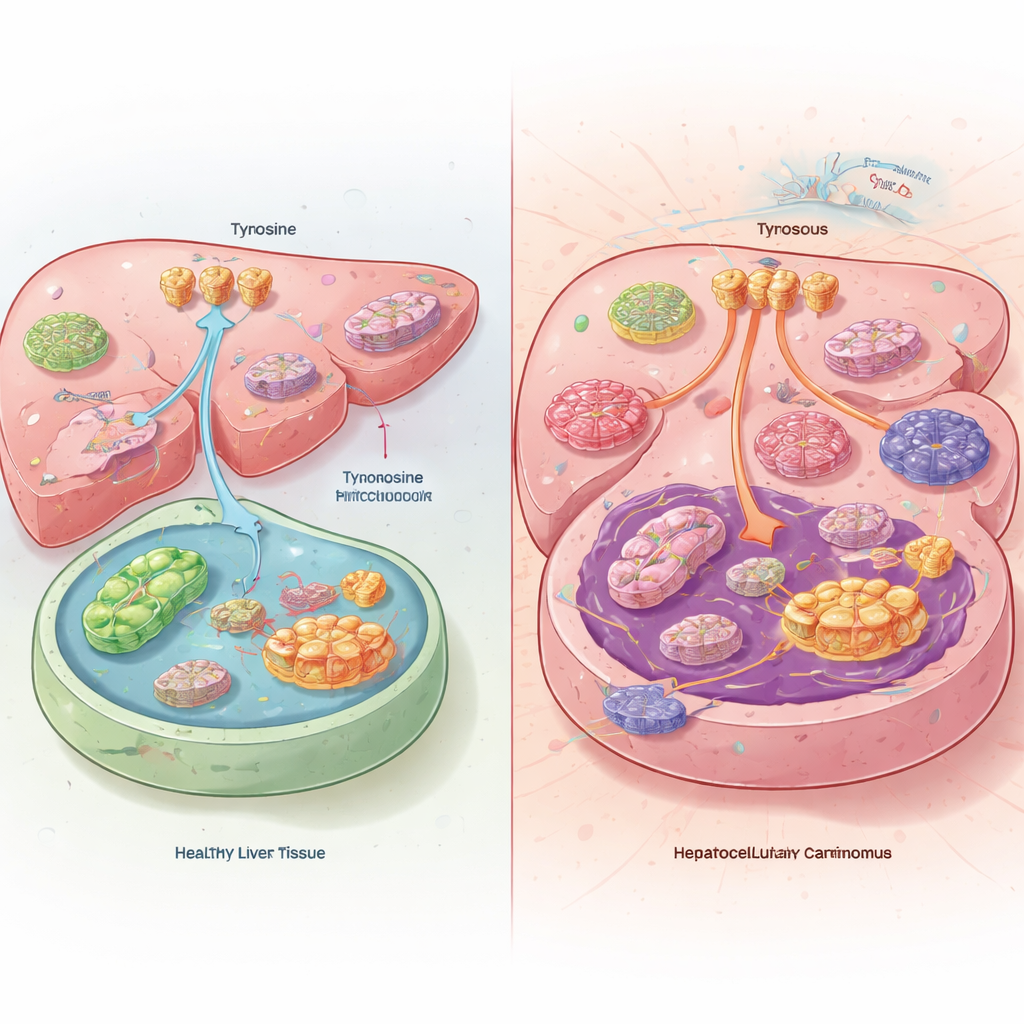
Een verborgen onevenwicht in levertumoren
Toen het team levertumoren vergeleek met gezond leverweefsel van patiënten en muizen, vonden ze iets puzzelends. Binnen de kankercellen waren de tyrosinewaarden eigenlijk laag, hoewel de tumoren meer tyrosine uit de bloedbaan opnamen en het minder afbraakten. In plaats van tyrosine als brandstof te verbranden, leidden levertumoren het om naar eiwitproductie. De kankers realiseerden dit door de activiteit van tyrosinetransporteurs aan het celoppervlak te verhogen en de enzymen die normaal tyrosine in de lever afbreken omlaag te schakelen. Muizen die een tyrosinevrij dieet kregen, ontwikkelden kleinere tumoren en leefden langer, terwijl extra tyrosine in het dieet hun kankers sneller liet groeien.
Hoe kanker eiwitproductie herprogrammeert
De onderzoekers traceerden deze tyrosinehonger naar een krachtig kankergendrijver genaamd MYC. In levertumoren schakelt MYC een eiwit aan dat YARS1 heet, dat tyrosine koppelt aan een specifiek transfer-RNA (tRNA-TyrGUA). Dit geladen tRNA is wat ribosomen nodig hebben om tyrosinerijke eiwitten te bouwen. De studie toonde aan dat levertumoren zowel YARS1 als het bijbehorende tRNA opvoeren, waarmee ze een bevoorrechte pijplijn van tyrosine naar eiwitsynthese garanderen. Het verstoren van deze pijplijn—ofwel door tyrosineniveaus te verlagen, YARS1 of tRNA-TyrGUA neer te schakelen, of het laden van tyrosine te blokkeren—maakte levertumorcellen veel minder fit in kweek en in muizen, wat een metabole kwetsbaarheid onthult die nauw samenhangt met hun hoge behoefte aan eiwitproductie.
De energiecentrales en vetbalans lamleggen
Door genoombrede metingen van RNA, eiwitproductie en metabolieten te combineren, identificeerde het team twee bijzonder gevoelige doelen van tyrosinerestrictie. Ten eerste is NDUFB8 een component van mitochondriaal complex I, een kernonderdeel van de energieproducerende machinerie van de cel. Ten tweede helpt SCD1 verzadigde vetten omzetten in enkelvoudig onverzadigde vetten die veiliger zijn om op te slaan in celmembranen en vetdruppels. Wanneer tyrosine voor translatie werd beperkt, daalde de productie van NDUFB8 en SCD1 terwijl hun RNA-niveaus grotendeels onveranderd bleven—duidelijke aanwijzing dat de translatie, niet de genexpressie, werd getroffen. Dit leidde tot slecht samengestelde complex I, verminderde cellulare respiratie, overtollige reactieve zuurstofsoorten en een verschuiving in vetten van enkelvoudig onverzadigde naar kwetsbaardere meervoudig onverzadigde vormen die gemakkelijk geoxideerd worden.
Kankercellen dwingen naar een ijzer-gedreven dood
De gecombineerde mitochondriale schade en onstabiele vetten duwden levertumorcellen richting ferroptose, een ijzerafhankelijke vorm van celdood die wordt aangedreven door lipideperoxidatie. De tumoren probeerden terug te vechten door natuurlijke ferroptoseblokkers zoals GPX4 en verwante moleculen te verhogen, maar een grote CRISPR-genbewerkingenscreen toonde aan dat het uitschakelen van deze beschermers tyrosinerestrictie nog dodelijker maakte. In cel- en muismodellen zorgde het combineren van tyrosynelimiterende strategieën met geneesmiddelen die GPX4 of BCL2 remmen—of met bestaande leverkankergeneesmiddelen zoals sorafenib en venetoclax—voor sterkere tumorgroei-remming, kleinere tumorladingen en langere overleving.
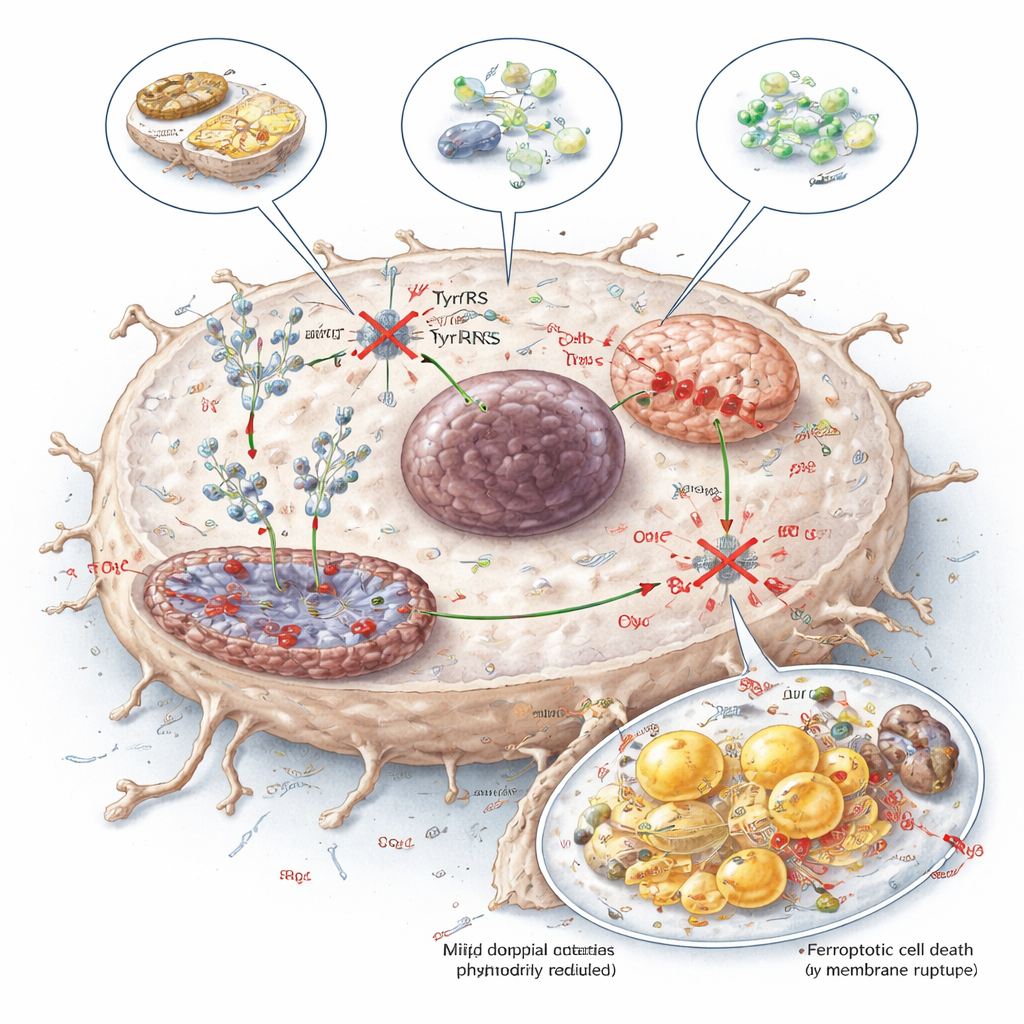
Een metabole zwakte omzetten in therapie
Om praktische manieren te onderzoeken om deze zwakte te benutten, testten de onderzoekers drie benaderingen: een tyrosinebeperkt dieet, een enzym (TAL) dat tyrosine enzymatisch afbreekt, en een klein molecuul genaamd tyrosinol dat concurreert met tyrosine voor binding aan YARS1. Alle drie verminderden de beschikbaarheid van tyrosine voor eiwitsynthese, verlaagden NDUFB8- en SCD1-niveaus, schaadden mitochondriale functie en verhoogden ferroptose in levertumoren, terwijl ze beheersbare effecten op normale weefsels bij muizen lieten zien. Voor een leek is de boodschap dat levertumoren lijken vast te zitten aan tyrosine, niet alleen als voedingsstof, maar als een precieze brandstof voor hun eiwitmakende machinerie. Het richten op deze afhankelijkheid—via dieet, enzymen of geneesmiddelen—biedt een veelbelovende nieuwe manier om tumoren te verzwakken en de werking van bestaande behandelingen te versterken.
Bronvermelding: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Trefwoorden: leverkanker, aminozuurmetabolisme, tyrosine, mitochondriën, ferroptose