Clear Sky Science · nl
Analyse van olfactorische spleetbiopsie van de pathobiologie van de ziekte van Alzheimer over ziektefasen heen
Waarom de neus aanwijzingen voor geheugenverlies kan bevatten
Veel mensen merken dat hun reukvermogen achteruitgaat lang voordat geheugenproblemen verschijnen, en artsen vermoeden al lang een verband met de ziekte van Alzheimer. Deze studie stelt een eenvoudige maar krachtige vraag: als reukgerelateerd weefsel in de neus zowel gemakkelijk bereikbaar is als nauw verbonden met de hersenen, zou het dan een vroeg, levend venster op de Alzheimer-biologie kunnen bieden — jaren voordat dementie ontstaat?
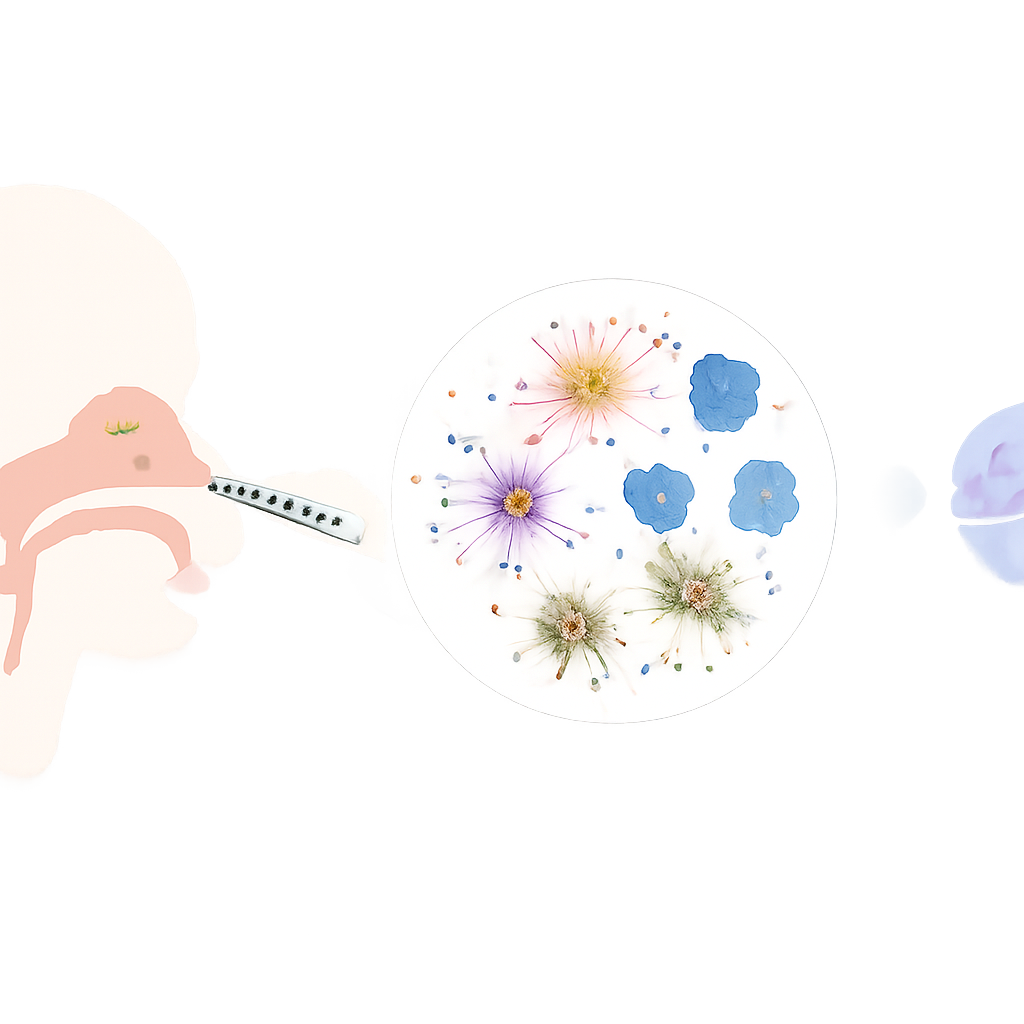
Een zachte borstel in de neus
De onderzoekers concentreerden zich op een klein gebied hoog in de neusholte dat het olfactorisch epitheel wordt genoemd, waar de zenuwcellen die geuren detecteren zich bevinden. Met een dun, flexibel borsteltje dat door een neusendoscoop werd geleid, schraapten ze dit gebied voorzichtig bij wakkere vrijwilligers tijdens een poliklinisch bezoek en verzamelden zo duizenden levende cellen per persoon. Ze namen drie soorten deelnemers op: mensen met normaal denken en normale ruggenmergvloeistoftesten voor Alzheimer; mensen waarvan de ruggenmergvloeistof stilletjes vroegtijdige Alzheimer aangaf maar die nog cognitief normaal testten ("preklinische" fase); en mensen met zowel abnormale ruggenmergvloeistof als geheugen- of denkproblemen (klinische Alzheimer).
Cel-voor-cel activiteit lezen
Uit deze kleine borstelsamples voerde het team single-cell RNA-sequencing uit, een techniek die leest welke genen in individuele cellen aanstaan. Dit stelde hen in staat niet alleen de reukzenuwcellen zelf te catalogiseren, maar ook lokale immuuncellen zoals T-cellen en myeloïde cellen (inclusief microglia-achtige cellen en macrofagen) die het weefsel bewaken. In totaal analyseerden ze meer dan 220.000 cellen. Door genactiviteitspatronen tussen de drie groepen te vergelijken, zochten ze naar veranderingen die vroeg ontstonden en sterker werden naarmate de ziekte vorderde, met focus op tekenen van ontsteking en stress in zowel zenuw- als immuuncellen.
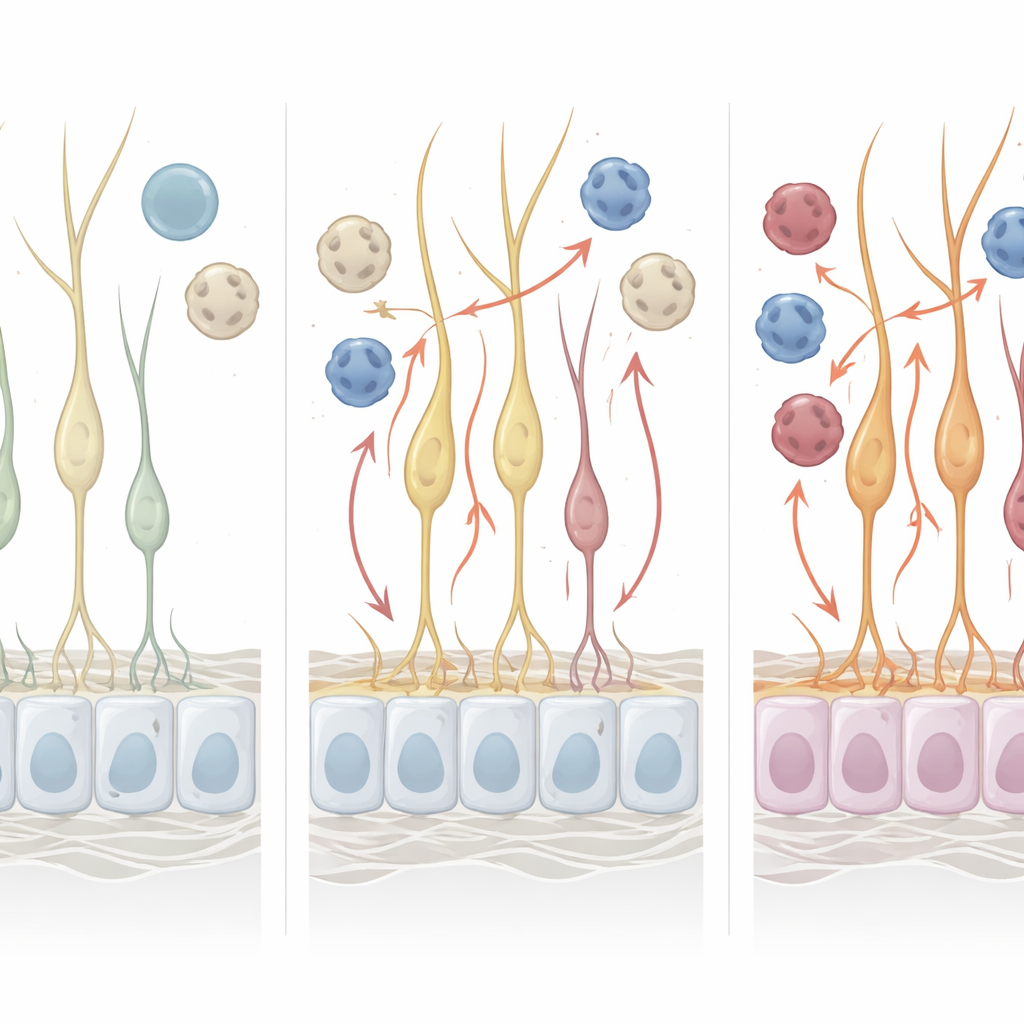
Immuuncellen geven een vroeg alarm
Een van de duidelijkste signalen kwam van T-cellen, een belangrijke component van het immuunsysteem. In de vloeistof rond de hersenen en het ruggenmerg had eerder werk ongewoon actieve CD8-geheugencellen aangetoond bij mensen met Alzheimer. Deze studie vond dat soortgelijke T-cellen in het reukweefsel van de neus al abnormaal geactiveerd waren in de preklinische groep, voordat symptomen verschenen. Myeloïde cellen in hetzelfde weefsel toonden eveneens opkomende inflammatoire programma’s die sterker werden bij klinische Alzheimer, waaronder verhoogde activiteit van genen die gelinkt zijn aan immuunrisicofactoren in de hersenen. Deze immuunverschuivingen suggereren dat het olfactorische slijmvlies het hersengerelateerde ontstekingsbeeld weerspiegelt en mogelijk zelfs bijdraagt aan ontsteking in de hersenen die bij de ziekte wordt gezien.
Gestreste reukzenuwcellen en wisselwerking met het immuunsysteem
De reukzenuwcellen zelf lieten genveranderingen zien die wijzen op beschadiging en veranderde communicatie met nabijgelegen immuuncellen. Sommige genen die oxidatieve stress en inflammatoire signalering kunnen bevorderen, waren verhoogd, terwijl andere genen die normaal helpen bij het beheren van vetachtige moleculen en mogelijk beschermen tegen amyloïdophoping, waren verlaagd. Toen het team modelleerde hoe neuronen en immuuncellen met elkaar zouden kunnen communiceren, vonden ze sterkere voorspelde paden voor inflammatoire moleculen in zowel preklinische als klinische stadia. Dit patroon schetst een beeld van voortdurende, tweerichtingscommunicatie: immuuncellen die actiever worden, en neuronen met stresssignaturen die hen kwetsbaarder kunnen maken.
Een neusmomentopname van vroege ziekte
Om deze complexe patronen naar iets bruikbaars te vertalen, combineerden de wetenschappers de meest informatieve genen uit zowel immuun- als neuronale cellen in één "module-score" voor de biopsie van elke persoon. Deze samengestelde score onderscheidde mensen met zowel preklinische als klinische Alzheimer van gezonde controles met goede nauwkeurigheid, en liep parallel met de hoeveelheid amyloïde-gerelateerde verandering in de ruggenmergvloeistof. Omdat de test toegankelijk weefsel gebruikt en herhaald kan worden in de tijd, biedt het een veelbelovende manier om ziektebiologie te volgen in een vroeger, mogelijk behandelbaarder stadium dan wat met hersenweefsel zelf mogelijk is.
Wat dit voor patiënten kan betekenen
De studie suggereert dat een snelle borstelbiopsie in de neus dezelfde soorten inflammatoire en neuronale stresssignalen kan vastleggen die zich diep in de hersenen ontvouwen bij de ziekte van Alzheimer — en dat deze signalen detecteerbaar zijn voordat geheugenproblemen optreden. Hoewel grotere, langlopende studies nodig zijn om deze benadering te bevestigen en te verfijnen, opent het werk de deur naar het gebruik van olfactorisch neusslijmvlies als vroeg waarschuwingssysteem en onderzoeksplatform. In de toekomst zouden dergelijke biopsies kunnen helpen risicovolle personen te identificeren, selectie voor preventieve behandelingen te sturen en nieuwe doelen te onthullen om schadelijke neuro-immuunactiviteit te kalmeren voordat blijvende schade ontstaat.
Bronvermelding: D’Anniballe, V.M., Kim, S., Finlay, J.B. et al. Olfactory cleft biopsy analysis of Alzheimer’s disease pathobiology across disease stages. Nat Commun 17, 2245 (2026). https://doi.org/10.1038/s41467-026-70099-7
Trefwoorden: Ziekte van Alzheimer, reukzin, olfactorisch epitheel, neuro-inflammatie, vroege detectie