Clear Sky Science · nl
Systematische identificatie van variant-specifieke RNA-structuur–kleinmolecuulinteracties geïllustreerd met RNA G-quadruplexen
Waarom kleine veranderingen in RNA belangrijk zijn voor toekomstige medicijnen
De meesten van ons erven kleine verschillen in ons DNA die ons uniek maken. Deze minieme veranderingen kunnen subtiel de vouwing van RNA-moleculen in onze cellen veranderen. De nieuwe studie introduceert een manier om te zien hoe zulke genetische variaties de grijpkracht van experimentele medicijnen die op RNA gericht zijn, beïnvloeden. Dat is belangrijk omdat hetzelfde medicijn bij de ene persoon heel anders kan werken dan bij een ander, vooral bij kanker of erfelijke aandoeningen.
Nieuwe methode om te zien waar medicijnen RNA raken
Veel geneesmiddelontwikkelaars richten zich nu op RNA, niet alleen op eiwitten, als therapeutische doelen. Kleinmoleculen kunnen zich vasthechten aan specifieke RNA-vormen en bepalen hoe genen worden afgelezen, maar tot nu toe werkten de meeste methoden alleen op een enkele ‘referentie’-RNA-sequentie. Ze negeerden grotendeels de ontelbare éénletterveranderingen die bij echte patiënten voorkomen. De auteurs ontwikkelden een hoogdoorvoerbenadering genaamd BIVID-MaP die gelijktijdig duizenden RNA-varianten kan testen en kan vaststellen waar een klein molecuul aan elk van hen bindt, tot op enkelvoudig-nucleotide-niveau. 
Chemische markeringen omzetten in een leesbaar signaal
BIVID-MaP werkt in drie hoofdstappen. Ten eerste koppelt het team een reactief label aan een RNA-bindend klein molecuul. Wanneer dit gelabelde verbindingje zich nestelt in zijn voorkeurs-RNA-structuur, zoals een compacte G-quadruplex gevormd door guanine-rijke sequenties, vormt het label een permanente chemische binding met een nabijgelegen RNA-basis. Ten tweede kopieert een speciaal enzym het gemodificeerde RNA naar DNA. Wanneer het enzym zo’n chemische markering tegenkomt, slaat het vaak één base over, waardoor er een kleine deletie in de kopie ontstaat. Ten derde leest diepe sequencing deze deletiesignaturen uit over miljoenen moleculen. Omdat bijna de hele omliggende sequentie bewaard blijft, kunnen de deleties nauwkeurig worden toegewezen aan specifieke genetische varianten in een gemengde pool.
De methode bewijzen met een gecontroleerd testgeval
Om te bevestigen dat BIVID-MaP daadwerkelijk variant-specifieke binding detecteert, bestudeerden de onderzoekers een RNA-segment van het CD44-gen dat normaal een G-quadruplex vormt. Een enkele G-naar-A-verandering verstoort deze structuur. In een mengsel met beide versies toonde alleen de intacte vorm sterke deletiesignalen in de buurt van het gevouwen gebied wanneer deze werd blootgesteld aan een berberine-gebaseerde probe, en onafhankelijke tests bevestigden daar sterkere binding. De mutant, die niet dezelfde vorm kan aannemen, leverde veel minder deleties en zwakkere binding op. Andere gangbare mappingtechnieken misten dit verschil of gaven verwarrende achtergrond, wat de verbeterde gevoeligheid en specificiteit van de nieuwe benadering benadrukt.
Scannen van kankergeassocieerde mutaties over veel genen
Het team schaalde de methode vervolgens op. Ze bouwden een RNA-bibliotheek van 5′ ongetransleerde regions (5′ UTRs) uit 283 kankegerelateerde genen, elk gekoppeld aan reële somatische mutaties die in tumoren zijn gerapporteerd. Met een probe die G-quadruplex-achtige structuren herkent, onthulde BIVID-MaP talrijke mutaties die de binding van kleinmoleculen zowel versterkten als verzwakten. In genen zoals DAXX en ING2 veranderden éénletterveranderingen in guanine-rijke reeksen de binding sterk, in overeenstemming met onafhankelijke biofysische tests van G-quadruplexvorming en directe bindingsmetingen met massaspectrometrie. In sommige gevallen verschoven mutaties buiten de voor de hand liggende G-tracks de binding nog steeds door subtiel te wijzigen hoe waarschijnlijk het is dat nabijgelegen basen paren, waardoor het structurele ‘ensemble’ werd hervormd zonder de voorspelde algehele vouwing grofweg te veranderen. 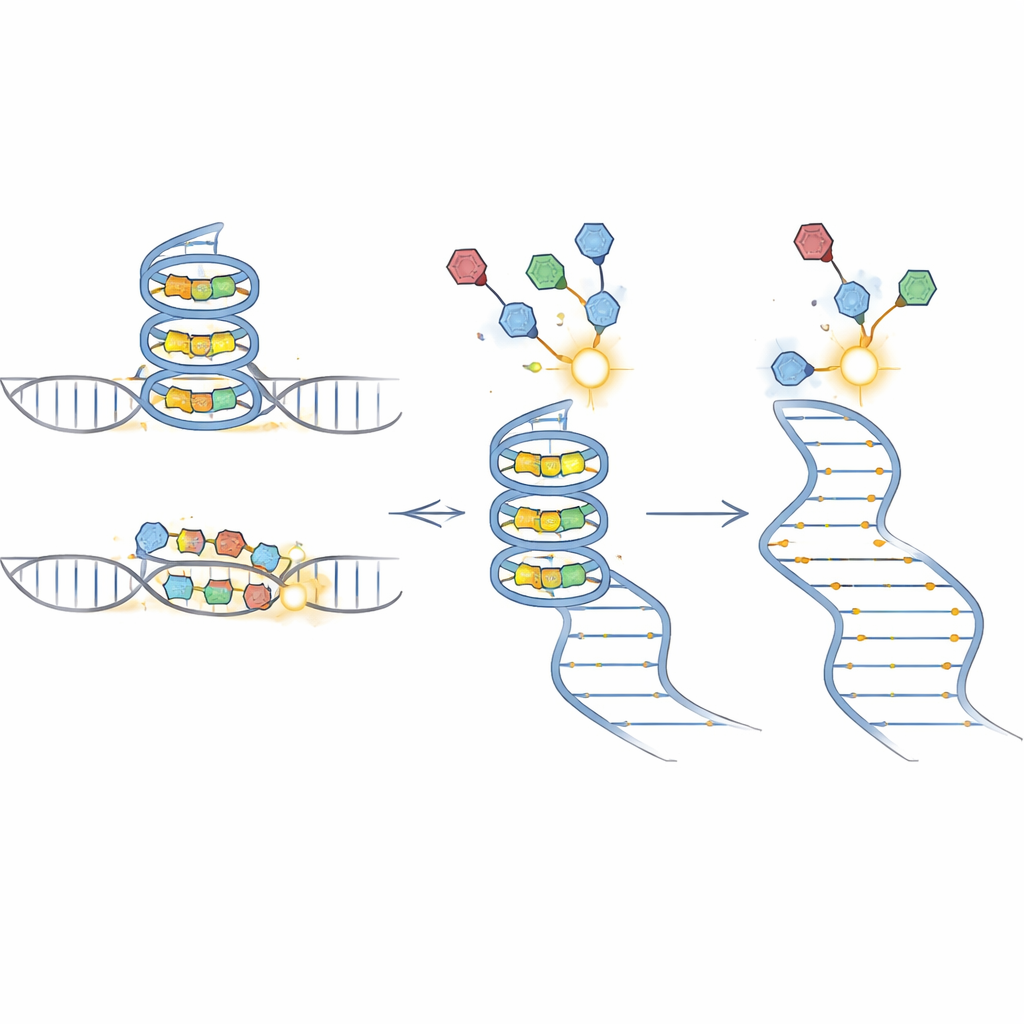
Wat computervoorspellingen missen
Belangrijk is dat bestaande voorspellingsinstrumenten voor RNA-structuur en G-quadruplexen vaak faalden in het voorspellen van de veranderingen die BIVID-MaP aan het licht bracht. Sommige varianten die computationeel weinig effect leken te hebben, veroorzaakten in de praktijk grote verschillen in binding. Andere leken de binding te beïnvloeden voor een hele klasse van G-quadruplex-targetende verbindingen, terwijl bepaalde mutaties drugspecifieke effecten hadden. Dit toont aan dat enkelvoudige-nucleotidevarianten het landschap van RNA-vouwingen en geneesmiddelcontacten kunnen afstemmen op manieren die moeilijk uit sequentie alleen af te leiden zijn.
Betekenis voor gepersonaliseerde RNA-geneesmiddelen
De auteurs concluderen dat BIVID-MaP een krachtig middel biedt om in kaart te brengen hoe individuele genetische verschillen RNA-structuren en hun interacties met kleinmoleculaire medicijnen herschikken. Door lokale chemische modificaties om te zetten in precieze deletiesignaturen kan de methode duizenden varianten parallel onderzoeken en die aanwijzen die de geneesmiddelbinding wezenlijk veranderen. Op lange termijn zouden dergelijke kaarten het ontwerp van RNA-georiënteerde medicijnen kunnen sturen die effectiever en veiliger zijn voor diverse patiënten, en eerder verborgen RNA-structuren onthullen die als nieuwe medicijndoelen zouden kunnen dienen.
Bronvermelding: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Trefwoorden: RNA-gerichte geneesmiddelen, G-quadruplex, genetische varianten, binding van kleinmoleculen, kankermutaties