Clear Sky Science · nl
Optimalisatie van de ruimtelijke organisatie van FtsZ-ringen voor grootschalige constrictie in synthetische cellen
Waarom kleine ringen belangrijk zijn voor het bouwen van synthetische cellen
Stel je voor dat je een eenvoudige, kunstmatige cel bouwt die uit zichzelf kan groeien en zich in tweeën kan splitsen. Om dat voor elkaar te krijgen, moeten onderzoekers leren hoe ze een zacht, zeepbelachtig membraan gecontroleerd kunnen samenknijpen met slechts een paar biologische onderdelen. Deze studie laat zien hoe een bacterieel eiwit geholpen kan worden grote, stabiele ringen te vormen op reusachtige vetbellen, waardoor deze model-"cellen" bijna tot deling kunnen samentrekken. Het onthult welk type eiwitarchitectuur nodig is om een membraan op de schaal van een hele cel te buigen en te hervormen.
Deelname aan de natuurlijke delingsgereedschapskist
Veel bacteriën delen met behulp van een eiwit genaamd FtsZ, een verre verwant van tubuline die het inwendige skelet van onze eigen cellen opbouwt. FtsZ assembleert tot filamenten die zich groeperen in een ring op het midden van de cel, en aangeeft waar de cel zal splitsen. In levende bacteriën hechten een hele reeks helper-eiwitten deze ring aan het binnenmembraan, positioneren ze deze in het midden en verbinden ze de ring met enzymen die de celwand omvormen. Eerdere laboratoriumpogingen om deze machinerie na te bootsen in grote, celgrootte vesikels slaagden erin ringen te vormen en kleine deuken in het membraan te veroorzaken, maar niet een vloeiende, progressieve constrictie die een reusachtige vesikel herschikt tot twee bijna afzonderlijke helften.
Een minimalistische benadering van een delende schelp
De auteurs vroegen zich af of ze dit systeem konden terugbrengen tot slechts twee onderdelen: een versie van FtsZ die direct aan membranen kan hechten, en een korte positief geladen staart van een ander delingseiwit, FtsN. Zij kapselden deze componenten in giant unilamellar vesicles — holle bolletjes van lipiden die op vereenvoudigde cellen lijken — en voorzagen ze van de energiemolecuul GTP en een traagwerkende GTP-analoga om de eiwitdynamiek bij te sturen. Zonder de FtsN-staart vormde FtsZ veel kleine ringen en vlekken die slechts lokale deukjes veroorzaakten. Met een overschot aan het FtsN-fragment (genoemd cytoFtsN) reorganiseerden die kleine ringen zich tot een enkele, grote ring die rond de vesikel nabij de evenaar lag en over enkele uren kon samentrekken.
Van verward netwerk naar enkele contractiele ring
Om te begrijpen hoe dit kleine peptide het gedrag zo ingrijpend verandert, observeerde het team FtsZ-filamenten op vlakke, ondersteunde membranen met hogeresolutiemicroscopie. Gewoonlijk vormt FtsZ op zulke oppervlakken zwervende, gebogen vortices. Het toevoegen van toenemende hoeveelheden cytoFtsN veegde deze spiralen geleidelijk weg en verving ze door rechtelijniger, meer gealigneerde bundels. Kwantitatieve beeldanalyse bevestigde dat het netwerk coherenter en ordelijker werd naarmate de peptideconcentratie steeg. Fluorescentie-herstelexperimenten toonden aan dat subeenheden binnen deze bundels langzamer uitgewisseld werden, wat aangeeft dat het peptide de filamenten stabiliseert en hun dynamische omwenteling vermindert.

Electrostatische "Velcro" die filamenten aan elkaar vastzet
Biochemische metingen toonden aan dat cytoFtsN en FtsZ voornamelijk via tegengestelde elektrische ladingen op elkaar inwerken: FtsZ is overwegend negatief, terwijl het peptide clusters van positieve ladingen draagt. Bij lagere zoutconcentraties hechtte het peptide sterker, bevorderde de vorming van dikkere FtsZ-bundels in oplossing en vertraagde het de afbraak van filamenten door de GTP-afbrekende activiteit van het eiwit te dempen. Toen de onderzoekers sleutelresiduen met positieve lading in het peptide veranderden, of de zoutconcentratie verhoogden om de elektrostatische aantrekking te schermen, verdwenen de bundelings- en reorganisatie-effecten. Dit wijst op een eenvoudige fysieke verklaring waarbij het positief geladen peptide fungeert als moleculair "Velcro", waardoor de afstoting tussen FtsZ-filamenten vermindert zodat ze zij aan zij kunnen pakken tot stijve bundels.
Hoe een enkele ring een reusachtige vesikel hervormt
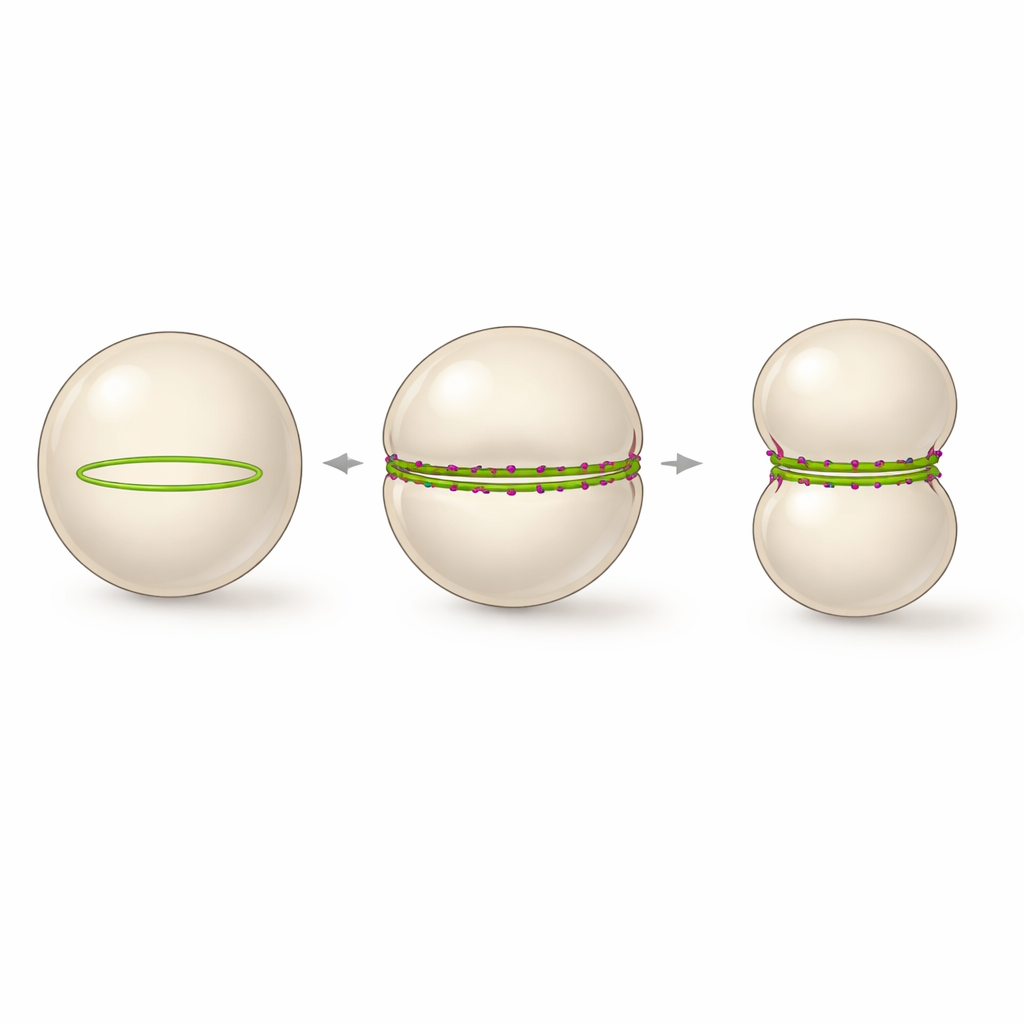
Binnen vesikels heeft dit door het peptide gestabiliseerde bundelen een opvallend gevolg. In plaats van veel kleine gebogen ringen, worden de rechtgetrokken FtsZ-bundels gedwongen de grote kromming van de vesikel te volgen en assembleren ze zich tot één continue ring die de hele omtrek overspant. Tijdsopnamen lieten zien dat telkens wanneer zo'n volledig gesloten ring gevormd werd, de vesikel betrouwbaar vervormde van een bol naar een haltervorm, met een nauwe taille waar de ring zat. Het proces kon in realtime gevolgd worden terwijl de vesikeldiameter kromp en de constrictie verdiept werd, bijna het compartiment in tweeën splijtend, hoewel uiteindelijke scissies niet bereikt werden. De auteurs stellen voor dat een stabiele, evenaaroverspannende FtsZ-ring met vertraagde maar nog steeds actieve turnover de minimale architectuur is die nodig is om grootschalige membraanconstrictie in een synthetische cel te bewerkstelligen.
Wat dit betekent voor toekomstige synthetische vormen van leven
Door aan te tonen dat een membraan-ankerde FtsZ-variant plus een kort cationisch peptide reusachtige lipidevesikels bijna tot deling kan hervormen, definieert dit werk een duidelijke ontwerprichtlijn voor kunstmatige cellen: een enkele, coherente proteïnering die past bij de grootte van de cel en mechanisch stabiel blijft in de tijd is voldoende om een zachte grens op cellulaire schaal samen te knijpen. Complexere factoren kunnen nog steeds nodig zijn om het membraan volledig door te snijden, maar de studie demonstreert dat gecontroleerde grootschalige constrictie geen volledige cast van bacteriële delingseiwitten vereist. In plaats daarvan kan zorgvuldige afstemming van filamentorganisatie en -dynamiek een eenvoudig proteïneraamwerk veranderen in een effectief contractiel ringmechanisme, waardoor echt zelf-delende synthetische cellen een stap dichterbij komen.
Bronvermelding: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Trefwoorden: synthetische celverdeling, FtsZ-ring, membraanconstrictie, minimaal divisoom, cytoskeletale zelforganisatie