Clear Sky Science · nl
Subcellulaire proteomics onthult een blauwdruk voor endosymbiontintegratie in de trypanosomaat Angomonas deanei
Verborgen partners in eencellig leven
Veel eencellige organismen leven niet echt alleen. Sommige herbergen bacteriën die permanent binnenin hen verblijven, waarbij ze voedsel en diensten ruilen in relaties die echoën van de oorsprong van onze eigen mitochondriën. Deze studie onderzoekt zo’n samenwerking in Angomonas deanei, een microscopische insectenparasiet, om te laten zien hoe een ooit vrijlevende bacterie diep verweven is geraakt met de interne werking van de gastheercel.
Van logé naar ingebouwd onderdeel
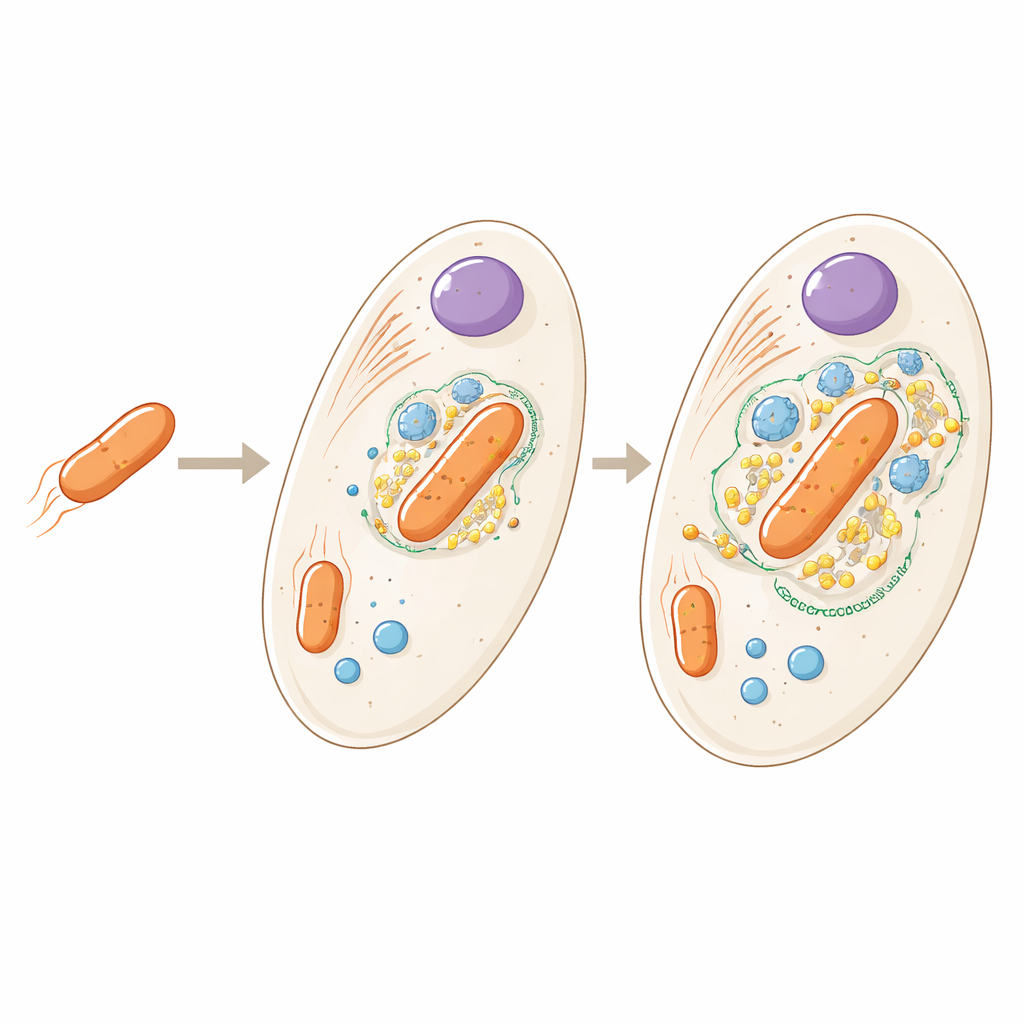
De bacterie die binnenin Angomonas deanei leeft is een verre verwant van vrijlevende bodemmicroben, maar hier komt hij voor als één exemplaar per gastheercel en kan hij niet meer zelfstandig overleven. Eerder werk toonde aan dat de gastheer speciale eiwitten produceert die in de bacterie binnengaan en zelfs helpen bij het controleren van wanneer die deelt. De nieuwe studie stelt een bredere vraag: als we de hele cel overzien, waar bevinden alle gastheer- en bacteriële eiwitten zich precies, en wat vertelt dat ons over hoe nauw de twee partners geïntegreerd zijn?
De binnenstad van de cel in kaart
Om dit te beantwoorden, braken de onderzoekers grote aantallen cellen heel voorzichtig open zodat interne structuren grotendeels intact bleven. Ze scheidden deze delen vervolgens door ze bij verschillende snelheden te centrifugeren en identificeerden duizenden eiwitten in elke fractie met behulp van hoogresolutie massaspectrometrie. Door te vergelijken hoe eiwitten over de fracties klusterden, en dit te controleren met bekende markers en fluorescerende microscopie, creëerden ze een gedetailleerd "adresboek" voor de cel en konden bijna 3.000 eiwitten worden toegekend aan 21 onderscheiden regio’s zoals de kern, het mitochondrion, gespecialiseerde opslaglichaampjes en de bacteriële endosymbiont zelf.
Gereedschap van de gastheer gericht op de inwoning-bacterie
Binnen deze atlas ontdekte het team een set door de gastheer gemaakte eiwitten die consequent met de endosymbiont meereisden, waarmee de bekende verzameling van zogenoemde endosymbiont-gerichte eiwitten werd uitgebreid. Een nieuw bevestigd voorbeeld, ETP10 genoemd, bekleedt de bacterie vergelijkbaar met een eerder beschreven eiwit, wat wijst op een scaffold van gastheerselementen rond de microbiele partner. Een andere kleine groep eiwitten deelde een ongewoon fysisch gedrag met een dynamine-achtig eiwit dat al bekendstaat om de bacterie tijdens deling af te knijpen. Samen suggereren deze bevindingen een gespecialiseerd, door de gastheer gebouwd mechanisme dat gewijd is aan het positioneren, vormen en reproduceren van de endosymbiont binnen de cel.
Energie-uitwisseling en chemische handelsroutes
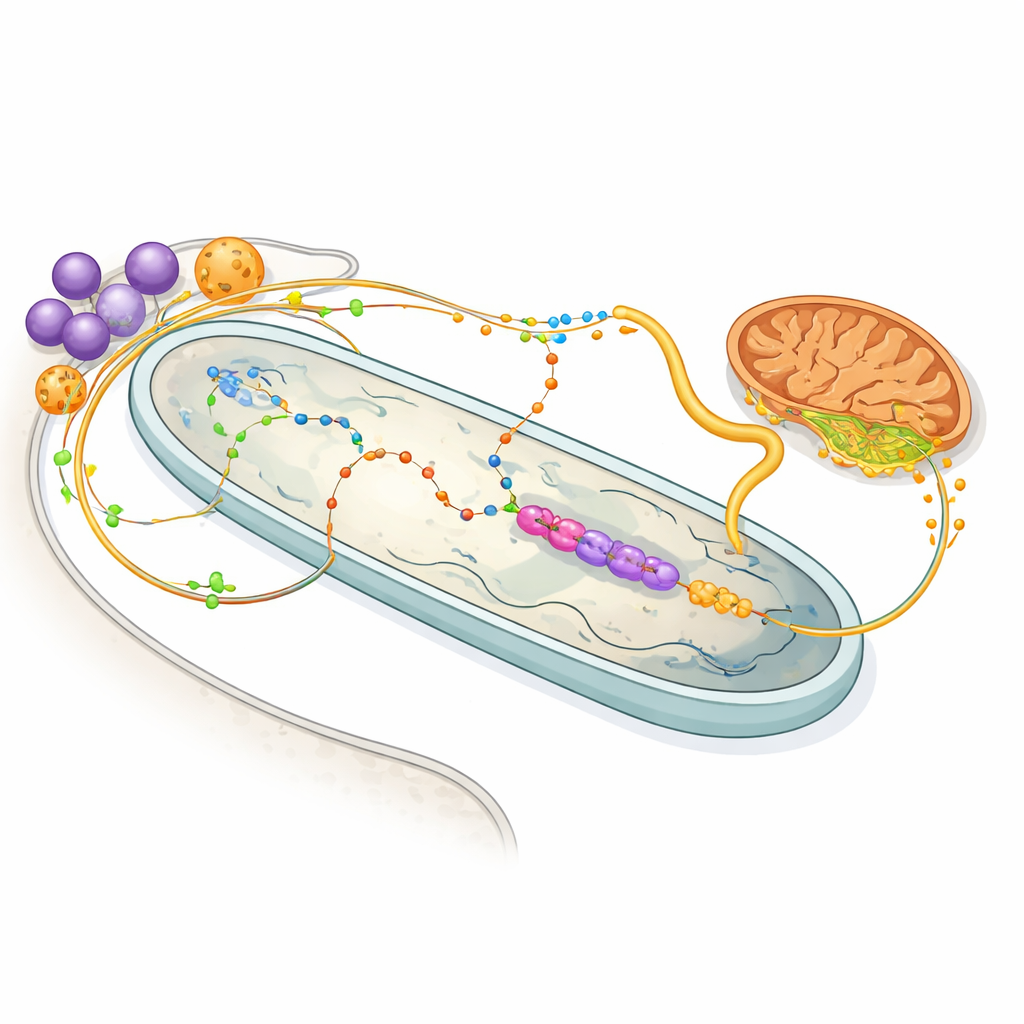
De eiwittengids belicht ook de levendige handel in moleculen tussen gastheer en bacterie. Enzymen in de glycosomen van de gastheer — organellen die suiker- en aminozuurmetabolisme afhandelen — lijken afgestemd om de bacterie te voeden met het aminozuur proline en de verbinding 2-oxoglutaraat, beide waardevolle energiebronnen. In de bacterie gebruikt een uitgeklede set enzymen 2-oxoglutaraat om NADH te genereren, wat een minimale respiratoire keten aandrijft, waarna succinaat teruggegeven wordt aan het mitochondrion van de gastheer. Andere routes laten zien dat de bacterie het grootste deel van de stappen in de synthese van heem uitvoert, een essentieel pigment dat de gastheer nodig heeft, terwijl hij ook cruciale bouwstenen voor nucleotiden levert. In wezen heeft elke partner bepaalde metabolische taken aan de ander uitbesteed, waardoor een gedeeld, onderling afhankelijk systeem is ontstaan.
Nieuwe communicatielijnen binnenin de cel
Naast metabolisme onthult de studie fysieke en waarschijnlijk signaalgevende verbindingen tussen de endosymbiont en andere organellen. Een duidelijke groep gastheer-eiwitten vormt wat de auteurs een "contactsite"-cluster noemen, verrijkt in componenten van de kernomhulling en het endoplasmatisch reticulum die fysiek co-sederen met de bacterie. Twee typen opslagorganellen — glycosomen en acidocalcisomen — verschijnen in twee populaties: sommige blijven vrij in het cytoplasma, terwijl andere consequent met de bacterie meereizen. Microscopie bevestigt dat subsets van deze organellen zich strak tegen de endosymbiont nestelen. Acidocalcisomen zijn bekende calcium- en fosfaatreservoirs, dus hun nauwe aanligging suggereert een tweerichtings signaal- en ionenverkeersroute die de bacterie, deze opslagplaatsen en het nabijgelegen endoplasmatisch reticulum verbindt.
Een blauwdruk voor leven gegroepeerd binnen leven
Gezamenlijk levert dit werk een rijke, celbrede blauwdruk van hoe een bacterie functioneel kan vervloeien met zijn gastheer zonder al te veranderen in een volwaardig orgaantje zoals mitochondriën. Angomonas deanei is afhankelijk van zijn endosymbiont voor sleutelvoedingsstoffen, terwijl de bacterie op zijn beurt afhankelijk is van gastheer-eiwitten en energierijke moleculen en is vastgekoppeld aan gastheerorganellen voor communicatie en controle. Voor niet-specialisten is de boodschap dat evolutie geleidelijk samenwerking tussen zeer verschillende levensvormen kan verankeren, stap voor stap, totdat hun scheiding onmogelijk wordt. Dit systeem biedt een levensechte momentopname van dat proces in actie en helpt wetenschappers beter te begrijpen hoe complexe cellen zoals die van ons ooit uit eenvoudiger beginstadia zijn ontstaan.
Bronvermelding: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
Trefwoorden: endosymbiose, celmetabolisme, organel-evolutie, protistbiologie, gastheer-microbe interacties