Clear Sky Science · nl
Single-molecule dynamics onthullen dat alleen ATP-binding het substraattranslocatie aandrijft bij een ABC-transporter
Waarom kleine cellulaire pompen ertoe doen
Elke cel in uw lichaam is afhankelijk van microscopische machines die moleculen over membranen verplaatsen en daarmee alles bepalen van nutriëntopname tot immuunverdediging. Een belangrijke klasse van deze machines, ABC-transporters genaamd, gebruikt de chemische brandstof ATP van de cel om lading tegen een concentratiegradiënt in te duwen. Toch werd er decennialang gedebatteerd over een fundamentele vraag: levert de eenvoudige handeling van ATP-binding de energie voor de transportstap, of komt de energie pas vrij wanneer ATP wordt afgebroken? Deze studie zoomt in op één transporter, molecuul voor molecuul, om die discussie te beslechten.
Eén transporter tegelijk observeren
In plaats van het gecombineerde gedrag van miljoenen moleculen te meten, bouwden de onderzoekers een opstelling waarmee ze individuele transportevenementen in realtime konden volgen. Ze concentreerden zich op TmrAB, een bacterieel familielid van de menselijke TAP-transporter die immuunpeptiden laadt voor presentatie aan cytotoxische T-cellen. TmrAB zit in een membraan en vervoert korte eiwitfragmenten (peptiden) van de ene kant naar de andere met behulp van ATP. Om elke transportstap te zien, vingen de onderzoekers een enkel TmrAB-molecuul in een kunstmatige membraanbel (een liposoom) en plaatsten binnen die bel een speciaal ontworpen “sensor”-eiwit dat van fluorescentie verandert wanneer het een peptide vangt. Met een zeer gevoelige microscoop konden ze vervolgens, zichtbaar als korte sprongen in het lichtsignaal, de exacte momenten waarnemen waarop het ene peptide na het andere in de bel arriveerde.
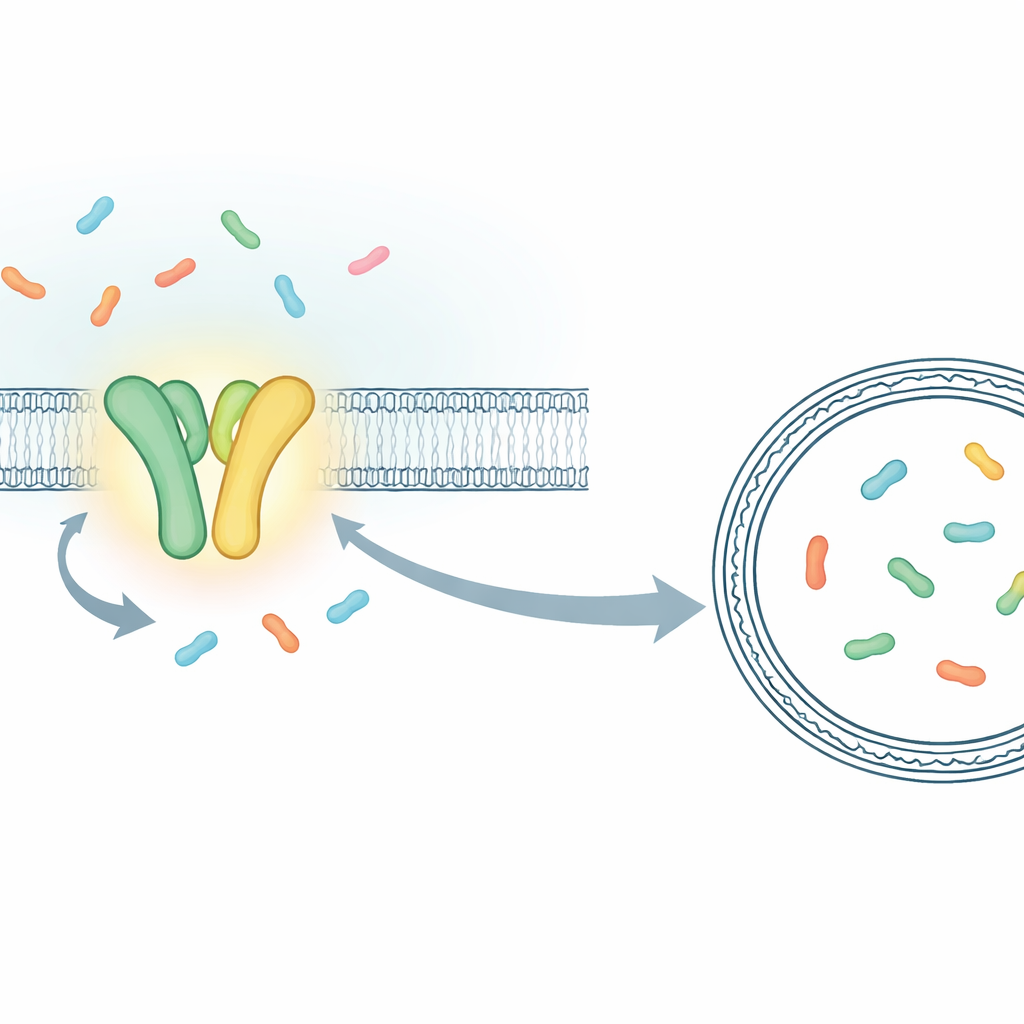
Aantonen dat één ATP-binding één peptide verplaatst
Met deze single-molecule assay konden de onderzoekers normaal TmrAB vergelijken met een gewijzigde, langzamer werkende variant waarvan de cycli in de tijd uitgerekt waren. De langzame variant maakte het mogelijk individuele gebeurtenissen te onderscheiden die anders in elkaar zouden overvloeien. Ze toonden aan dat wanneer ATP en peptiden samen aanwezig waren, de sensor binnenin het liposoom in discrete stappen verschuift van een “lege” naar een “geladen” staat, telkens consistent met het transport van één enkel peptide. Door te analyseren hoe snel de sensor om peptiden sloot en door het kleine volume binnen elk liposoom te schatten, konden ze deze lichtveranderingen zelfs omzetten in geschatte peptideconcentraties. De getallen kwamen overeen met wat je zou verwachten als één, daarna twee peptiden zich ophopen in bellen van ongeveer 100 nanometer in diameter, wat bevestigt dat ze transportevenementen één voor één telden.
Alleen ATP-binding zet de moleculaire schakel om
De kern van de controverse betreft magnesiumionen (Mg2+), die gewoonlijk ATP in cellen vergezellen en bekend staan als noodzakelijk voor efficiënte ATP-hydrolyse. Sommige modellen stelden dat Mg2+ ook nodig zou kunnen zijn voor ATP-binding of voor het sluiten van de transporter. Om deze rollen te scheiden, verwijderden de onderzoekers Mg2+ met een chelerend middel maar leverden nog steeds ATP. Onder deze omstandigheden konden zowel de normale als de langzame transporter precies één peptidetransportstap per molecuul uitvoeren, en stopten ze daarna. Dat gedrag wijst erop dat ATP nog steeds kan binden en de transporter kan dwingen te schakelen van een naar binnen gerichte naar een naar buiten gerichte conformatie en een peptide te verplaatsen, zelfs zonder Mg2+. Zonder Mg2+ kan de transporter echter ATP niet efficiënt splitsen en kan hij zichzelf dus niet resetten voor een volgende ronde.
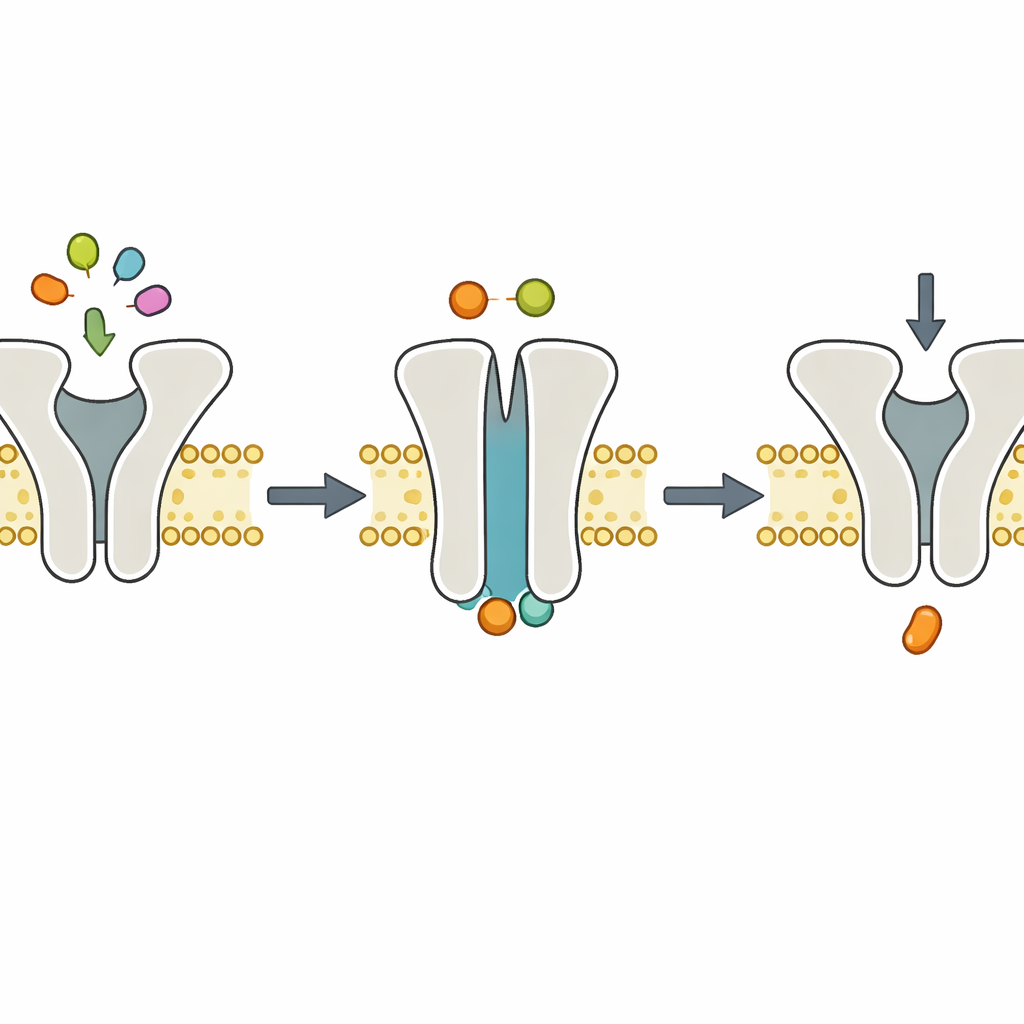
Structurele momentopnames ondersteunen de dynamica
Om te zien hoe het molecuul eruitziet tijdens deze Mg2+-vrije stap, gebruikte het team cryo-elektronenmicroscopy, die ingevroren moleculen met bijna atomair detail afbeeldt. Ze reconstitueerden TmrAB in lipide nanodiscs, voegden ATP toe zonder Mg2+ en vroren de complexen in. De resulterende structuren toonden TmrAB in een naar buiten gerichte, “geokcludeerde” conformatie met ATP geklemd in beide interne bindingspockets, maar zonder zichtbare Mg2+. Deze momentopnames waren in wezen niet te onderscheiden van eerdere structuren verkregen met ATP en Mg2+ aanwezig. Samen met biochemische assays die laten zien dat ATP-hydrolyse volledig vastloopt zonder Mg2+, ondersteunen de beelden een eenvoudige taakverdeling: ATP-binding drijft de conformationele wissel aan die het peptide verplaatst, terwijl Mg2+-afhankelijke ATP-hydrolyse zorgt voor de herstelstap.
Een helderder beeld van hoe cellulaire pompen werken
Door enkele transporters te volgen en hun structuren op te lossen, lost dit werk een langlopende vraag over ABC-transporters op: de mechanische krachtstoot die een peptide verplaatst, wordt geïnitieerd door ATP-binding zelf en niet door de latere chemische afbraak van ATP. Mg2+ speelt vooral een rol bij het mogelijk maken van ATP-splitsing, wat de transporter reset zodat hij opnieuw kan werken. Naast het verhelderen van een fundamenteel stuk celbiologie, biedt deze single-molecule-benadering een blauwdruk om andere membraanmachines te ontleden die ten grondslag liggen aan immuniteit, medicijnresistentie en vele ziekten — één molecuul en één transportstap tegelijk.
Bronvermelding: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Trefwoorden: ABC-transporters, ATP-binding, single-molecule FRET, membraantransport, TAP en TmrAB