Clear Sky Science · nl
Pruisisch-blauwe nanodeeltjes die meerdere PANoptosoom-gemedieerde PANoptose richten voor therapie van myocardiale ischemie-reperfusieletsel
Waarom het beschermen van het herstellende hart belangrijk is
Wanneer iemand een hartaanval krijgt, haasten artsen zich om de geblokkeerde slagader te openen en de bloedtoevoer te herstellen. Deze levensreddende stap brengt echter een verborgen prijs met zich mee: de plotselinge terugkeer van zuurstof kan het hart zelf beschadigen, cellen doden en de aanzet geven tot hartfalen. Deze studie onderzoekt een inventief nanomedicijn dat het hart tijdens dit kwetsbare venster wil beschermen door gelijktijdig meerdere verweven celdoodroutes te blokkeren, wat mogelijk leidt tot zachtere hersteltrajecten na een hartaanval.
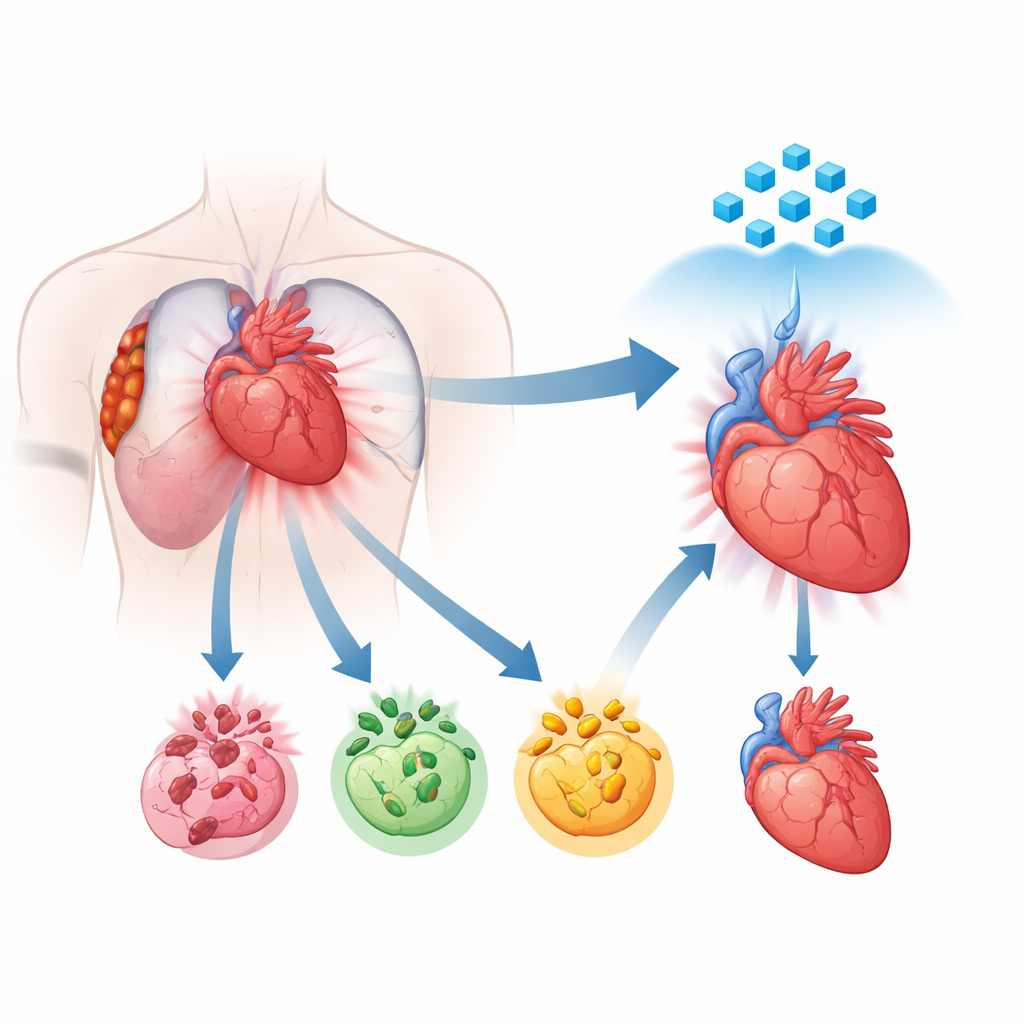
Een nieuw perspectief op hoe hartcellen sterven
Jarenlang wisten wetenschappers dat beschadigde hartcellen via verschillende geprogrammeerde routes kunnen sterven, waaronder apoptose, necroptose en pyroptose. Elk volgt zijn eigen moleculaire script, maar toenemend bewijs laat zien dat deze routes niet geïsoleerd werken. Ze communiceren juist met elkaar en kunnen samensmelten tot een gecombineerd, uit de hand lopend proces dat PANoptose wordt genoemd. In deze toestand vuren meerdere doodsprogramma’s tegelijk, waardoor therapieën die slechts één pad blokkeren teleurstellend zwak zijn. De auteurs gebruikten single-nucleus RNA-sequencing van menselijk hartweefsel van patiënten met recente hartinfarcten om in kaart te brengen waar en hoe sterk deze doodsprogramma’s zijn ingeschakeld. Ze vonden dat in de meest beschadigde gebieden hartspiercellen een krachtige verschuiving naar deze gecombineerde doodsmodus vertoonden, waarmee PANoptose een centrale aandrijver van schade blijkt te zijn.
Het ontwerpen van een klein veeldoelgereedschap voor het beschadigde hart
Om zo’n complex proces aan te pakken, wendde het team zich tot Pruisisch blauw, een al lang goedgekeund medisch middel dat vooral bekendstaat als tegengif bij bepaalde metaalvergiftigingen. Op nanoschaal gedragen Pruisisch-blauwe deeltjes zich als kleine katalytische robots die schadelijke moleculen kunnen neutraliseren en celgedrag kunnen beïnvloeden. Met behulp van computersimulaties toonden de onderzoekers aan dat deze nanodeeltjes direct aan drie sleutelproteïnehubs — RIPK1, ZBP1 en AIM2 — konden binden die helpen bij het assembleren van het moleculaire apparaat van PANoptose. Door op verschillende manieren aan deze hubs te binden, werd voorspeld dat de deeltjes de bouw van de doodveroorzakende complexen die de drie celdoodroutes coördineren zouden verstoren.
Nanodeeltjes rechtstreeks naar beschadigd hartweefsel sturen
Nanodeeltjes werken alleen als ze de juiste plaats bereiken, dus omhulde het team Pruisisch-blauwe deeltjes met natuurlijke membranen die van bloedplaatjes waren gestript — de bloedcellen die zich naar beschadigde vaten richten. Deze coating creëerde PB@PM, een biomimetische drager die circuleert als een bloedplaatje maar een therapeutische lading aflevert. Bij muizen die aan een gecontroleerde hartaanval en heropening van de slagader werden onderworpen, toonde beeldvorming dat PB@PM veel sterker in het beschadigde hartgebied ophoopte dan ongecoate deeltjes, terwijl gezonde organen grotendeels werden vermeden. Belangrijk is dat de gecoate deeltjes goed werden verdragen: bloedonderzoeken en weefselexamens toonden geen duidelijke toxiciteit, wat hun potentieel voor verdere ontwikkeling ondersteunt.
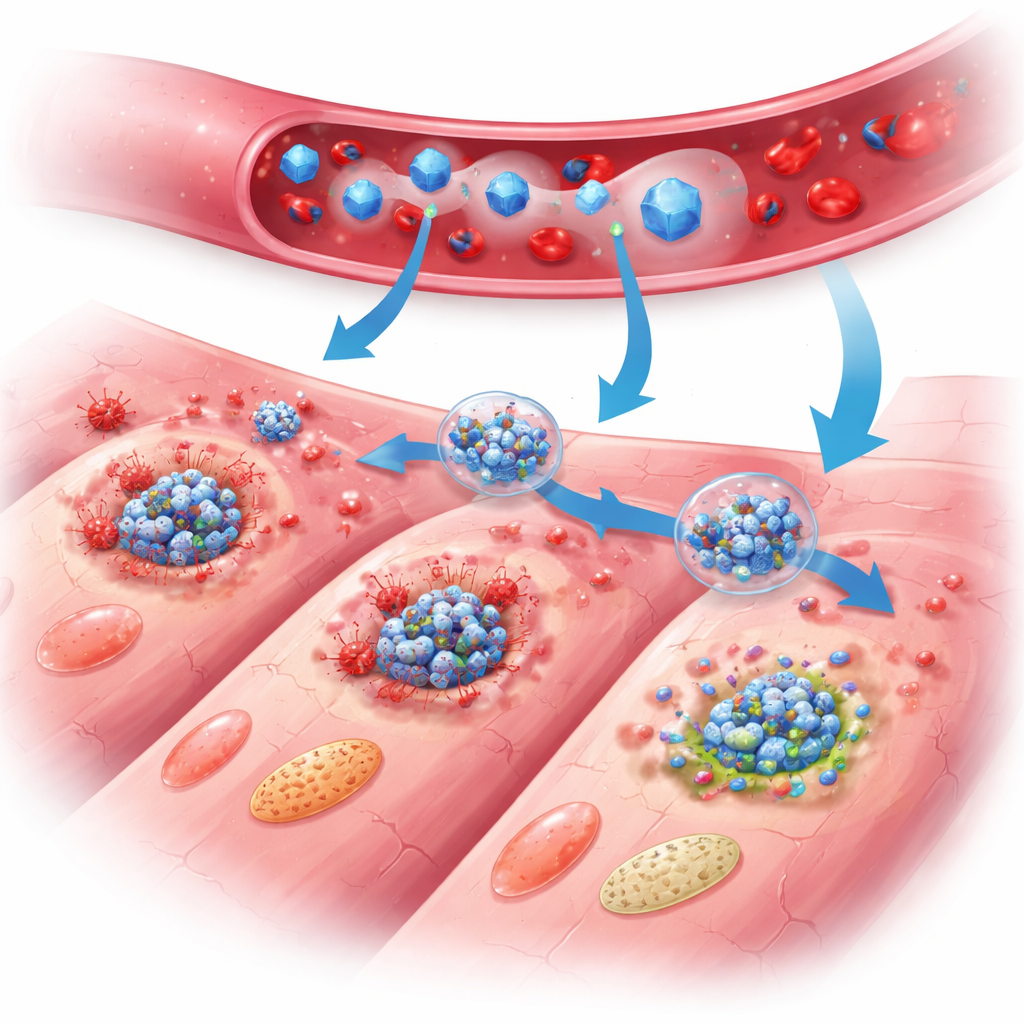
Hoe het nano-schild het hart beschermt
Bij behandelde muizen werden de voordelen van PB@PM duidelijk over dagen en weken. De pompfunctie van het hart verbeterde, de littekenomvang nam af en de hartwand werd minder dun in vergelijking met onbehandelde dieren. Gedetailleerde weefselstudies toonden minder stervende hartcellen, rustigere ontstekingscellen en beter gestructureerd reparatieweefsel met gezondere bloedvaatjesgroei en minder abnormale vergroting van overlevende cellen. Op moleculair niveau lieten brede genexpressieprofielen en eiwitmetingen zien dat PB@PM de drie belangrijkste geprogrammeerde-doodroutes tegelijkertijd dempte, de assemblage van de multi-eiwit PANoptose-complexen verstoorde en de niveaus van signaalmoleculen die ontsteking aanwakkeren verlaagde. De deeltjes ruimden ook schadelijke reactieve zuurstofsoorten op, stabiliseerden mitochondriën — de energiecentrales van de cel — en herstelden een normaler energiemetabolisme, waarmee ze sleuteltriggers verwijderden die anders cellen naar zelfvernietiging zouden duwen.
Wat dit kan betekenen voor toekomstige zorg bij hartaanvallen
Simpel gezegd toont dit werk aan dat een slim ontworpen nanodeeltje kan fungeren als een veelzijdig schild voor het hart, het dempen van een wirwar van destructieve doodssignalen in plaats van één pad tegelijk na te jagen. Door zich te richten op beschadigd hartweefsel, kernregulatoren te binden en oxidatieve en inflammatoire stress te verminderen, verminderde PB@PM scherp de kettingreactie van celverlies en littekenvorming die vaak volgt op het heropenen van een geblokkeerde slagader. Hoewel er nog veel testen nodig zijn voordat deze strategie patiënten kan bereiken, levert de studie een proof of concept dat het richten op PANoptose als geheel — en dat met slimme, biologisch geïnspireerde deeltjes — een nieuw hoofdstuk kan openen in het beschermen van het hart na een hartaanval.
Bronvermelding: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Trefwoorden: myocardiale ischemie reperfusie, nanodeeltje-therapie, geprogrammeerde celdood, cardiale ontsteking, mitochondriale bescherming