Clear Sky Science · nl
RPA stimuleert direct de processiviteit van helicase Mer3 om normale crossover‑vorming tijdens meiose te waarborgen
Hoe cellen DNA herschudden om gezonde eicellen en zaadcellen te maken
Elke keer dat een plant, dier of mens eicellen of zaadcellen vormt, moeten de cellen chromosomen herschikken zodat elk nageslacht een nieuwe mix van ouderlijk DNA krijgt. Deze genetische herschikking berust op zorgvuldig geplaatste DNA‑uitwisselingen, of crossovers, tussen chromosoomparen. De gepresenteerde studie onthult hoe twee sleutelproteïnen, Mer3 en RPA, samenwerken als een microscopische machine om te garanderen dat deze crossovers efficiënt en veilig tot stand komen — een proces met implicaties voor vruchtbaarheid, evolutie en mogelijk ook kanker.
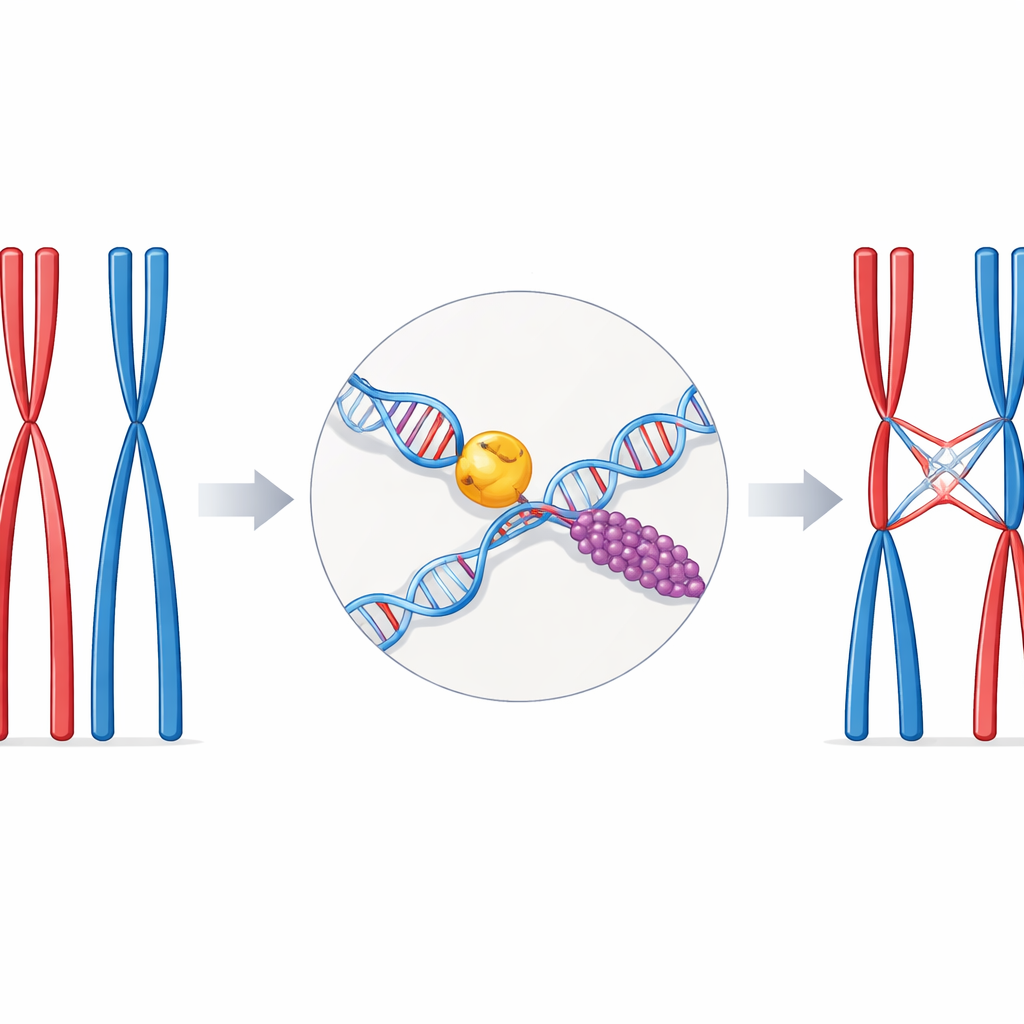
Een delicate afweging bij seksuele voortplanting
Tijdens de speciale celdeling die meiose heet, treden chromosomen op in bijpassende paren, één van elke ouder. Om deze paren correct te laten scheiden, moeten ze op een paar goedgekozen plekken langs hun lengte fysiek met elkaar verbonden zijn. Die verbindingen zijn de crossovers — gedeelten waar DNA‑strengen van het ene chromosoom worden geruild met die van de partner. Te weinig crossovers vergroten het risico op foutieve segregatie van chromosomen en infertiliteit; te veel of slecht geplaatste crossovers kunnen het genoom beschadigen. Cellen vertrouwen daarom op gespecialiseerde herstelroutes en hulpproteïnen om een gevaarlijke DNA‑breuk om te zetten in een goed gereguleerde crossover.
Maak kennis met Mer3 en RPA, een DNA‑ontwikkende tandem
De onderzoekers richtten zich op Mer3, een moleculaire motor die DNA ontwindt en crossover‑vorming bevordert. Het menselijke equivalent, HFM1, is bekend als belangrijk voor de vruchtbaarheid. Ze ontdekten dat Mer3 direct bindt aan RPA, een proteïnecomplex dat normaal gesproken blootliggend enkelstrengs DNA bekleedt om het te beschermen en andere herstelactoren aan te trekken. Met biochemische tests, structurele modellering en interactieassays kaartte het team een specifiek dockingspunt uit waar een korte staart van Mer3 in een groef op een RPA‑subeenheid past. Dit interactievlak is geconserveerd van gist tot zoogdieren, wat suggereert dat het een langdurige evolutionaire oplossing is om DNA‑herstel tijdens de meiose te reguleren.
Een enkele DNA‑motor in actie bekijken
Om te zien wat deze samenwerking daadwerkelijk doet, gebruikten de wetenschappers single‑molecule magnetic tweezers — een instrument dat een enkel DNA‑haartje als een piepkleine veer vasthoudt en meet hoe één Mer3‑molecuul het in de loop van de tijd ontwindt. Ze vonden dat Mer3 met een constante snelheid langs DNA beweegt, ook zelfstandig. Maar onder omstandigheden die de relatief lage fysieke spanning binnen cellen nabootsen, laat Mer3 vaak los van het DNA nadat het slechts een korte stretch heeft ontwonden. Wanneer een kleine hoeveelheid RPA aanwezig is, wordt Mer3 plots veel volhardender: het kan veel langere DNA‑stretches ontwinden zonder los te laten, vooral wanneer het DNA de neiging heeft in zichzelf terug te vouwen. Een gemuteerde versie van Mer3, ontworpen om de RPA‑bindende staart te verstoren, krijgt deze extra vasthoudendheid niet, wat aantoont dat direct contact met RPA Mer3’s processiviteit verhoogt.
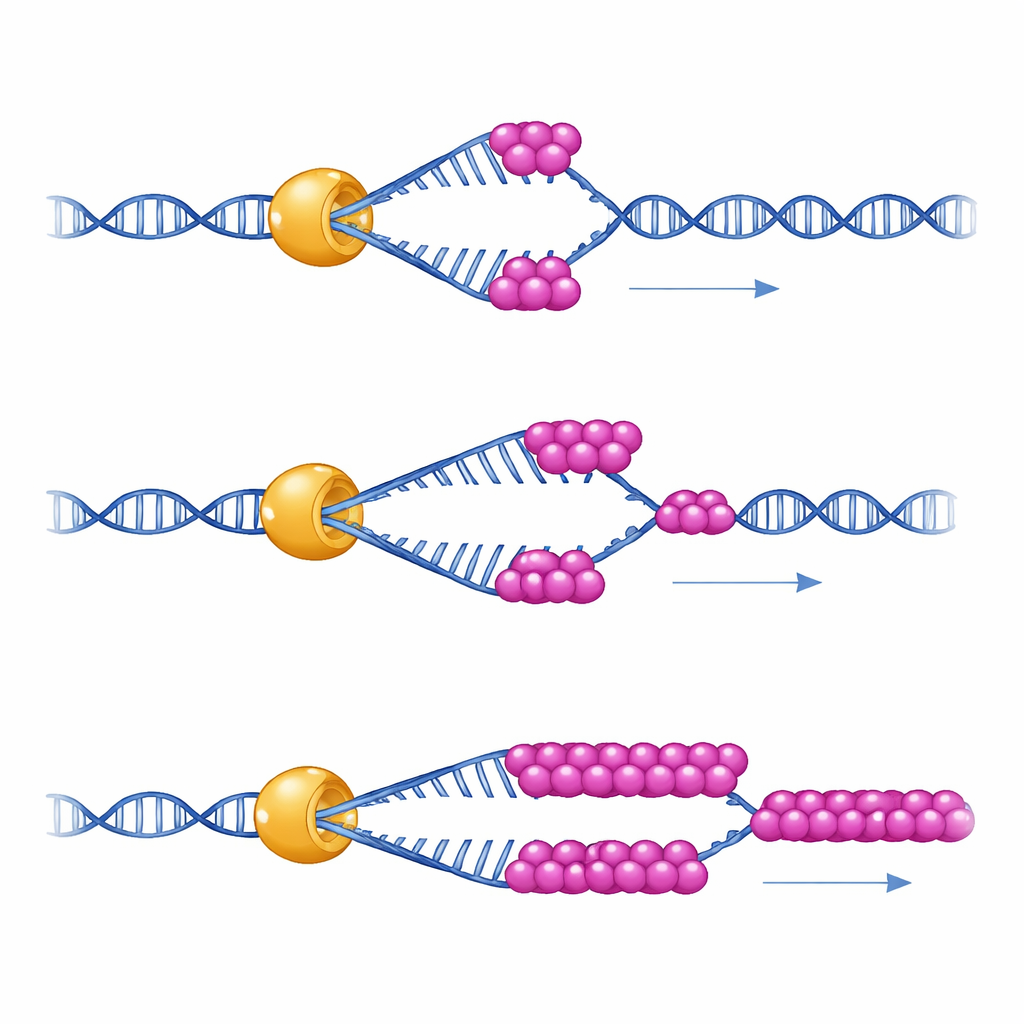
Gevolgen voor crossovers in levende cellen
Het team vroeg vervolgens wat er in echte gistcellen gebeurt wanneer Mer3 RPA niet goed kan vasthouden. Ze vervingen het normale MER3‑gen door de RPA‑bindende mutant en volgden de meiose. Deze cellen konden nog wel delen en sporen vormen, maar hun vruchtbaarheid daalde en het totale aantal crossovers langs bepaalde chromosoomregio’s nam af. Gedetailleerde DNA‑analyse toonde meer herstelgebeurtenissen die eindigden als non‑crossovers en een opeenhoping van niet‑opgeloste recombinatie‑intermediaten. Genoomwijde kaartlegging van Mer3’s locatie liet zien dat het gemuteerde eiwit minder stabiel werd aangetrokken naar plaatsen waar geprogrammeerde DNA‑breuken optreden, ondanks dat de vroege associatie met chromosoomassen normaal leek. Met andere woorden: zonder sterke RPA‑binding blijft Mer3 niet lang genoeg op breukplaatsen om deze betrouwbaar naar crossover‑uitkomsten te leiden.
Wat dit betekent voor vruchtbaarheid en genoomstabiliteit
Samengevat laat de studie zien dat RPA meer doet dan alleen los DNA bekleden; het stelt direct het gedrag van een belangrijke meiotische helicase bij. Door aan RPA te docken, wordt Mer3 een vastberadener DNA‑ontwinder, in staat de gezamenlijke DNA‑structuren uit te breiden en te stabiliseren die uitrijpen tot crossovers. Wanneer deze interactie verzwakt is, schakelen cellen over naar veiligere maar minder bruikbare hersteluitkomsten en blijven meer intermediaten onopgelost, waardoor de chromosoomsegregatie subtiel wordt ondermijnd. Aangezien dezelfde moleculaire spelers ook bij mensen aanwezig zijn — en mutaties in HFM1 aan infertiliteit worden gekoppeld — levert dit werk een mechanistisch kader voor hoe kleine veranderingen op een proteïneinterface zich kunnen uitvergroten tot effecten op voortplantingsgezondheid en de genetische diversiteit van toekomstige generaties.
Bronvermelding: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Trefwoorden: meiose, genetische recombinatie, DNA‑helicase, vruchtbaarheid, chromosoomcrossover