Clear Sky Science · nl
Ontregeling van de DNA-schaderespons door fosforothioaat antisense-oligonucleotiden
Wanneer nuttige gentherapieën het herstelteam van de cel misleiden
Antisense-oligonucleotiden, of ASO’s, zijn een opkomende klasse precisiegeneesmiddelen die ontworpen zijn om individuele genen aan of uit te zetten. Ze worden al gebruikt voor de behandeling van enkele zeldzame genetische aandoeningen en worden voor veel meer ziekten onderzocht. Deze studie onthult een onverwachte keerzijde van een veelgebruikte chemische aanpassing die deze middelen stabieler maakt: onder de juiste omstandigheden kan die aanpassing de cel doen geloven dat het DNA beschadigd is, waardoor het herstelmechanisme vastloopt en het genoom op de lange termijn risico loopt.
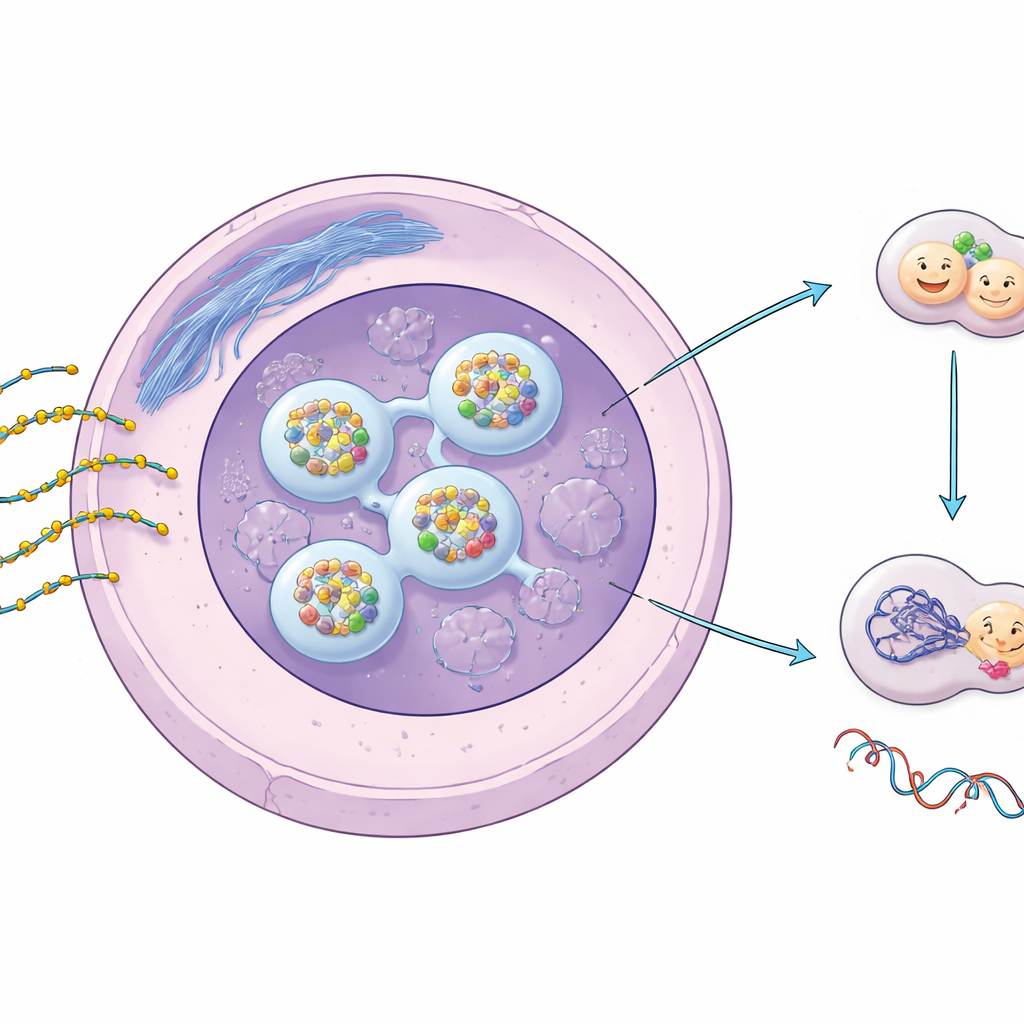
Ontwerpers van genschakelaars en hun chemische upgrade
ASO’s zijn korte, enkelstrengige fragmenten genetisch materiaal die ontworpen zijn om specifieke RNA-boodschappen in onze cellen te herkennen en te binden, waardoor deze worden uitgeschakeld of gewijzigd. Om in het lichaam te overleven en efficiënt cellen binnen te dringen, dragen de meeste therapeutische ASO’s een fosforothioaat (PS)-modificatie, waarbij een zwavelatoom een zuurstofatoom in de ruggegraat van de streng vervangt. Deze kleine wijziging vergroot hun stabiliteit en hun neiging om met eiwitten te interageren aanzienlijk. Eerder werk toonde aan dat PS-ASO’s zich ophopen in onderscheiden plekken in de celkern en bepaalde nucleaire structuren kunnen belasten, maar wat dit betekent voor DNA-herstel en veiligheid op lange termijn bleef onduidelijk.
Kunstmatige druppels die echte DNA-herstelplaatsen nabootsen
De auteurs volgden fluorescent gelabelde PS-ASO’s in menselijke cellen en vonden dat ze bij veelgebruikte experimentele concentraties snel opstapelen in de kern en nieuwe bolvormige structuren vormen die PS-lichamen worden genoemd. Deze lichamen ontstaan afhankelijk van de concentratie en gedragen zich als vloeibare druppels die samenvoegen, oplossen en afhankelijk zijn van zwakke moleculaire krachten — kenmerkend voor vloeistof–vloeistof fase-separatie. Cruciaal is dat ze niet op de plaatsen zitten waar daadwerkelijke DNA-breuken optreden en niet de gebruikelijke markers van gebroken DNA bevatten. In plaats daarvan laat de studie zien dat belangrijke DNA-herstelenzymen — waaronder DNA‑PKcs, ATM, ATR en PARP1 — direct binden aan de PS-ASO’s en sterk verrijkt raken binnen deze kunstmatige druppels, ondanks dat het onderliggende DNA intact is.
Vals alarm dat de schadesignalen van de cel activeert
Eens gevormd doen de door ASO’s geïnitieerde druppels meer dan eiwitten passief vasthouden: ze schakelen de herstelenzymen in. Binnen een uur na opname van ASO’s worden de enzymen in deze druppels geactiveerd en beginnen ze de nabijgelegen chromatine te modificeren, waarbij histoneiwitten chemische merkers krijgen die normaal gesproken na echte DNA-schade verschijnen. Dit zet de volledige DNA-schaderespons in gang — het rekruteren van extra herstelcomponenten, het inschakelen van checkpointsignalen en het terugschakelen van de activiteit van celcyclusmotoren genaamd CDK’s. Hierdoor vertragen of stoppen cellen hun voortgang door belangrijke fasen van de celcyclus, met name op het punt waarop ze normaal controleren of het DNA intact is voordat ze delen. In muizenhersenen die werden blootgesteld aan klinisch relevante ASO-toediening, observeerden de onderzoekers ook verhoogde DNA-schadesignalisatie in regio’s met hogere ASO-opname, wat aangeeft dat deze effecten niet beperkt zijn tot celkweken.
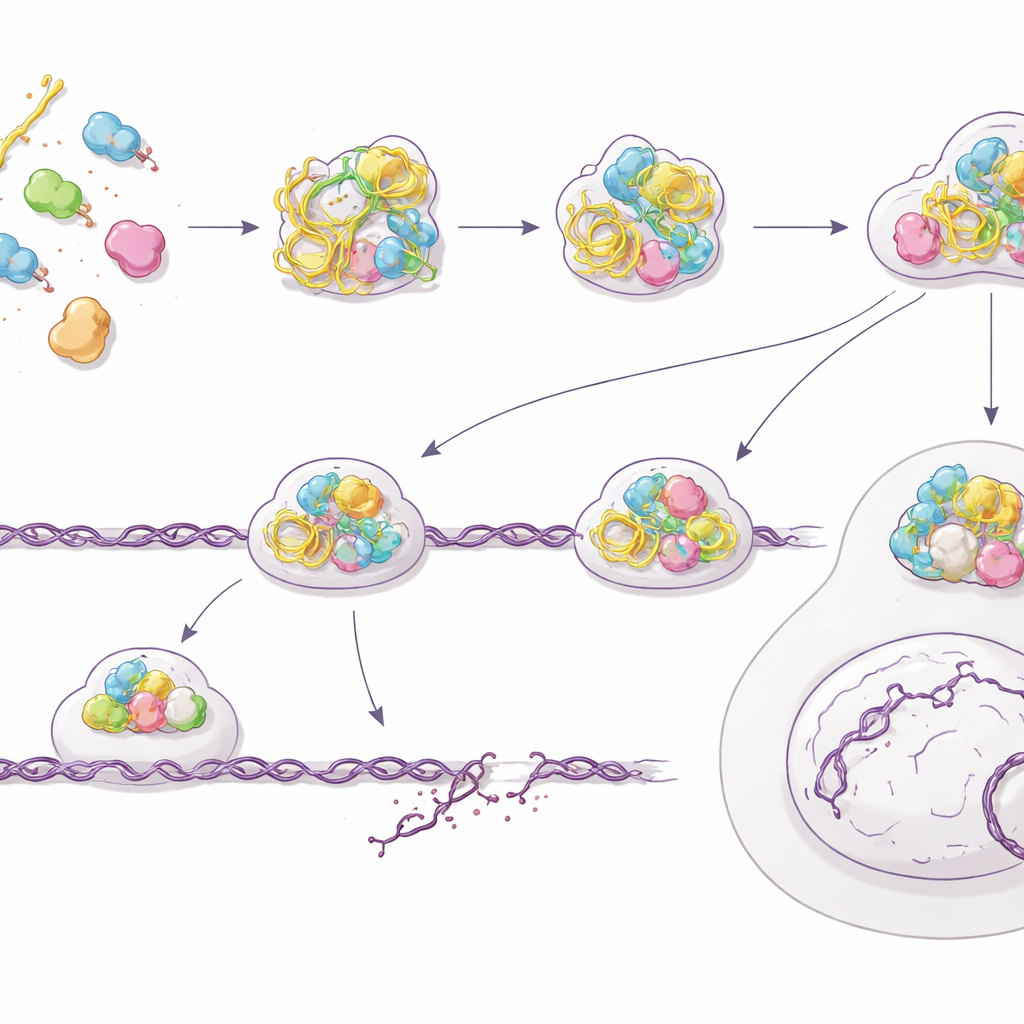
Herstel dat verkeerd gaat en een toenemende last van DNA-breuken
Paradoxaal genoeg verslechtert terwijl het alarm van de cel afgaat de daadwerkelijke capaciteit om gevaarlijke DNA-breuken te herstellen. Het team toonde aan dat cellen die vooraf behandeld waren met PS-ASO’s moeite hebben om schade na bestraling op te ruimen en zelfs meer spontane breuken accumuleren, gemeten met comet-assays en aanhoudende herstelplekken. Een nadere blik op een van de meest nauwkeurige herstelroutes van de cel — homologe recombinatie — onthulde het probleem: sleutelspelers zoals BRCA2 en RAD51 slagen er niet in zich correct te assembleren bij gebroken DNA-einden, terwijl eerdere markers van verwerking aan die uiteinden wel verschijnen. Met behulp van een genetisch reportingsysteem kwantificeerden de auteurs een daling van ongeveer 60% in de efficiëntie van homologe recombinatie na blootstelling aan PS-ASO’s. Cellen verliezen over het algemeen levensvatbaarheid en worden opvallend gevoeliger voor straling, wat overeenkomt met een repairsysteem dat wel wordt gesignaleerd maar niet correct wordt ingezet.
Wat dit betekent voor de toekomst van gentargeting-medicijnen
Samengevat suggereert de studie dat PS-gemodificeerde ASO’s kunstmatige vloeibare druppels in de kern kunnen nucleëren die DNA-herstelenzymen concentreren en activeren, zelfs wanneer er geen schade is om te herstellen. Dit chronische valse alarm verstoort normale herstelkeuzes, in het bijzonder de accurate homologe recombinatie, wat leidt tot persistente DNA-laesies, checkpoint-activatie en celdood. Hoewel de sterkste effecten worden gezien bij hoge nucleaire ASO-niveaus typisch voor transfectie-experimenten, is subtiele activatie van damagesignalen detecteerbaar zelfs bij lagere, medicijnachtige doses. Voor patiënten en geneesmiddelenontwikkelaars is de boodschap duidelijk: de chemische eigenschappen die ASO’s effectieve geneesmiddelen maken, kunnen in sommige contexten interfereren met de meest fundamentele waarborg van de cel — het vermogen om een stabiel genoom te behouden — wat de noodzaak benadrukt om veiligere ruggraden te ontwerpen en DNA-herstelroutes tijdens therapie te monitoren.
Bronvermelding: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Trefwoorden: antisense-oligonucleotiden, DNA-schaderespons, vloeibare-fase-separatie, homologe recombinatie, genoomstabiliteit