Clear Sky Science · nl
Chirale peptidoglycaan‑mimics richten zich op de biosynthese van de bacteriewand voor interventie tegen ziekteverwekkers
Een nieuwe manier om schadelijke kiemen op te sporen
Infecties die resistent zijn tegen antibiotica nemen wereldwijd toe, maar artsen hebben nog steeds geen middelen die gevaarlijke bacteriën precies kunnen opsporen en aanvallen zonder onze eigen cellen te beschadigen. Deze studie introduceert een slim moleculair "lokmiddel" dat een belangrijk bouwsteen van bacteriële celwanden nabootst. Deze ontworpen moleculen kunnen zowel infecties zichtbaar maken voor beeldvorming als antibiotica rechtstreeks naar de microben vervoeren, en bieden zo een nieuwe strategie om moeilijk te behandelen ziekteverwekkers te bestrijden.
Het bacteriële pantser imiteren
Bacteriën zijn omgeven door een stevig netwerk dat de celwand wordt genoemd, opgebouwd uit suikers en ongewone spiegelbeeld‑aminozuren die onze eigen cellen grotendeels niet gebruiken. De onderzoekers maakten gebruik van dit verschil door lange suikerketens te creëren die zijn voorzien van een specifieke spiegelbeeldvorm van alanine, een veelvoorkomend aminozuur. Deze ketens, chiral peptidoglycaan‑mimics genoemd, zijn ontworpen om sterk te lijken op de natuurlijke ingrediënten die bacteriën gebruiken om hun wanden te bouwen, maar ontbreken in zoogdierweefsel. Door nauwkeurig af te stemmen hoeveel van dit D‑vormige alanine werd aangebracht, produceerde het team varianten die duidelijk de voorkeur gaven aan bacteriën boven menselijke cellen.
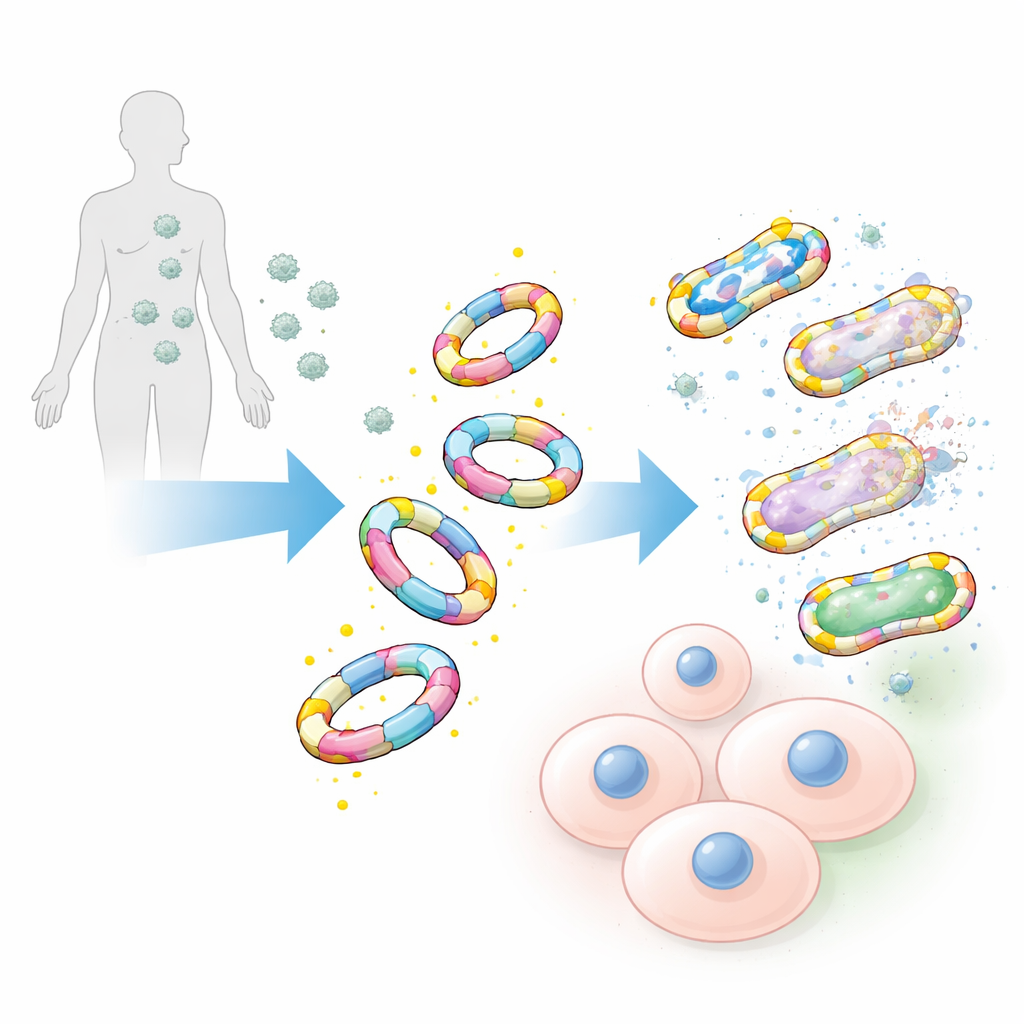
Zich vasthechten aan bacteriën, niet aan onze cellen
Bij testen tegen een breed scala aan ziekteverwekkers, waaronder beruchte ziekenhuisstammen zoals methicilline‑resistente Staphylococcus aureus en andere ESKAPE‑bacteriën, hechtten de met D‑alanine versierde mimics zich met opvallende efficiëntie aan bacteriële oppervlakken. Hun spiegelbeeldtegenhangers opgebouwd uit de L‑vorm van alanine, evenals de oorspronkelijke suikerketens alleen, toonden slechts zwakke of verwaarloosbare binding. Het team vergeleek deze grote mimics ook met traditionele kleine chemische sondes die zijn gebaseerd op enkele D‑alaninemoleculen. Zelfs wanneer de kleine sondes extreem fel werden gemaakt, markeerden ze nog steeds veel minder bacteriën en gaven ze zwakkere signalen, wat de kracht van het grotere, meer levensechte ontwerp onderstreept.
De assemblagelijn van de celwand kapen
Om te begrijpen waarom de herkenning zo sterk wordt, onderzochten de wetenschappers hoe de mimics interageren met het machinerie voor de bouw van de bacteriewand. Ze ontdekten dat de op D‑alanine gebaseerde ketens niet alleen aan de buitenkant vastplakken; ze worden opgenomen alsof het echte bouwstenen zijn en gevoed in dezelfde enzymatische stappen die normaal celwandcomponenten aan elkaar koppelen. Chemische analyse detecteerde nieuwe tussenproducten die alleen ontstaan wanneer deze mimics aanwezig zijn, en computersimulaties toonden aan dat sleutelenzymen voor wandopbouw de mimics zelfs strakker grijpen dan de natuurlijke substraten. Over meerdere rondes van bacteriële groei hoopten de mimics zich op in de wand, vervormden geleidelijk de structuur en maakten deze lekkend.
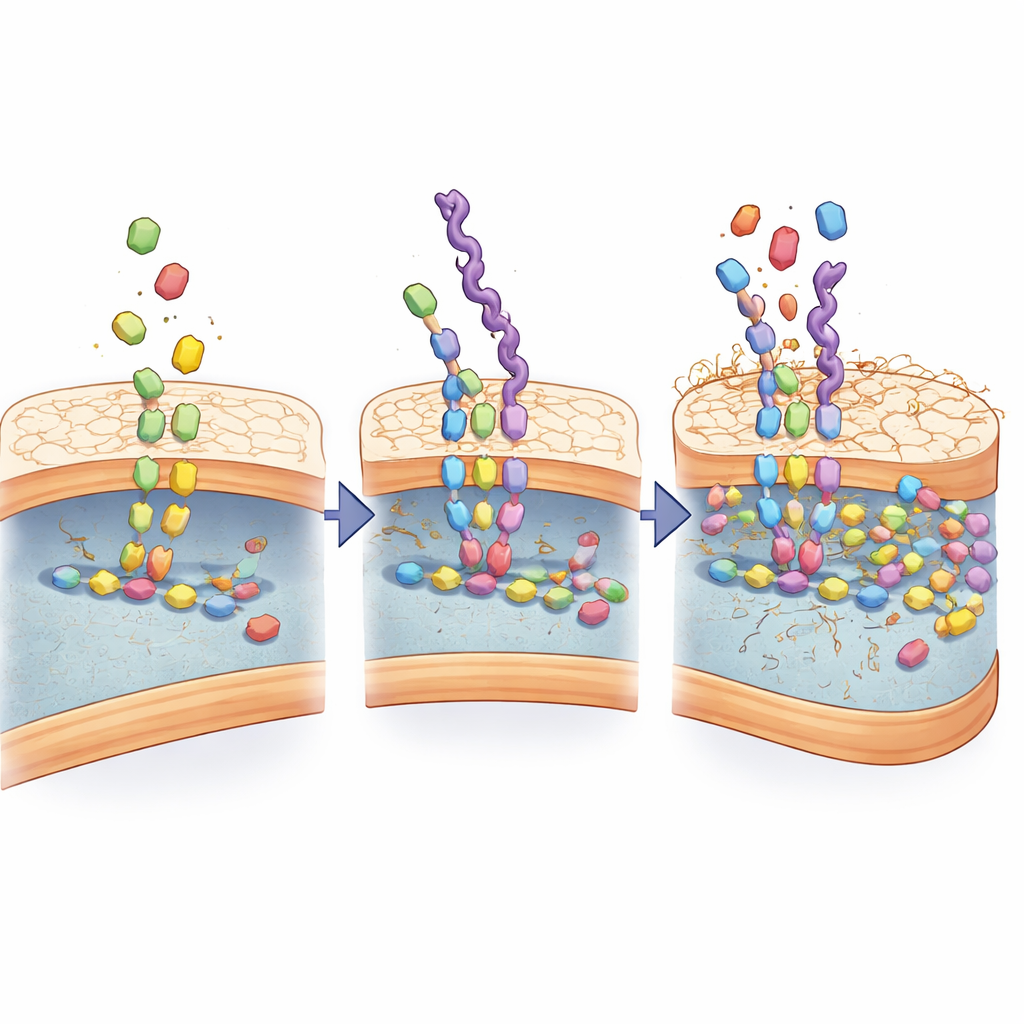
Mimics omzetten in slimme geneesmiddelcarriers
Aangezien deze ketens van nature in water samenklonteren tot kleine deeltjes en veel chemische aanhechtingspunten dragen, gebruikte het team ze als raamwerk voor beeldvormingskleurstoffen en antibiotica. Fluorescerende varianten tekenden bacteriën duidelijk af in celkweken, terwijl ze nauwelijks interageerden met naast elkaar gekweekte zoogdiercellen. De onderzoekers laadden vervolgens het antibioticum tetracycline in de op mimics gebaseerde deeltjes. In laboratoriumtests maakte deze verpakking tetracycline vele malen effectiever, waarbij zelfs resistente stammen werden gedood bij veel lagere doses dan het vrije geneesmiddel. Microscopen toonden dat met antibiotica geladen mimics zich ophoopten op bacteriën, hun omhulsels binnendrongen en uitgebreide celdood veroorzaakten vergeleken met niet‑gerichte formuleringen.
Infecties in het lichaam bestrijden
De meest veeleisende tests vonden plaats in muismodellen van gelokaliseerde huidwonden en levensbedreigende buikinfecties. In geïnfecteerde wonden homden de fluorescerende mimics zich op bacteriën diep in het weefsel en raakten, wanneer ze tetracycline droegen, bijna alle microben kwijt. Dit leidde tot snellere genezing, dikkere nieuwe huid, ordelijkere collageenvorming en rijkere groei van kleine bloedvaten. In modellen van systemische infectie hoopten de mimics zich specifiek op in geïnfecteerde organen zoals de milt en de longen, waar ze het aantal bacteriën sterk verminderden wanneer ze met antibioticum waren geladen. Belangrijk is dat hoge doses van alleen de mimics een goede veiligheid toonden, zonder duidelijke schade aan belangrijke organen of bloedchemie.
Wat dit kan betekenen voor toekomstige behandelingen
Door een nauw chemisch neefje van de eigen ingrediënten van de bacteriële celwand te bouwen, toont dit werk een nieuwe manier om "op te gaan in" de stofwisseling van een ziekteverwekker in plaats van alleen van buitenaf aan te vallen. Deze chirale mimics fungeren zowel als hoogprecieze bakens voor beeldvorming als slimme voertuigen die antibiotica rechtstreeks naar hun microbie‑doelen sturen, inclusief resistente stammen, terwijl ze zoogdiercellen ontzien. Als ze in klinische hulpmiddelen worden vertaald, zouden dergelijke biomimetische platformen artsen kunnen helpen precies te zien waar infecties zich verschuilen en ze effectiever te behandelen met lagere geneesmiddedoseringen, wat een veelbelovend wapen biedt tegen de groeiende uitdaging van antimicrobiële resistentie.
Bronvermelding: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Trefwoorden: antibioticaresistentie, bacteriële celwand, gerichte medicijnafgifte, moleculaire beeldvorming, nanotherapie