Clear Sky Science · nl
Multimodale dissectie van cel-typespecifieke TDP-43-pathologie in de motorische cortex
Waarom dit onderzoek belangrijk is voor mensen
Amyotrofische laterale sclerose (ALS) en frontotemporale dementie (FTD) zijn verwoestende hersenziekten die mensen hun beweging, spraak en persoonlijkheid ontnemen. De meeste patiënten met ALS en veel patiënten met FTD vertonen een gemeenschappelijk microscopisch kenmerk: ophopingen van een eiwit genaamd TDP-43 op plaatsen waar het niet hoort. Deze studie onderzoekt twee praktische vragen met grote implicaties voor toekomstige behandelingen: welke hersencellen worden precies het zwaarst getroffen door TDP-43-problemen, en wat gaat er mis binnen die cellen op het niveau van DNA-regulatie en genactiviteit?
De schade volgen naar het bewegingscentrum van de hersenen
De onderzoekers richtten zich op de primaire motorische cortex, de strook hersenweefsel die vrijwillige bewegingen aanstuurt. Met post-mortem gedoneerde hersenmonsters van mensen met ALS, ALS-FTD en neurologisch gezonde controles isoleerden ze individuele celkernen en bepaalden zowel welke genen actief waren als hoe open of dicht het lokale DNA was verpakt. Deze “multi-omische” aanpak, toegepast op meer dan 180.000 kernen, stelde hen in staat cellen nauwkeurig in typen in te delen: meerdere klassen van exciterende en remmende neuronen, evenals steuncellen zoals astrocyten, oligodendrocyten en microglia. Ze combineerden dit met ruimtelijke genkaarten uit een andere menselijke dataset om deze celtypen terug te plaatsen in de bekende gelaagde structuur van de cortex.
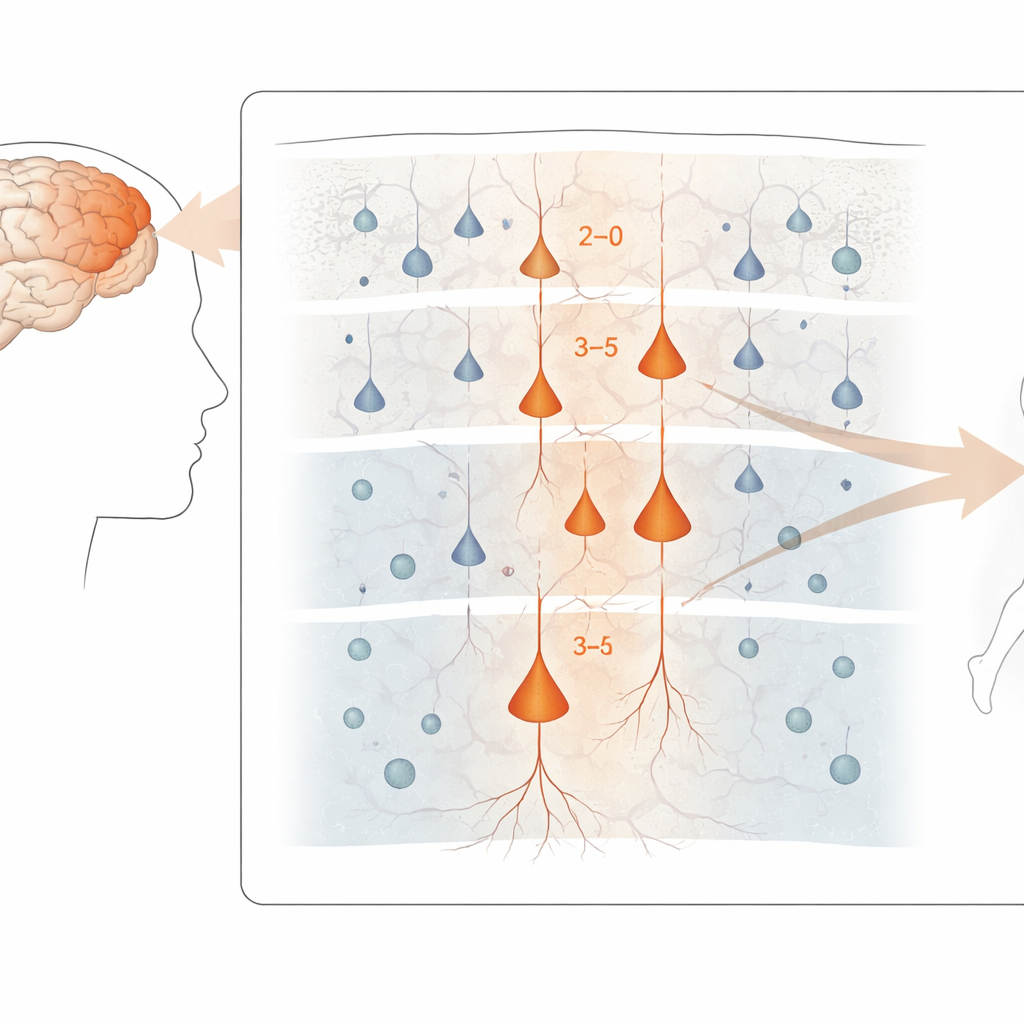
De meest kwetsbare neuronen aanwijzen
Door de motorische cortex heen waren de sterkste ziektegerelateerde genveranderingen zichtbaar in exciterende neuronen, de cellen die activiteit door hersencircuits voortdrijven. Vooral bovenste en middelste laagsneuronen die verbindingen binnen de cortex leggen, evenals bepaalde diepe-laagcellen die signalen uit de cortex voeren—including de grote “Betz”-cellen die spinale motorneuronen aansturen—tonen de meest uitgesproken veranderingen. Ter vergelijking: remmende interneuronen en veel gliacellen waren op het niveau van genexpressie minder getroffen, hoewel sommigen subtielere verschuivingen vertoonden. Ondanks deze moleculaire onrust was de algehele samenstelling van de belangrijkste celtypes in het weefsel verrassend vergelijkbaar tussen patiënten en controles, wat suggereert dat de schade meer over functieverlies van cellen gaat dan simpelweg over het aantal verloren cellen.
Hoe TDP-43 van binnenuit genactiviteit hervormt
Om effecten die direct door TDP-43 worden veroorzaakt te scheiden van andere ziekteprocessen, gebruikte het team een slimme sorteerstrategie. Ze labelden kernen met antilichamen tegen TDP-43 en een neuronale marker, en gebruikten vervolgens flowcytometrie om neuronen te scheiden waarvan de kernen TDP-43 hadden verloren (een teken van pathologie) van neuronen die het behielden. Het sequencen van meer dan 12.000 van deze kernen toonde aan dat verlies van TDP-43 overweldigend plaatsvond in exciterende neuronen, vooral in specifieke subtypen in lagen 2–3, 3–5, 5 en 6. In die kwetsbare neuronen waren honderden genen ontregeld, waaronder veel die al met ALS waren geassocieerd. Klassieke moleculaire tekenen van TDP-43-dysfunctie—zoals het verschijnen van “cryptische” extra stukjes in STMN2- en KALRN-transcripten, en verschuivingen in waar RNA-moleculen worden geknipt en uitgeregen aan hun uiteinden—waren duidelijk verrijkt in de TDP-43–deficiënte kernen.
Epigenetische herstructurering: niet alle verandering komt door TDP-43
Aangezien ze zowel genactiviteit als chromatine-openheid in dezelfde kernen maten, konden de auteurs nagaan welke veranderingen samenhingen met verschuivingen in DNA-verpakking. Ze vonden tienduizenden plekken in het genoom waar lokale chromatine-toegankelijkheid correleerde met genexpressie. Veel van de genen die in ALS en ALS-FTD veranderd waren, lagen in zulke regio’s, wat aangeeft dat een deel van het ziektekenmerk bredere epigenetische herstructurering weerspiegelt in plaats van directe gevolgen van TDP-43-verlies. Interessant genoeg convergeerden deze chromatine-gerelateerde veranderingen vaak op signaalroutes die betrokken zijn bij celcommunicatie en axongeleiding, en waren ze bijzonder sterk in bepaalde exciterende neuronen en oligodendrocyten. Toen het team genveranderingen gerelateerd aan TDP-43-pathologie vergeleek met die gerelateerd aan chromatineverschuivingen, zagen ze dat deze deels overlappen maar grotendeels verschillende lagen van verstoring vormen.
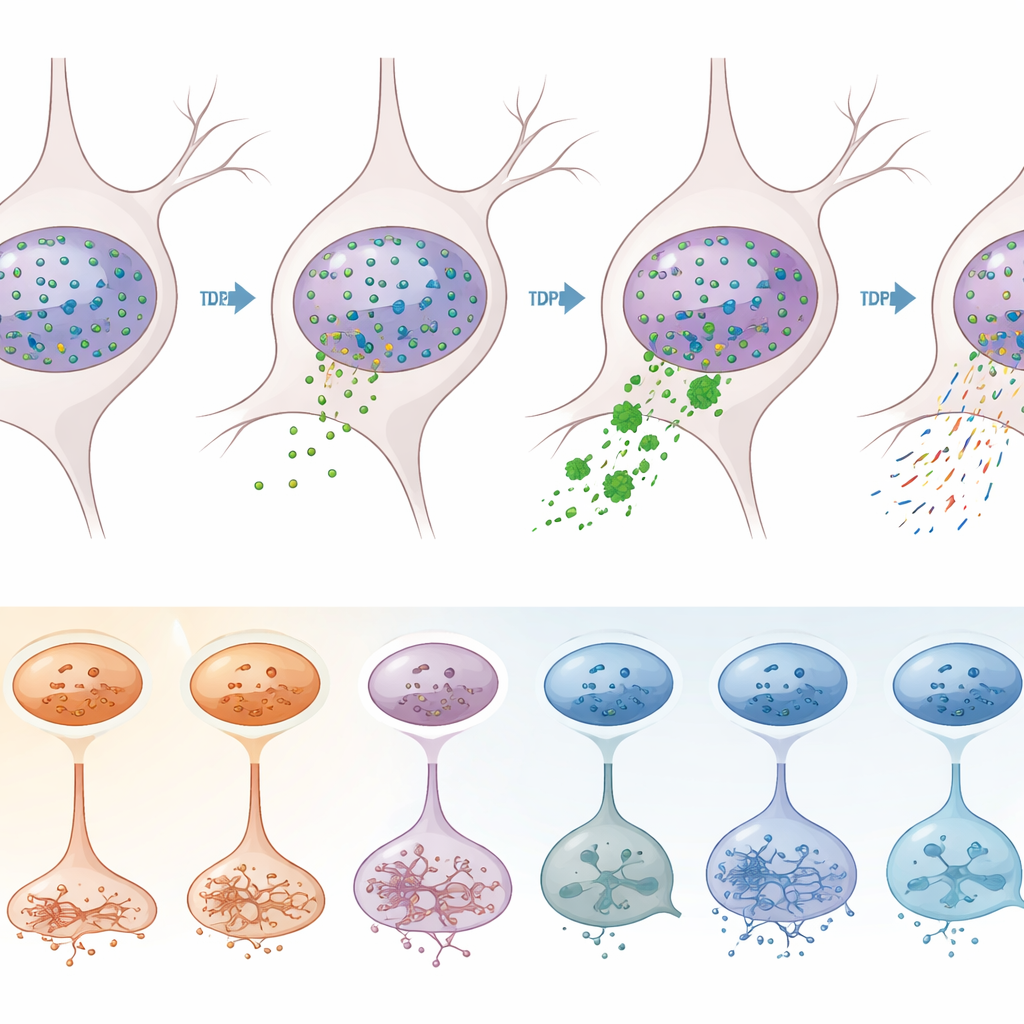
Wat dit betekent voor toekomstige therapieën
Voor de niet-specialistische lezer is de kernboodschap dat ALS en ALS-FTD de motorische cortex niet uniform beschadigen. In plaats daarvan treffen ze specifieke typen exciterende neuronen en, in mindere mate, bepaalde steuncellen, en veranderen ze hun genprogramma’s op manieren die zowel afhankelijk zijn van het disfunctioneren van TDP-43 als van bredere veranderingen in de wijze waarop DNA wordt verpakt en afgelezen. Deze bevindingen suggereren dat effectieve behandelingen zowel cel-type specifiek als routespecifiek moeten zijn—bijvoorbeeld het herstellen van TDP-43-functie of het corrigeren van zijn splicingfouten in de meest kwetsbare neuronen, terwijl tegelijk epigenetische en signaleringsveranderingen worden aangepakt die meerdere celtypes delen. Door dit complexe landschap in hoge resolutie in kaart te brengen, biedt de studie een blauwdruk voor het ontwerpen van nauwkeurigere interventies gericht op het vertragen of voorkomen van verlies van bewegingscontrole bij ALS en ALS-FTD.
Bronvermelding: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
Trefwoorden: ALS, frontotemporale dementie, TDP-43, neuronen van de motorische cortex, single-nucleus multiomics