Clear Sky Science · nl
VAMP7-afhankelijke late endosomale secretie van ER- en mitochondriale eiwitten beïnvloedt het tumor-micro-omgeving en de betrokkenheid van macrofagen
Hoe gestreste cellen om hulp signaleren
Kankercellen hebben het zwaar. Uitgehongerd van zuurstof en voedingsstoffen hopen zich beschadigingen op in de kleine energiecentrales (mitochondriën) en eiwitfabrieken (endoplasmatisch reticulum, of ER) binnenin. Deze studie onthult een onverwachte manier waarop onder druk staande cellen beschadigde stukjes van deze binnenstructuren naar buiten toe afvoeren. In hersentumoren die glioblastomen worden genoemd, blijkt dit cellulaire "vuilnisexport"-systeem, aangedreven door een eiwit genaamd VAMP7, van invloed te zijn op hoe immuuncellen het tumorweefsel waarnemen en binnendringen.
Verborgen vervoersroutes binnenin cellen
De meeste eiwitten die een cel verlaten gebruiken een klassieke route: ze komen het ER binnen, passeren een centraal sorteerstation genaamd het Golgi-apparaat en worden daarna verpakt in kleine blaasjes die met het celoppervlak fuseren. Maar cellen vertrouwen ook op onconventionele routes die het Golgi omzeilen. Een dergelijke route gebruikt late endosomen—interne zakjes die met het oppervlak kunnen samensmelten en hun inhoud naar buiten kunnen vrijgeven. De auteurs richten zich op een moleculair "rits"-eiwit, VAMP7, dat al bekendstaat om te helpen bij het fuseren van late endosomen met het buitenmembraan en het vrijgeven van kleine extracellulaire vesikels, piepkleine pakketjes die lading tussen cellen vervoeren.
Versleten onderdelen naar de uitgang verplaatsen
Met behulp van genetisch gemodificeerde ratnierkliere- en gliomacellen zonder VAMP7 volgden de onderzoekers wat er gebeurt met eiwitten die normaal in het ER en de mitochondriën voorkomen. Ze toonden aan dat cellen zonder VAMP7 veel minder van een korte vorm van een ER-vormend eiwit genaamd RTN3 en van VDAC, een kanaal op het mitochondriale oppervlak, vrijlieten. Tegelijkertijd raakten late endosomen verkeerd gepositioneerd en werden kleine vesikels rijk aan de marker CD63 slecht uitgescheiden. Hoge-resolutiebeeldvorming en nabijheidsassays lieten zien dat RTN3 en mitochondriaal materiaal fysiek geassocieerd zijn met CD63-positieve late endosomen voordat ze worden vrijgegeven, en dat deze overdracht afhankelijk is van VAMP7 en zijn partner-fusie-eiwitten. Deze bevindingen ondersteunen een model waarin gestreste ER en mitochondriën kleine vesikels afsnoeren die fuseren met late endosomen, die vervolgens hun lading buiten de cel exporteren. 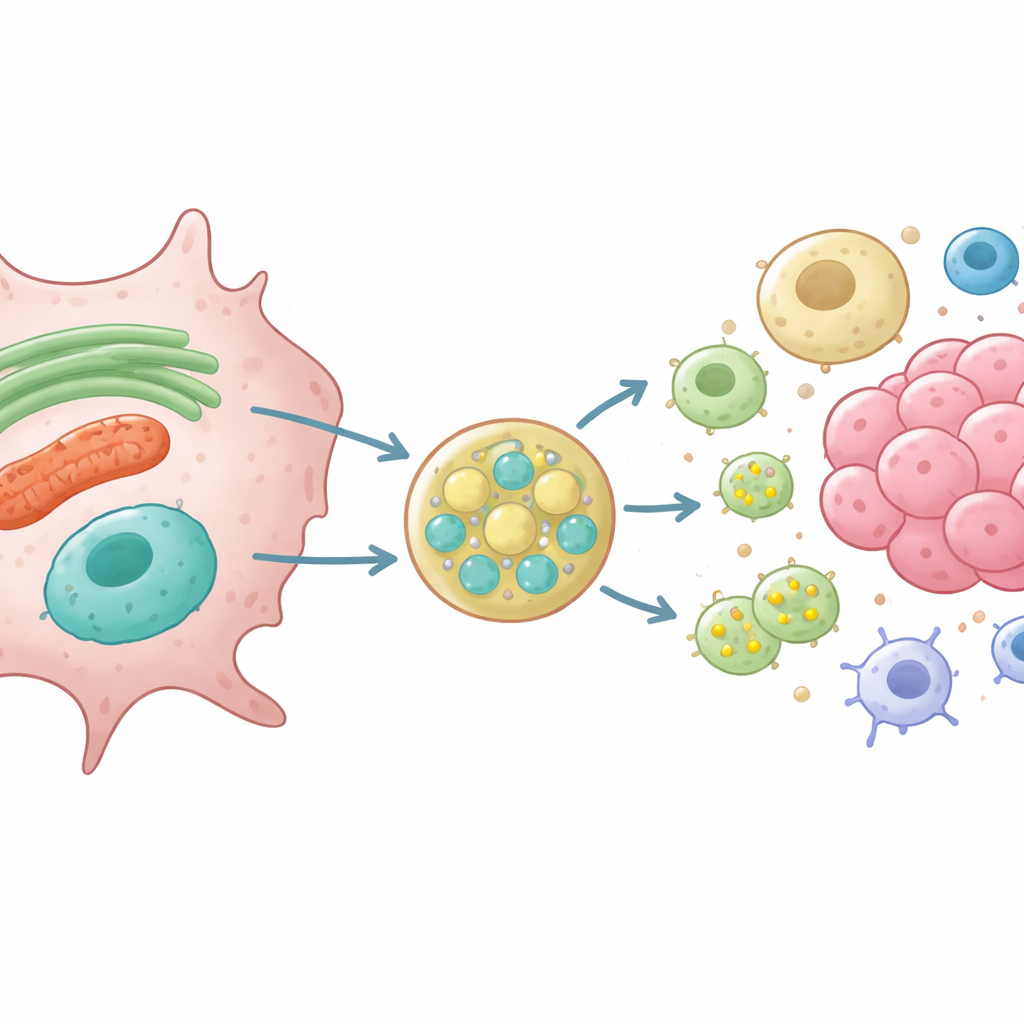
Stressvermindering en kwaliteitscontrole
Cellen zonder VAMP7 verloren niet de algemene recyclingroute die bekendstaat als autofagie, maar ze vertoonden wel duidelijke tekenen van spanning. Genexpressiepatronen wezen op activatie van stressreacties in het ER en veranderingen in mitochondriële genen. Microscopie toonde abnormale "wervelingen" van ER-membraan en overmatig gefuseerde, verlengde mitochondriën, beide kenmerkend voor organellen die moeite hebben hun evenwicht te bewaren. Metingen van zuurstofverbruik toonden aan dat, ondanks een grotere mitochondriale massa, cellen zonder VAMP7 of zonder een cruciaal autofagie-eiwit (ATG5) zwakkere energieproductie hadden. Toen de wetenschappers opzettelijk ER- of mitochondriale stress opwekten met medicijnen, verhoogden cellen met intacte VAMP7 de secretie van respectievelijk RTN3 of VDAC. Deze toename verdween wanneer VAMP7 werd verwijderd, wat impliceert dat late endosomale secretie werkt als een overdrukventiel om beschadigde componenten af te voeren en de interne toestand van de cel uit te zenden.
De tumoromgeving vormgeven
Om het belang van deze route in ziekte te testen, wendde het team zich tot een ratmodel van glioblastoom, een zeer agressieve hersentumor. Ze implanteerden normale, VAMP7-deficiënte of ATG5-deficiënte gliomacellen in rattenhersenen. Tumoren die voortkwamen uit VAMP7-ontbrekende cellen werden groot en bevatten veel meer dood weefsel, maar werden door minder macrofagen geïnfiltreerd—de immuuncellen die puin opnemen en kunnen beïnvloeden of een tumor groeit of stagneert. Ter vergelijking: tumoren zonder ATG5 waren over het algemeen kleiner maar toonden niet dezelfde selectieve afname van macrofaagbinnendringing in de tumorkern. Analyses van menselijke hersentumor-datasets toonden verder aan dat lagere expressie van VAMP7 (en RTN3) geassocieerd is met slechtere patiëntoverleving, wat suggereert dat deze stressgekoppelde secretieroute van nature kan bijdragen aan het remmen van tumorprogressie door het immuunlandschap te vormen. 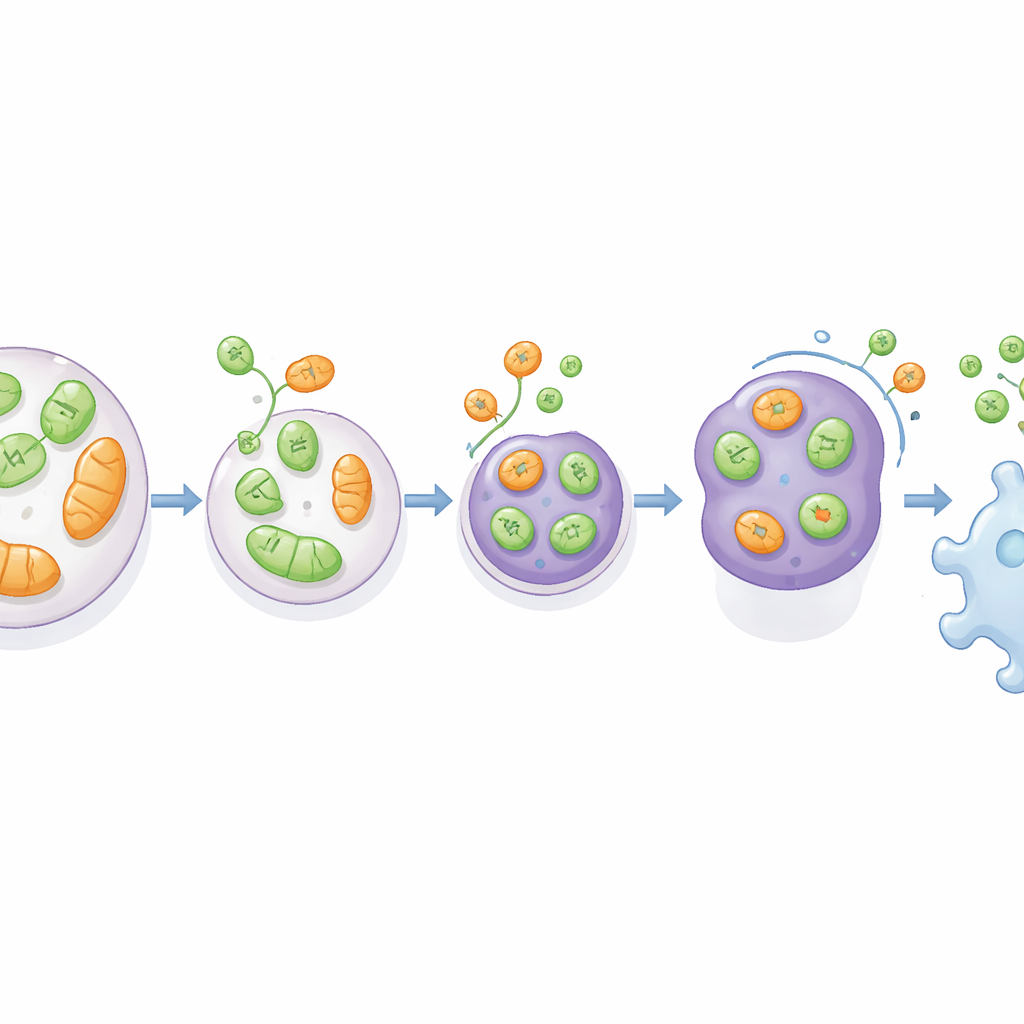
Waarom dit belangrijk is voor kanker en immuniteit
Kort gezegd stelt de studie voor dat VAMP7 cellen helpt beschadigde onderdelen van hun interne machinerie te verpakken en via late endosomen naar buiten te exporteren, vooral onder stress. In glioblastoom lijkt deze uitgaande stroom van ER- en mitochondriële afgeleide materialen te fungeren als een noodsignaal dat macrofagen aanmoedigt de tumor binnen te gaan en puin op te ruimen, wat bijdraagt aan een meer tumorremmende omgeving. Wanneer VAMP7 ontbreekt, verzwakt het signaal, hoopt organelbeschadiging zich op, worden tumoren necrotischer en neemt de betrokkenheid van macrofagen af. Begrijpen en mogelijk bijsturen van dit secretie-gebaseerde kwaliteitscontrolesysteem zou nieuwe wegen kunnen openen om hardnekkige tumoren zichtbaarder en responsiever voor het immuunsysteem te maken.
Bronvermelding: Vats, S., Dionisio, P., Lemercier, Q. et al. VAMP7-dependent late endosomal secretion of ER and mitochondrial proteins impacts the tumor microenvironment and macrophage engagement. Nat Commun 17, 3012 (2026). https://doi.org/10.1038/s41467-026-69900-4
Trefwoorden: onconventionele eiwitsecretie, VAMP7, glioblastoom, tumor-micro-omgeving, extracellulaire vesikels