Clear Sky Science · nl
Eukaryotische initiatiefactor 6 beïnvloedt de plasticiteit van kleincellige longkanker via de integrine-FAK signaleringsas
Waarom dit longkankeronderzoek ertoe doet
Kleincellig longcarcinoom (SCLC) is een van de dodelijkste vormen van longkanker. Het reageert aanvankelijk vaak goed op chemotherapie, maar keert bijna altijd terug, snel en agressief. Deze studie behandelt een centrale vraag: wat stelt SCLC-cellen in staat om van “persoonlijkheid” te veranderen en drugresistent te worden, en kan dat veranderingsvermogen worden vertraagd of geblokkeerd?
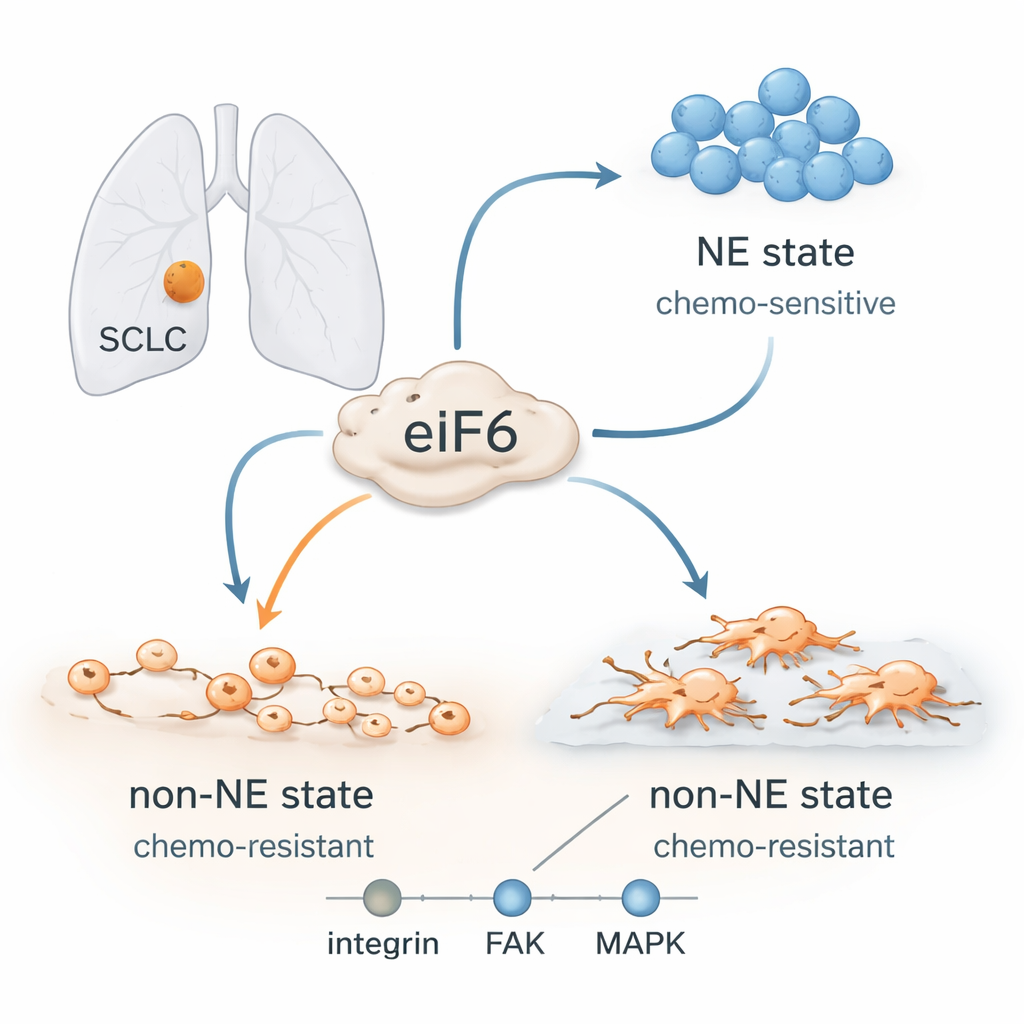
Vormveranderende kankercellen
Artsen dachten vroeger dat SCLC een uniforme ziekte was, maar inmiddels is duidelijk dat deze tumoren verschillende celtypes bevatten. Sommige cellen hebben een sterke “neuro-endocriene” identiteit: ze groeien in dichte zwevende clusters, reageren goed op platinumgebaseerde chemotherapie en bevatten vaak veel bepaalde zenuwachtige eiwitten. Andere verliezen deze identiteit en nemen een “niet-neuro-endocriene” staat aan: ze spreiden zich uit, hechten zich aan het omringende weefsel, vertonen kenmerken van mobielere, invasieve cellen en zijn veel moeilijker te doden met medicijnen. Tumoren van patiënten evolueren tijdens of na behandeling vaak van de gevoelige naar de resistente staat, hoewel hun DNA niet veel verandert. Dat wijst op flexibele celprogramma’s in plaats van nieuwe mutaties als motor van terugkeer.
Een translatiefactor met een dubbelrol
De auteurs richtten zich op een eiwit genaamd eIF6, vooral bekend van zijn rol bij de assemblage van ribosomen, de eiwitfabrieken van de cel. Door patiëntmonsters, muismodellen en meerdere menselijke SCLC-celijnen te bestuderen, ontdekten ze dat eIF6-niveaus consequent stegen wanneer cellen overschakelden naar de drugresistente, niet-neuro-endocriene staat. Verassend genoeg ging deze toename samen met een algemene daling in de totale eiwitsynthese, wat suggereert dat eIF6 meer doet dan zijn tekstboekfunctie. Gedetailleerde analyses van hoe boodschapper-RNA’s aan ribosomen binden toonden aan dat de basisribosomale componenten weinig veranderden. In plaats daarvan werd de manier waarop boodschappen voor translatie werden geselecteerd en verwerkt heringericht toen cellen van identiteit veranderden.
Loskomen om aan overlevingssignalen te koppelen
Dieper gravend ontdekte het team dat eIF6 in resistente cellen deels losraakt van ribosomen en zich associeert met een oppervlakte-signaleringshub rond integrines en een eiwit genaamd focal adhesion kinase (FAK). Integrines helpen cellen hun omgeving te voelen en zich eraan vast te hechten; FAK geeft die signalen naar binnen door en activeert vaak paden die migratie, overleving en geneesmiddel-tolerantie ondersteunen. Biochemische pull-downs en nabijheidsassays in cellen toonden aan dat eIF6 fysiek interageert met de integrinepartner CD104 en met FAK, en dat deze complexen overvloediger zijn in niet-neuro-endocriene cellen. Deze eIF6–integrine–FAK-assemblage verhoogt op haar beurt de activiteit in het MAPK-signaleringspad, een bekende aanjager van groei en stressresistentie.
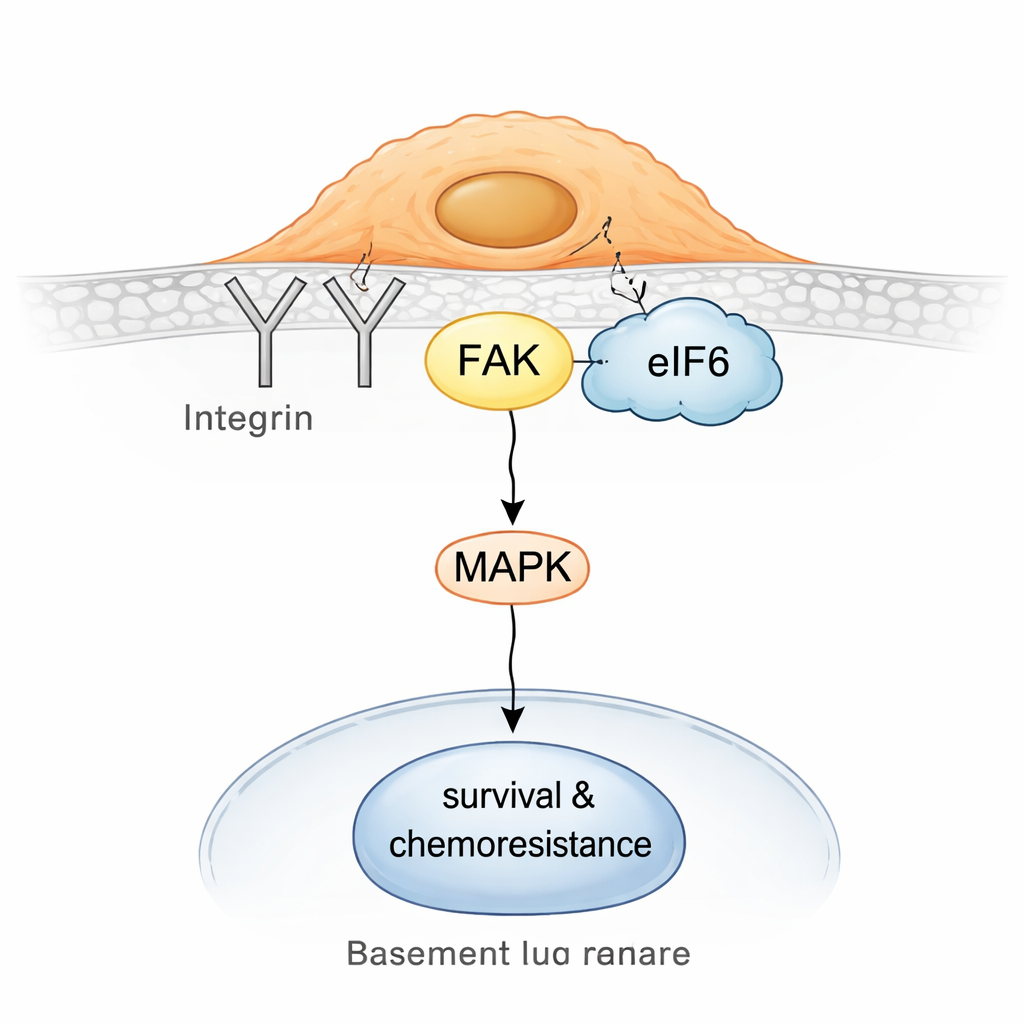
Resistente tumoren weer kwetsbaar maken
De onderzoekers vroegen zich vervolgens af of manipulatie van eIF6 het gedrag van SCLC kon veranderen. Wanneer ze eIF6-niveaus verlaagden in resistente cellen, werden genen die samenhangen met een mobiele, littekenvorming-achtige (epitheliaal–mesenchymaal) programmareactie naar beneden bijgesteld, terwijl klassieke neuro-endocriene genen gedeeltelijk werden hersteld. Deze veranderingen draaiden de klok niet volledig terug, maar vertraagden de overgang naar de resistente staat. Cruciaal is dat cellen met minder eIF6 gevoeliger werden voor de standaard carboplatinum–etoposide chemotherapie in kweek en in muistumoren, met minder overlevende kolonies en een duurzamere krimp. Omdat er momenteel geen specifieke remmers van eIF6 bestaan, testte het team FAK-remmers die al in klinische ontwikkeling zijn. Het blokkeren van FAK-signaalgeving herkoppelde resistente cellen naar gevoeligheid voor chemotherapie en in muizen gaf de combinatiebehandeling de sterkste tumorgroei-onderdrukking.
Van laboratoriuminzichten naar toekomstige patiëntinstrumenten
Tenslotte onderzochten de auteurs tumormonsters van patiënten met beperkt stadium SCLC die een operatie hadden ondergaan. Met een gevoelige kleuringstechniek die eiwitten alleen laat oplichten als ze dicht bij elkaar zitten, maten ze hoe vaak eIF6 in complex zit met CD104 of FAK binnen tumorcellen. Hoge niveaus van deze complexen—meer nog dan eIF6 alleen—hingen samen met vroegere terugkeer en kortere overleving, waarmee ze veelbelovende prognostische markers vormen. Samengevat laat dit werk zien dat eIF6 ‘‘een dubbelleven’’ kan leiden buiten ribosomen om kankercellen aan krachtige overlevingscircuits te koppelen. Door deze eIF6–integrine–FAK-as in kaart te brengen, suggereert de studie manieren om patiënten met een hoger terugkeringsrisico te identificeren en ondersteunt zij het combineren van FAK-remmers met chemotherapie om de gevaarlijke plasticiteit van SCLC tegen te gaan.
Bronvermelding: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Trefwoorden: kleincellige longkanker, drugresistentie, celplasticiteit, eIF6, integrine FAK-signaleringspad