Clear Sky Science · nl
Contextafhankelijke remming van translatie als therapeutische benadering bij kanker
De eiwitfabrieken tegen kanker keren
Kankercellen overleven doordat ze voortdurend grote hoeveelheden kortlevende "driver"-eiwitten produceren die hun groei en deling in stand houden. Deze studie onderzoekt een nieuwe manier om kanker te bestrijden door de eiwitproducerende machines van de cel—de ribosomen—subtiel te blokkeren, maar alleen wanneer ze proberen bepaalde eiwitsequenties te maken, met name die in moeilijk te bestrijden oncogenen zoals MYC. Die selectieve verstoring zou tumorcellen kunnen doden terwijl veel van de normale eiwitsynthese gespaard blijft.
Hoe cellen eiwitten bouwen—en waar het mis kan gaan
Elke cel is afhankelijk van ribosomen, kleine moleculaire fabrieken die genetische boodschappen (mRNA) lezen en aminozuren aan elkaar rijgen tot eiwitten. De meeste bestaande middelen die ribosomen remmen, zoals antibiotica of oudere kankergeneesmiddelen, werken als botte instrumenten: ze schakelen de eiwitsynthese breed uit, wat gezonde cellen kan beschadigen en ernstige bijwerkingen kan veroorzaken. De auteurs redeneerden dat omdat elke nascent eiwitketen zijn eigen unieke sequentie en chemische eigenschappen heeft, het mogelijk zou kunnen zijn kleine moleculen te ontwerpen die alleen het ribosoom blokkeren wanneer een specifieke sequentie in de machine zit, en de rest van de eiwitproductie grotendeels ongemoeid laten.
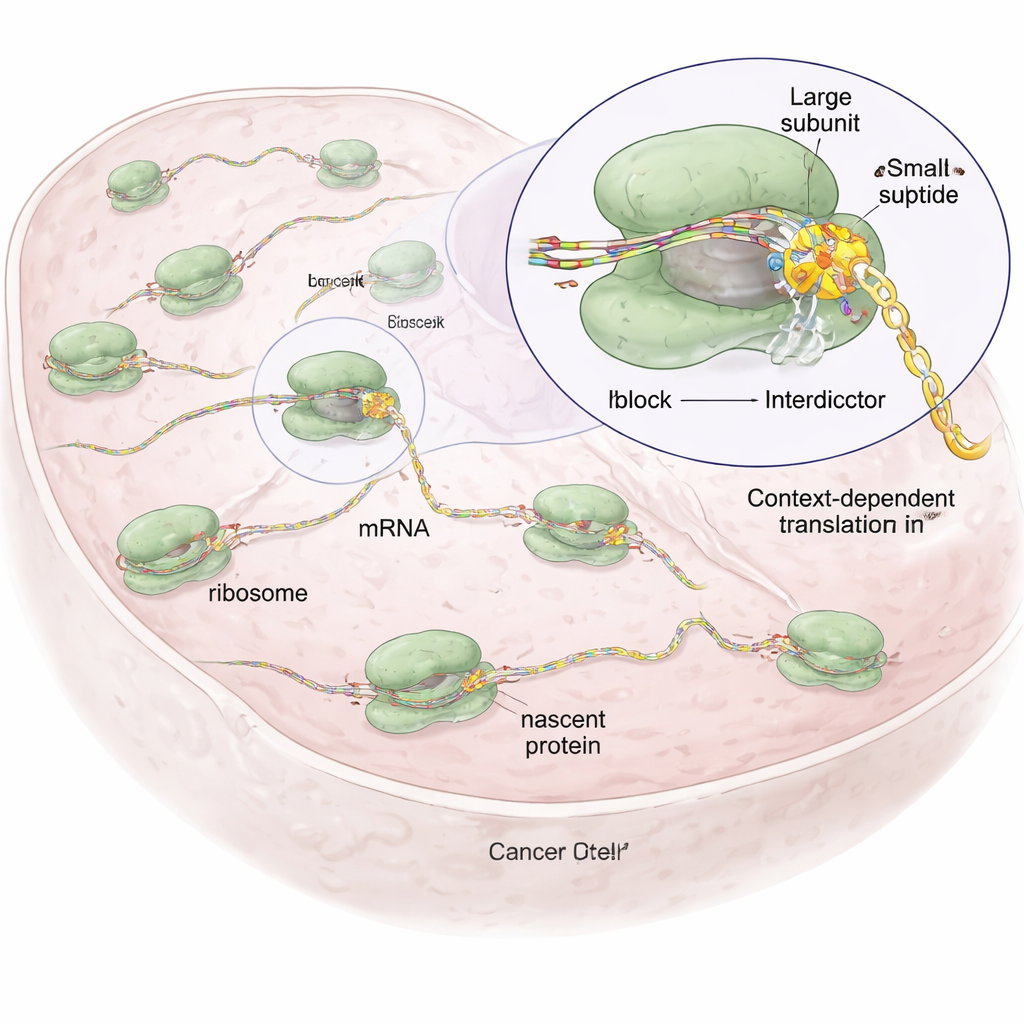
Ontworpen moleculen die alleen bij bepaalde eiwitsequenties stagneren
Voortbouwend op een natuurlijk verbinding genaamd anisomycine, dat zich bindt aan het katalytische hart van het ribosoom waar peptidebindingen worden gevormd, creëerden de onderzoekers een familie synthetische moleculen die zij "interdictors" noemen. Ze delen allemaal een kernscaffold die hen in het ribosoom verankert, maar ze verschillen in zijketens die richting de groeiende eiwitketen wijzen. Die zijketens zijn afgestemd op bepaalde typen aminozuren—bijvoorbeeld een interdictor (IDB-001) is aangetrokken tot negatief geladen residuen, terwijl een andere (IDB-002) de voorkeur geeft aan kleine, olieachtige (hydrofobe) residuen. Met een techniek genaamd ribosoomprofilering, die wereldwijd in kaart brengt waar ribosomen vertragen op mRNAs in cellen, toonde het team aan dat elke verbinding stalling veroorzaakt bij onderscheidende korte motieven in de nascente keten, vaak bij het voorlaatste (−1) aminozuur, wat wijst op sequentieafhankelijke werking in plaats van een willekeurige uitschakeling.
Het middel en het ribosoom atoom voor atoom zien samenkomen
Om te begrijpen hoe deze selectiviteit fysiek werkt, bevroor de groep menselijke ribosomen terwijl ze ontworpen peptidesequenties vertaalden en beeldde ze deze af met cryo-elektronenmicroscopie bij bijna-atomaire resolutie. Ze zagen de interdictor genesteld in de actieve plek van het ribosoom en precieze contacten maken met de laatste paar aminozuren van de nascente keten. In één structuur wordt een hydrofobe zijketen van IDB-002 opgevangen door kleine, niet-ruimtelijke resten in het peptide, wat verklaart waarom grotere zijketens daar ongunstig zijn. In een andere structuur zwaait de zure zijketen van een MYC-afgeleid residu om een zoutbrug te vormen met een positief geladen groep op IDB-001. De aanwezigheid van het geneesmiddel duwt ook nabijgelegen basen van ribosomale RNA naar nieuwe posities die de actieve plaats vernauwen en de instroom van het volgende tRNA gedeeltelijk blokkeren, wat helpt de elongatie bij die favoriete sequenties te bevriezen.
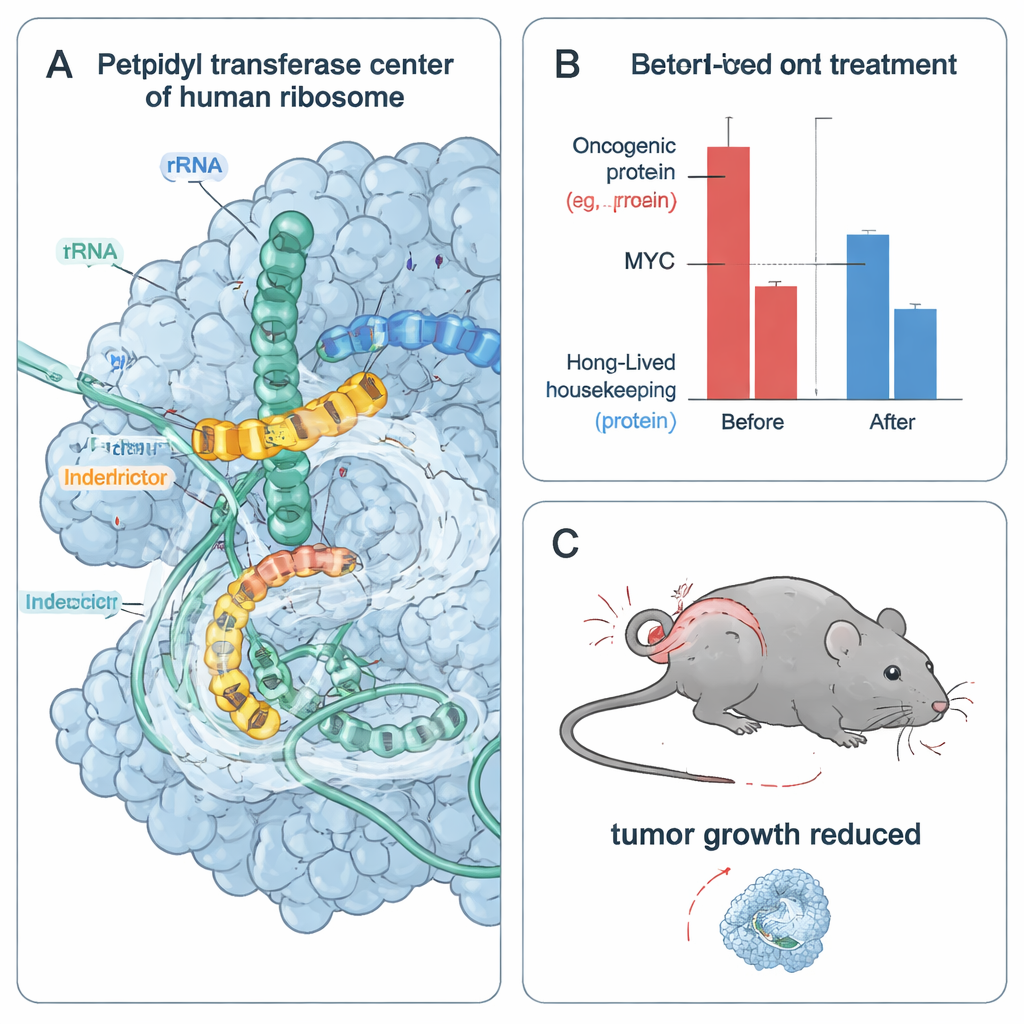
Van vastgelopen ribosomen naar gestreste en stervende tumorcellen
Aangezien snel delende kankercellen sterk afhankelijk zijn van kortlevende oncogene eiwitten zoals MYC en CCND1, testte het team hoe interdictors het overleven van tumorcellen beïnvloeden. In meerdere MYC-afhankelijke kankercellijnen verminderden IDB-001 en IDB-002 de celviabiliteit bij nanomolaire tot lage micromolaire concentraties. Een verder geoptimaliseerd analoog, IDB-003, bleek nog krachtiger en geschikt voor orale toediening. In cellen leidden deze verbindingen snel tot uitputting van MYC en andere snel turnoverende oncoproteïnen terwijl langerlevende huishoudelijke eiwitten relatief stabiel bleven in hetzelfde tijdvenster. De middelen veroorzaakten ook cellulaire stressreacties die verband houden met botsende ribosomen, maar het blokkeren van die stress-signaleringsroutes verwijderde de verminderde levensvatbaarheid niet, wat suggereert dat directe uitputting van essentiële oncogene eiwitten een belangrijke oorzaak van tumorceldood is.
Proof of concept in een lastig borstkankermodel
Om te onderzoeken of deze benadering in dieren werkt, behandelden de auteurs muizen met humane triple-negatieve borstkankertumoren met oraal toegediende IDB-003. Over 28 dagen groeiden de behandelde tumoren veel langzamer dan die in controledieren, met tot 80% remming van tumorgroei bij hogere doses en geen ernstige toxiciteit gerapporteerd in deze studie. Genexpressie-analyse van de tumoren toonde sterke downregulatie van MYC-doelgenprogramma's, consistent met verminderde MYC-activiteit in vivo. Samen wijzen deze resultaten erop dat selectief het ribosoom laten stagneren op specifieke eiwitsequenties tumoren kan verzwakken die afhankelijk zijn van instabiele oncogene drivers, terwijl men mogelijk de brede toxiciteit van klassieke translatieblokkers vermijdt.
Waarom dit belangrijk is voor toekomstige kankerbehandelingen
Dit werk introduceert een nieuw soort klein-molecuul geneesmiddel: een dat niet werkt door te binden aan een voltooid eiwit, maar dat het eiwit onderschept terwijl het wordt gemaakt en alleen wanneer een korte "adreslabel"-sequentie aanwezig is. Omdat veel kankeverwekkende eiwitten flexibel, kortlevend of zonder duidelijke bindingspockets zijn voor conventionele middelen, kan het rechtstreeks richten op hun synthese aan het ribosoom een weg openen om tumoren te behandelen die worden aangedreven door momenteel "on-druggable" genen zoals MYC. De studie suggereert ook dat door de chemie van interdictors af te stemmen, toekomstige geneesmiddelen kunnen worden ontworpen om zich op verschillende sequentiemotieven en ziektes te richten, waarmee deze strategie verder reikt dan oncologie naar andere aandoeningen waarbij het terugschakelen van specifieke eiwitten de gezondheid zou kunnen herstellen.
Bronvermelding: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Trefwoorden: ribosoomgerichte kankertherapie, remming van translatie, MYC-gedreven tumoren, contextafhankelijke kleine moleculen, triple-negatieve borstkanker