Clear Sky Science · nl
TRIM13 in situ-engineering versterkt anti-inflammatoire vermogen van CAR-Ms voor therapie van leverfibrose
De opruimploeg van de lever herprogrammeren
Leverfibrose, een littekenproces dat kan leiden tot cirrose en leverfalen, treft miljoenen mensen en heeft momenteel weinig effectieve behandelingen. Deze studie onderzoekt een manier om de eigen immuuncellen van de lever te benutten en te herprogrammeren zodat ze niet alleen cellen die littekenweefsel vormen verwijderen, maar ook schadelijke ontsteking dempen — mogelijk een veiliger en krachtiger therapie voor chronische leverziekten.
Waarom leverlittekens zo moeilijk te stoppen zijn
Wanneer de lever herhaaldelijk beschadigd raakt—door virussen, alcohol of metabole aandoeningen—probeert hij te genezen door littekenweefsel aan te leggen. Gespecialiseerde cellen, hepatische stercellen, schakelen over naar een “geactiveerde” toestand en produceren taaie vezels, vergelijkbaar met bouwvakkers die beton storten. Na verloop van tijd vervormt deze littekening, bekend als fibrose, het orgaan en belemmert het zijn functie. Immuuncellen die macrofagen worden genoemd, staan centraal in dit proces. In een beschadigde lever kunnen ze als een tweesnijdend zwaard werken: in de ene modus stimuleren ze ontsteking en activeren ze stercellen; in een andere, meer herstellende modus helpen ze littekenweefsel af te breken en het evenwicht te herstellen.
Schadelijke signalen omzetten in behulpzame signalen
De onderzoekers richtten zich op een belangrijk alarmsignaal in beschadigde lever: mitochondriaal DNA dat uit gewonde cellen lekt. Macrofagen herkennen dit DNA via een route die bekendstaat als cGAS‑STING, wat hen in een pro-inflammatoire, pro-fibrotische toestand duwt. Een eiwit genaamd TRIM13 helpt normaal gesproken STING in toom te houden door het te markeren voor afbraak. Het team redeneerde dat het verhogen van TRIM13 binnen levermacrofagen hen terug kon zetten naar een kalmerende, weefselherstellende modus. Tegelijk wilden ze deze cellen direct laten jagen op en verwijderen van de stercellen die littekenweefsel vormen. Hiervoor gebruikten ze het concept van de chimerische antigeenreceptor (CAR), ontleend aan kankertherapie: een synthetische receptor die immuuncellen in staat stelt een gekozen doelwit te herkennen—in dit geval een eiwit genaamd FAP dat overvloedig aanwezig is op geactiveerde stercellen.
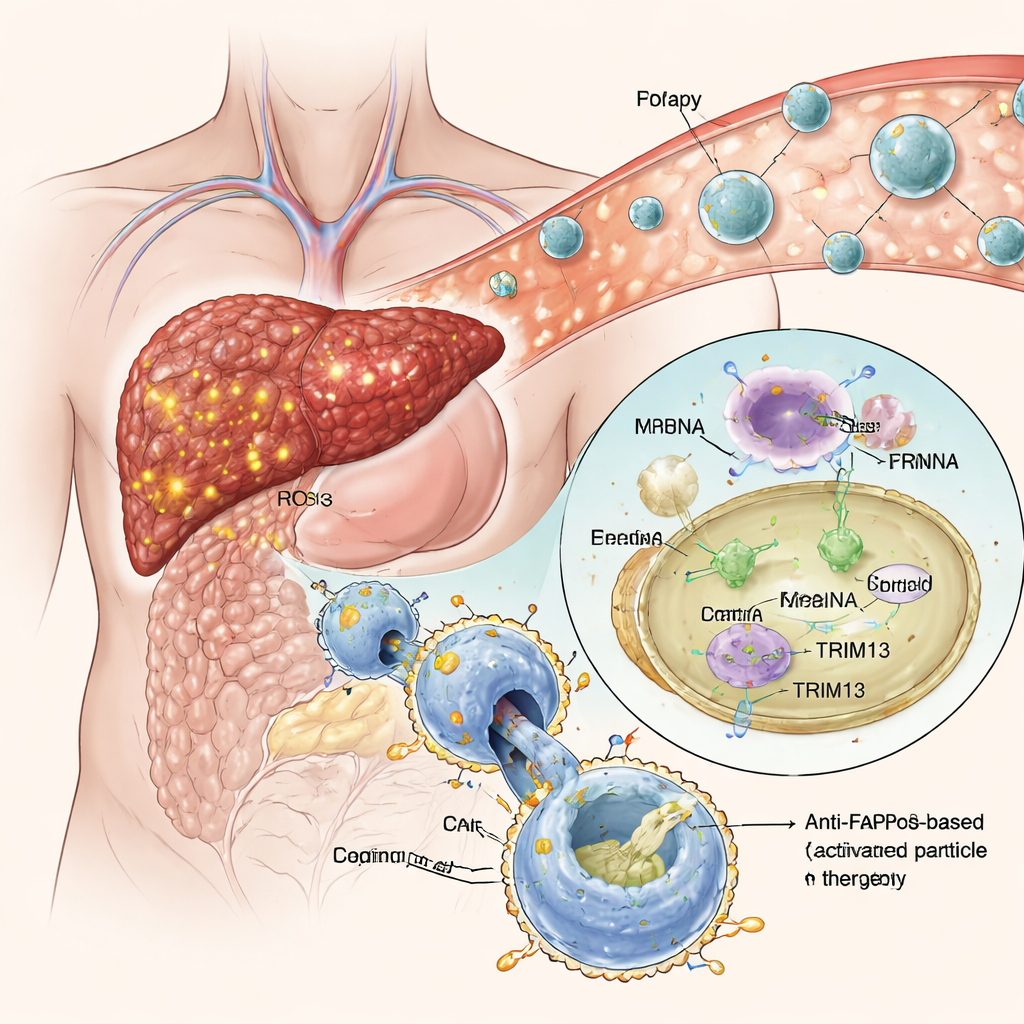
Slimme nanodeeltjes die naar ziek weefsel trekken
In plaats van macrofagen buiten het lichaam te bewerken, ontwikkelde het team “efferocytose‑geactiveerde” lipide‑nanodeeltjes—kleine vetbolletjes die genetische instructies in de vorm van boodschapper‑RNA (mRNA) dragen. Deze deeltjes zijn bekleed met een vermomde vorm van fosfatidylserine, een natuurlijk “eet‑mij”-signaal dat stervende cellen tonen om macrofagen aan te trekken. In de hoog‑oxiderende omgeving van fibrotisch leverweefsel wordt de vermomming verwijderd en het signaal onthuld, waardoor nabijgelegen macrofagen de nanodeeltjes opnemen. Eenmaal binnen wordt het mRNA vrijgegeven en door de cel gelezen, wat leidt tot productie van zowel TRIM13 als de anti‑FAP CAR. In kweekexperimente lukte deze benadering erin macrofagen richting een anti‑inflammatoire toestand te sturen terwijl ze een sterke, selectieve voorkeur kregen voor FAP‑positieve littekenvormende cellen, zonder hun normale vermogen om ander afval te ruimen te verstoren.
Van zieke naar regenererende lever bij muizen
Het team testte deze strategie vervolgens in muismodellen van leverfibrose veroorzaakt door ofwel een toxische chemische stof ofwel door een vetrijk, voedings‑tekort dieet. Systemisch geïnjecteerde nanodeeltjes bereikten efficiënt de lever en werden, vooral in fibrotische dieren, voornamelijk door macrofagen opgenomen. Daar toonden de gemodificeerde cellen verminderde activiteit van de STING‑route en lagere productie van ontstekingsmoleculen, samen met verbeterde vernietiging van geactiveerde stercellen. Weefselanalyses toonden opvallende dalingen in collageen en andere littekenmarkers, een fijner en meer normaal extracellulair matrix‑patroon, en verbeterde bloedwaarden van leverfunctie. De lever van behandelde muizen vertoonde meer delende cellen en herwonnen een gezondere architectuur, wat wijst op echte orgaanherstel in plaats van slechts een tijdelijke demping van ontsteking.
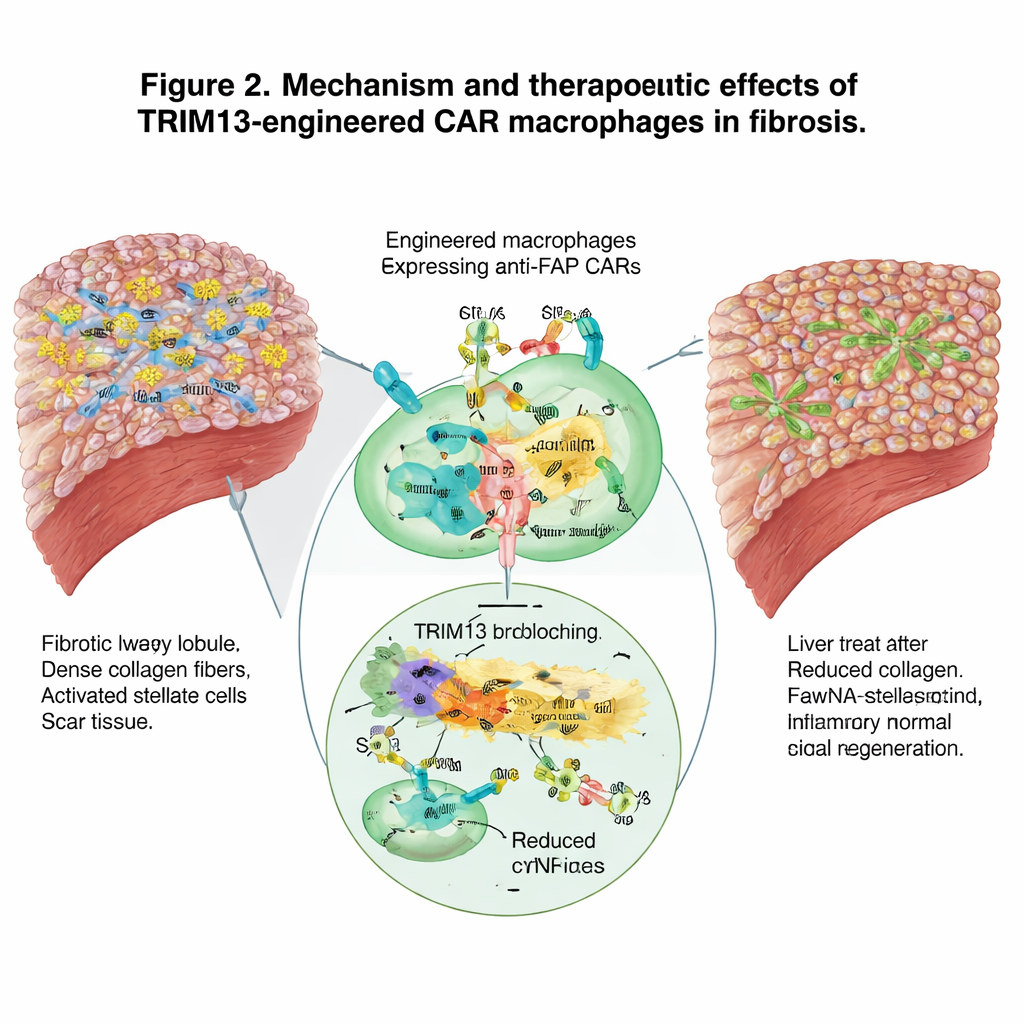
Het bredere immuunsysteem inschakelen
Naast directe verwijdering van littekenweefsel vormden de gemodificeerde macrofagen het bredere immuunlandschap om. Ze verschoofen van een agressief, schadebevorderend profiel naar een meer oplossend, herstellend profiel en verminderden ontstekingssignalen in het bloed. Tegelijkertijd fungeerden ze door het verslinden van littekenvormende cellen als leraren voor het adaptieve immuunsysteem, door neutrofielen, dendritische cellen en T‑cellen aan te trekken en een gecoördineerde respons tegen het fibrotische weefsel te stimuleren. Single‑cell RNA‑sequencing van leverimmuuncellen bevestigde een verschuiving weg van pro‑inflammatoire genprogramma’s en naar een verbeterd vermogen om schadelijke cellen en restant‑materiaal te fagocyteren en te verwijderen.
Wat dit voor patiënten zou kunnen betekenen
Voor een niet‑specialistische lezer is de kernboodschap dat dit werk wijst op een manier om de eigen afvalopruimers van de lever te “heropvoeden”, zodat ze zowel littekenweefsel ontmantelen als de chronische alarmsignalen uitschakelen die de schade in stand houden. Door kortdurende mRNA‑instructies te gebruiken verpakt in slimme nanodeeltjes, voorkomt de therapie permanente verandering van cellen en beperkt ze de activiteit tot zieke regio’s, wat bijwerkingen kan verminderen. Hoewel er nog veel meer tests nodig zijn voordat dit bij mensen kan worden geprobeerd, schetst deze strategie een veelbelovend raamwerk voor de behandeling van leverfibrose—en mogelijk andere fibrotische aandoeningen—door het eigen immuunsysteem van het lichaam te transformeren van een aanjager van littekenvorming naar een actieve partner in genezing.
Bronvermelding: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Trefwoorden: leverfibrose, macrofagen‑therapie, nanodeeltje mRNA-afgifte, chimerische antigeenreceptor, TRIM13 STING-route