Clear Sky Science · nl
ERCC6L2 waarborgt nauwkeurige reparatie van verspringende-einden DNA dubbelstrengsbreuken
Waarom deze ontdekking belangrijk is voor ons DNA
Elke cel in je lichaam loopt voortdurend schade op aan haar DNA, vooral het gevaarlijkste type: breuken die beide strengen van de dubbele helix doorsnijden. Als deze breuken niet correct worden gerepareerd, kunnen ze leiden tot kanker, erfelijke aandoeningen of mislukte medische genoombewerking. Deze studie onthult een eerder ondergewaardeerd "beschermend" eiwit, ERCC6L2, dat specifiek één lastig type breuk beschermt tegen het veranderen in grote gaten en verstoorde chromosomen. Inzicht in deze beschermer helpt een zeldzame menselijke beenmergaandoening te verklaren en waarschuwt dat bepaalde genbewerkingstechnieken mogelijk averechts kunnen werken bij kwetsbare patiënten.
Verschillende soorten DNA-breuken, verschillende risico's
Niet alle DNA-breuken zijn gelijk. Sommige sneden zijn schoon, waarbij beide strengen op hetzelfde punt worden doorgesneden, alsof je een touw recht doorsnijdt. Andere zijn getrapt en laten korte overhangende uiteinden achter die niet precies uitlijnen. Moderne genoomeditors zoals Cas9 maken meestal schone, stomp afgesneden breuken, terwijl hulpmiddelen zoals Cas12a, TALENs en sommige gepaarde nickase-systemen verspringende, overhangende breuken veroorzaken. De onderzoekers vergeleken systematisch hoe menselijke cellen met deze twee breuktypen omgaan door duizenden genen uit te schakelen en te onderzoeken welke genen vooral belangrijk waren voor het repareren van elk type snede.
Een verborgen beschermer voor verspringende breuken
Uit deze genoom-brede screens bleek ERCC6L2 een cruciale beschermer voor verspringende breuken, maar grotendeels overbodig voor stompe breuken. Cellen zonder ERCC6L2 konden stompe Cas9-snedes nog steeds herstellen met alleen kleine inserties of deleties, de typische signaturen van routinematige DNA-reparatie. In scherp contrast daarmee produceerden ERCC6L2-deficiënte cellen, wanneer verspringende breuken werden veroorzaakt door Cas12a, TALENs of dubbele-nickase Cas9, veel meer grote deleties tot duizenden DNA-letters en ruim uit elkaar liggende chromosomale herschikkingen, translocaties genoemd. Deze effecten werden niet alleen gezien in gemodificeerde cellijnen, maar ook in beenmergcellen van patiënten met erfelijke ERCC6L2-mutaties, wat de klinische relevantie van de bevinding onderstreept. 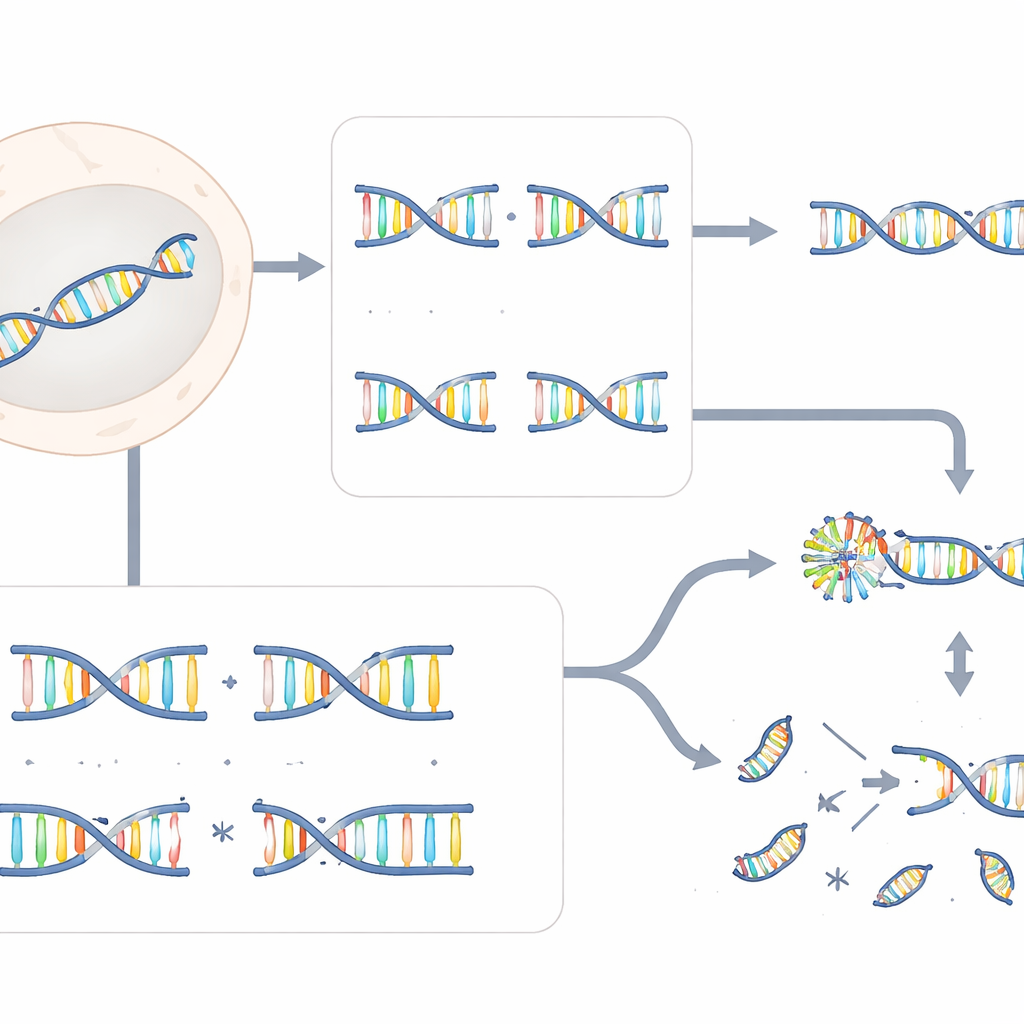
Wanneer veel sneden zich opstapelen, falen cellen
De gevaren van het verliezen van ERCC6L2 werden nog duidelijker toen het team meerdere verspringende breuken tegelijk over het genoom induceerde. In deze experimenten hadden cellen zonder ERCC6L2 moeite om te overleven en vormden ze vaak micronuclei—kleine, verkeerd geplaatste DNA-bevattende lichaampjes die aangeven dat chromosomen verbrijzeld of verkeerd gesegregeerd zijn. Dezelfde kwetsbaarheid verscheen toen de onderzoekers een natuurlijke bron van verspringende breuken gebruikten: het enzym TOP2, dat tijdelijk het DNA knipt om torsie tijdens normale celactiviteiten te verlichten. Het chemotherapeuticum etoposide houdt TOP2 in zijn gebroken toestand gevangen, waardoor deze tijdelijke knipjes veranderen in blijvende verspringende breuken. Cellen zonder ERCC6L2 waren zeer gevoeliger voor etoposide en vertoonden buitensporige erosie van DNA-einden, wat overeenkwam met wat werd gezien bij Cas12a-geïnduceerde breuken.
Hoe ERCC6L2 het schadeapparaat reguleert
Om te begrijpen hoe ERCC6L2 op moleculair niveau werkt, reconstrueerde het team het proces in een reageerbuis met gezuiverde eiwitten en DNA. Ze vonden dat ERCC6L2 aan veel DNA-vormen bindt maar een bijzondere vaardigheid heeft: het kan actief korte overhangende eindjes op verspringende breuken "smelten" of ontwinden, en dat vereist zijn energieverbruikende motoractiviteit. In cellen balanceert ERCC6L2 een ander reparatiemechanisme, het MRN-complex, dat normaal gesproken DNA-einden afknabbelt om stukken enkelstrengs DNA te creëren. Deze resectie is nuttig in sommige reparatieroutes maar wordt gevaarlijk wanneer die te ver gaat, wat leidt tot grote deleties en gebroken chromosomen. In ERCC6L2-deficiënte cellen loopt MRN-gedreven resectie onbelemmerd door bij verspringende breuken. Het blokkeren van MRN of zijn regelaar ATM keerde het buitensporige DNA-afknabbelen om en verminderde de frequentie van grote deleties, wat aantoont dat ERCC6L2 deze route normaal gesproken onder controle houdt.
Wat dit betekent voor patiënten en genoombewerking
Samengevoegd stellen de auteurs voor dat ERCC6L2 fungeert als een specialistische beschermer voor verspringende DNA-breuken. Door de overhangen te smelten en snelle, nette hersluiting te bevorderen, voorkomt het langdurig DNA-verlies en mis-koppeling tussen verre chromosomen. Bij mensen die met ERCC6L2-mutaties zijn geboren, hopen dagelijkse bronnen van verspringende breuken—met name die veroorzaakt door TOP2—waarschijnlijk ongerepareerd of foutief gerepareerd op, wat leidt tot beenmergfalen, leukemie en mogelijk bepaalde neurologische problemen. Voor gentherapie geeft dit werk een duidelijke boodschap: genoombewerkingshulpmiddelen die opzettelijk overhangende sneden veroorzaken, zoals Cas12a, TALENs of sommige nickase-ontwerpen, kunnen bijzonder riskant zijn bij deze patiënten. Het kiezen van bewerkingsstrategieën die verspringende breuken vermijden, kan essentieel zijn om te voorkomen dat het herstellen van één gen per ongeluk de rest van het genoom destabiliseert. 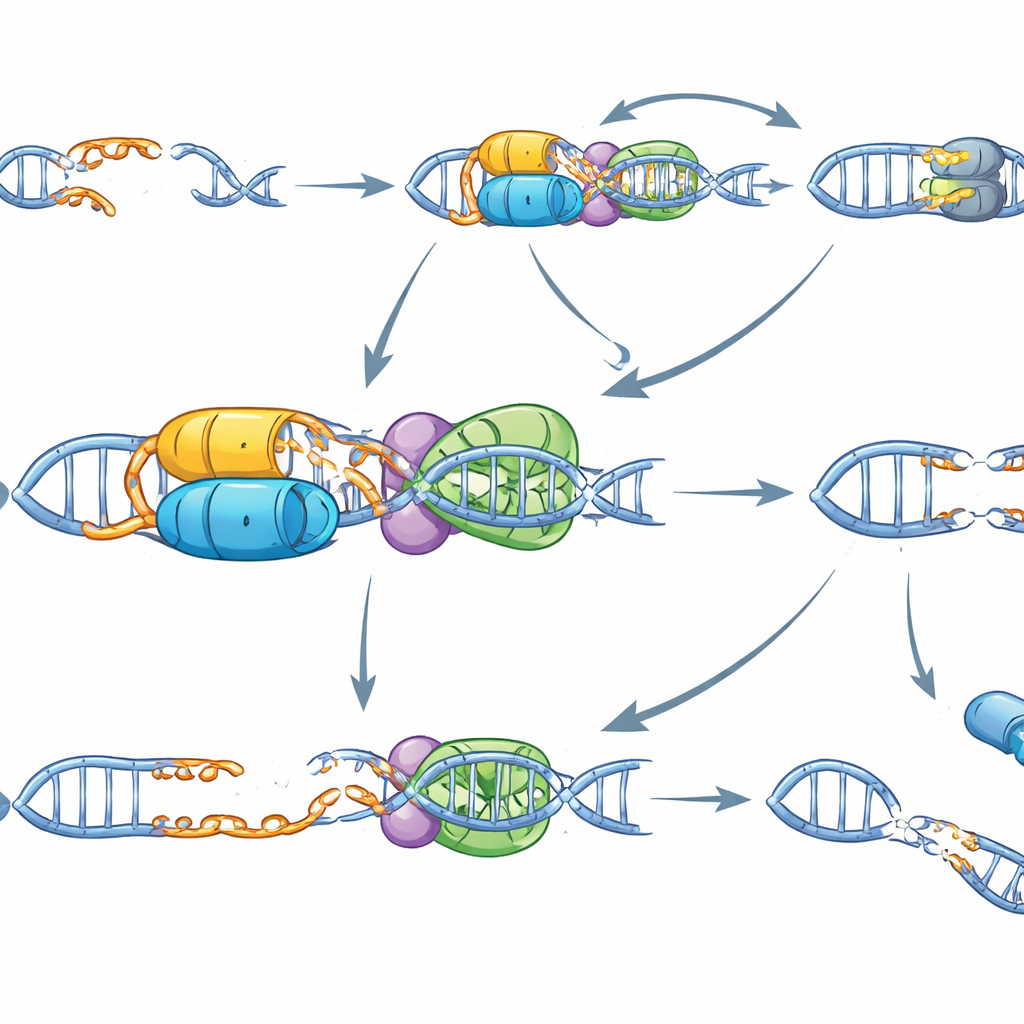
Bronvermelding: Aird, E.J., Serrano-Benitez, A., Siegner, S.M. et al. ERCC6L2 ensures repair fidelity for staggered-end DNA double-strand breaks. Nat Commun 17, 2743 (2026). https://doi.org/10.1038/s41467-026-69843-w
Trefwoorden: DNA-reparatie, genoombewerking, dubbelstrengsbreuken, ERCC6L2, chromosomale instabiliteit