Clear Sky Science · nl
Maximalisatie van energiegebruik en efficiëntie van lithiumlixivering via sequentiële elektrochemische dubbele oxidatie en weken‑ontspanning
Waarom oude autobatterijen nog steeds van belang zijn
Lithium‑ionbatterijen voeden onze telefoons, laptops en in toenemende mate ook onze auto's. Maar nu miljoenen pakketten van elektrische voertuigen het einde van hun levensduur bereiken, ontstaan er een nieuwe vorm van afval — en een nieuwe kans. Het lithium en andere metalen in gebruikte batterijen zijn waardevol, maar de terugwinning ervan vergt veel energie. Deze studie onderzoekt een slimmere manier om lithium terug te winnen met elektriciteit, efficiënter qua energiegebruik, met lagere kosten en een kleinere milieuvoetafdruk, zodat we kunnen voldoen aan de groeiende wereldwijde vraag naar batterijmaterialen.
Afvalbatterijen omzetten in een hulpbron
Tegenwoordig steunt de meeste industriële recycling van lithium‑ionbatterijen op agressieve chemicaliën of hoogtemperatuurovens. Deze methoden kunnen metalen terugwinnen, maar ze verbruiken vaak veel energie en maken het moeilijk om lithium schoon te scheiden van nikkel, kobalt en mangaan in zogeheten NCM‑batterijen. De onderzoekers richtten zich op een nieuwere, schonere route: met behulp van een elektrische stroom in zout water lithium uit het gebruikte kathodemateriaal trekken. Ze stelden een eenvoudige maar cruciale vraag: kunnen we het moment en de manier van stroomgebruik herschikken zodat bijna elk watt helpt lithium te verwijderen in plaats van verloren te gaan in nevenreacties?
Een tweestapsdans: kracht, dan stilte
Het team ontwierp een proces in twee fasen dat een actieve “duw” combineert met een stille “week”-fase. In de eerste fase, genoemd elektrochemische dubbele oxidatie, wordt een constante spanning aangelegd over een cel met een gebruikte NCM‑kathode en een natriumchlorideoplossing. De stroom trekt lithiumionen uit de vaste stof naar de vloeistof en vormt tegelijkertijd krachtige oxiderende soorten in de oplossing. De wetenschappers vonden dat het meeste nuttige werk in het eerste uur gebeurt: lithium verlaat de kristalstructuur snel aan het begin, maar later gaat veel energie verloren aan nevenreacties zoals zuurstofontwikkeling (bellen).
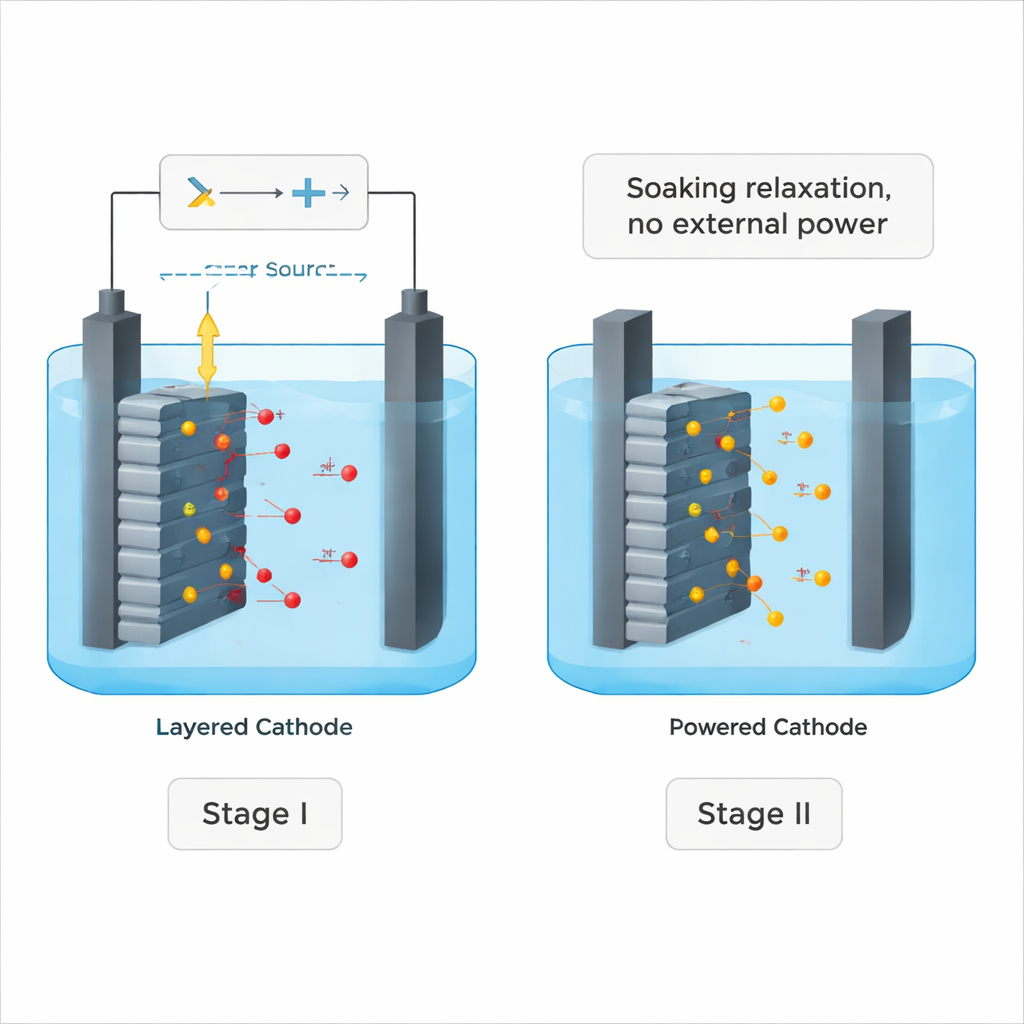
De chemie het werk laten afmaken
In plaats van de stroom langer en langer door te laten lopen, schakelden de onderzoekers de stroom simpelweg uit en lieten ze de elektrode weken in de inmiddels oxiderende zoutoplossing. Verrassend genoeg bleef lithium uitlogen totdat bijna alles was verwijderd — ongeveer 99% terugwinning voor vers NCM‑materiaal en rond de 98% voor echte gebruikte kathodes. Gedetailleerde metingen toonden aan dat zuurstofatomen in de kristalstructuur, die tijdens de geëlektrificeerde fase tijdelijk in een reactievollere toestand werden gebracht, de verborgen motor waren in deze tweede, stille fase. Deze “geactiveerde” zuurstofsoorten bevorderden een langzame uitwisseling: lithiumionen diffundeerden naar de vloeistof terwijl natrium‑ (of kalium‑)ionen uit de oplossing in de lege plaatsen glipten, alles zonder verdere elektrische input.
Hoe de kristalstructuur zich herschikt
Met elektronenmicroscopen, röntgendiffractie en spectroscopie observeerde het team hoe de kathodepartikels barstten, dunner werden en hun interne stapeling veranderde naarmate lithium vertrok. Het materiaal doorliep meerdere bekende gelaagde ordeningen toen het van lithiumrijk naar lithiumarm ging, eindigend in een natriumrijk vorm die de structuur bij elkaar hield maar niet veel lithium meer bevatte. Gedurende dit proces veranderden nikkel‑ en kobaltatomen hun ladingsstaten om het totale materiaal elektrisch in balans te houden, terwijl mangaan grotendeels onveranderd bleef en zo het kader stabiliseerde. De onderzoekers toonden ook aan dat kaliumionen, die hun watermoleculen gemakkelijker afstaan dan natrium, de ionenuitwisseling nog verder konden versnellen.
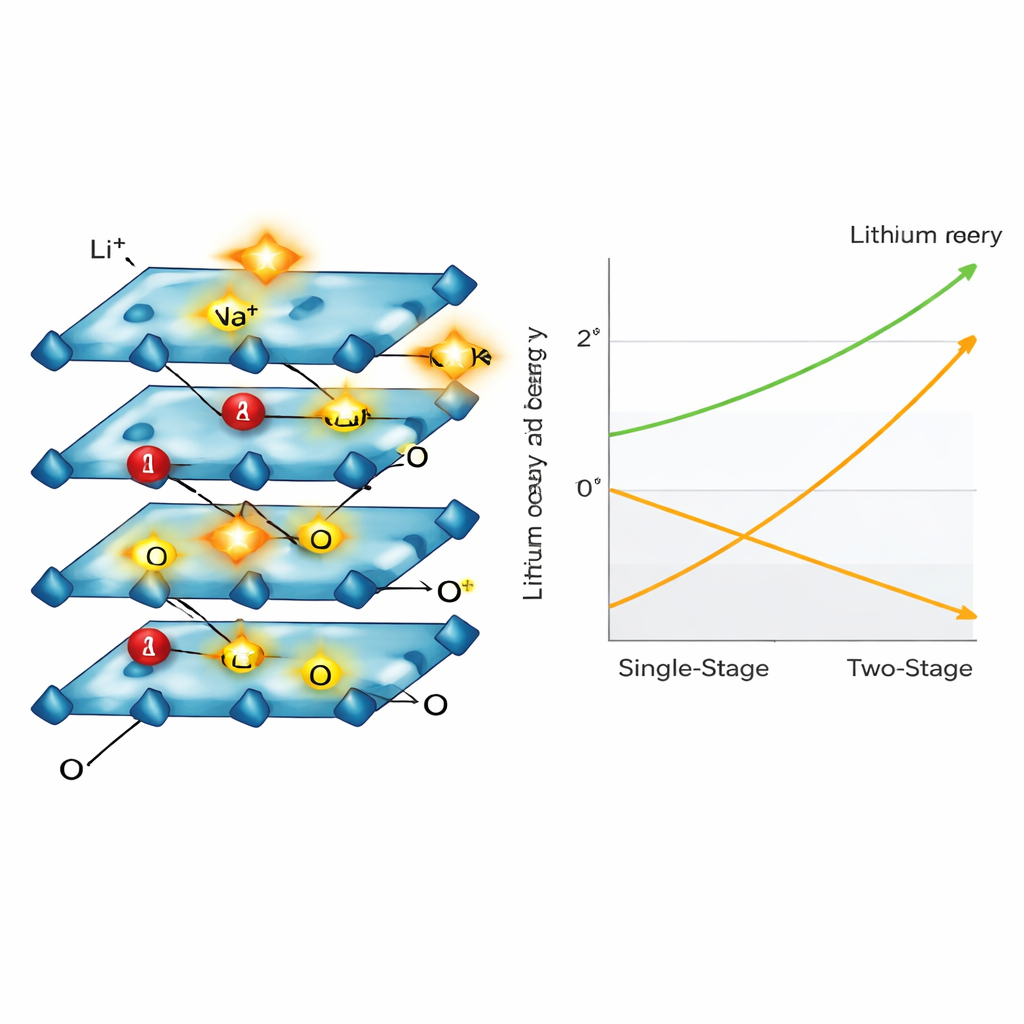
Van labbank naar industrievloer
Om te testen of dit idee buiten het lab kon werken, bouwde het team een pilotinstallatie die een halve kilogram echt batterijafval per partij kan behandelen. Met hun tweefasenmethode herwonnen ze meer dan 98% van het lithium als hoogzuivere lithiumcarbonaat, geschikt voor de productie van nieuwe batterijen. Cruciaal was dat, omdat de stroom wordt uitgezet zodra de “slimme chemie” in gang is gezet, het proces ongeveer de helft van de elektrische energie verbruikte vergeleken met een standaard eendelige elektrochemische methode, wat meer dan een vijfde van de totale operationele winst per ton gerecyclede kathodematerialen bespaarde.
Wat dit betekent voor toekomstige batterijen
In eenvoudige woorden toont de studie aan dat we niet altijd doorlopend elektriciteit hoeven te blijven toepassen om waardevolle materialen uit oude batterijen terug te winnen. Een welgetimede stoot energie kan het materiaal en de oplossing zodanig voorbereiden dat de rest van het werk uit zichzelf gebeurt, aangedreven door interne chemische krachten. Als deze tweefasenbenadering op grote schaal wordt toegepast, kan het recyclen van lithium uit gebruikte NCM‑batterijen goedkoper, schoner en aantrekkelijker voor de industrie maken, waardoor de circulaire keten van batterijen wordt gesloten en de druk op nieuwe lithiumwinning vermindert.
Bronvermelding: Zhong, W., Gu, X., Feng, X. et al. Maximizing energy utilization and lithium leaching efficiency via sequential electrochemical dual-oxidation and soaking-relaxation. Nat Commun 17, 2050 (2026). https://doi.org/10.1038/s41467-026-69834-x
Trefwoorden: lithiumrecycling, batterijafval, energiezuinige lixivering, NCM‑kathodes, elektrochemische terugwinning