Clear Sky Science · nl
Natuurlijk fotosynthetisch systeem voor het herstellen van de homeostase van het interactienetwerk van organellen in dieren
Plantkracht omzetten in een nieuw soort medicijn
Pijn in de rug door versleten tussenwervelschijven is een van de meest voorkomende redenen waarom mensen beperkingen in mobiliteit en kwaliteit van leven ervaren. Diep in die schijven raken kleine structuren binnen cellen uit balans door langdurige stress. Deze studie onderzoekt een verrassend eenvoudig idee met grote implicaties: de zonlichtgestuurde machinerie van planten lenen en die in dierlijke cellen installeren om hen te helpen weer in balans te komen en te genezen. 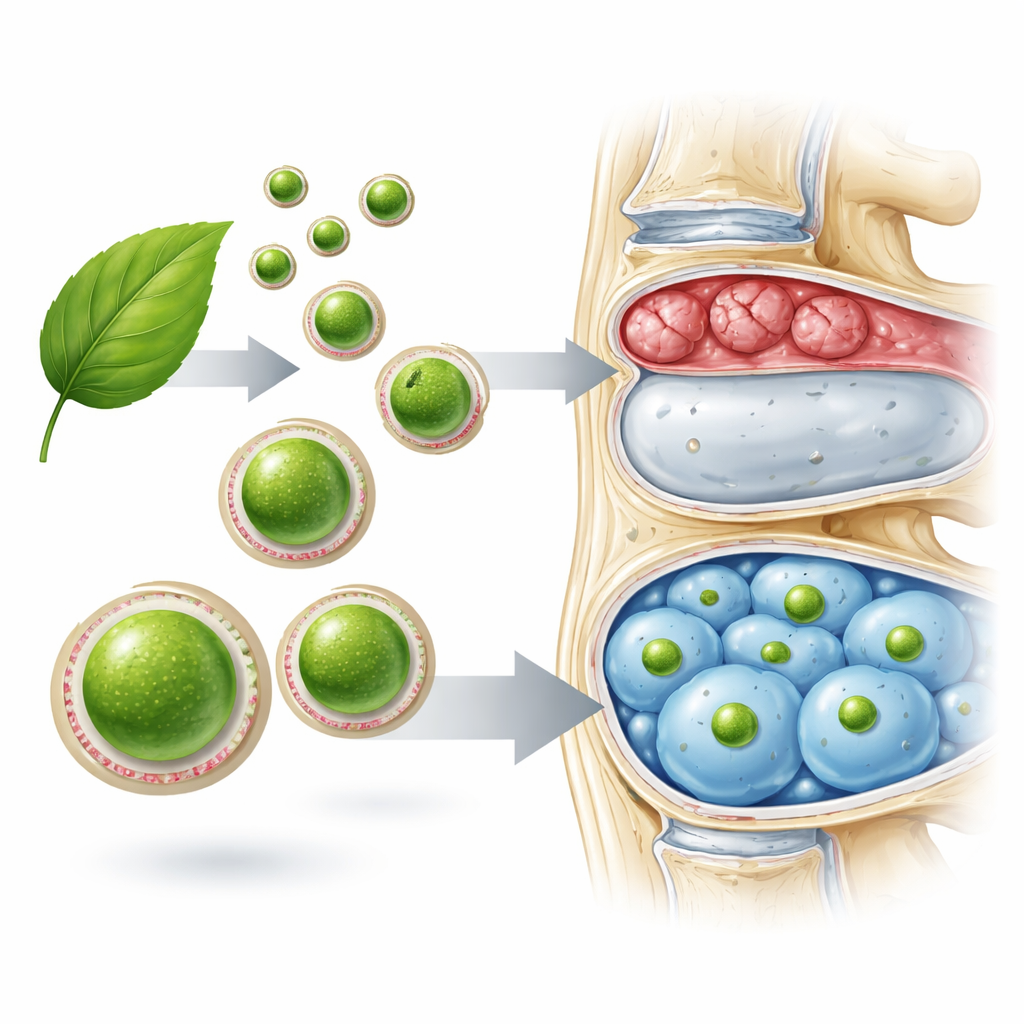
Wanneer celinterieurs uit balans raken
Onze cellen zitten vol miniatuuropdelingen, of organellen, die voortdurend met elkaar moeten communiceren. Twee van de belangrijkste zijn mitochondriën, die functioneren als energiecentrales, en het endoplasmatisch reticulum, een netwerk dat helpt bij het beheer van vetten, eiwitten en calciumsignalen. In weefsel van mensen met degenererende tussenwervelschijven vonden de onderzoekers dat deze communicatie verstoord raakt. Schijfcellen vertoonden stresssignalen, een overmaat aan reactieve zuurstofmoleculen en abnormale calciumwaarden. De contactzones waar mitochondriën en het endoplasmatisch reticulum elkaar raken werden te strak en te talrijk, wat leidde tot overbelaste, beschadigde mitochondriën die geen gezonde energieniveaus meer konden handhaven.
Fotosynthese smokkelen in dierlijke cellen
Planten kunnen goed omgaan met omgevingsstress omdat ze extra energie uit fotosynthese kunnen halen en hun interne chemie nauwkeurig kunnen regelen. De onderzoekers isoleerden kleine functionele eenheden uit spinazie-thylakoïdemembranen — in wezen nanoschaal fotosynthetische druppeltjes — en noemden ze nanothylakoïde-eenheden. Om deze veilig en doelgericht in schijfcellen te krijgen, omhulden ze de deeltjes met membranen afkomstig van nucleus pulposus-cellen, het belangrijkste celtype binnen tussenwervelschijven. Deze coating hielp de deeltjes afbraak te ontwijken, met doelcellen te versmelten en het afvalverwerkingssysteem van de cel te omzeilen. Eenmaal binnen en blootgesteld aan rood licht produceerden deze hybride deeltjes meetbare hoeveelheden ATP, de energievaluta van de cel, en genereerden ze ook NADPH, een sleutelmolecuul dat helpt bij het beheersen van oxidatieve stress.
Het gesprek tussen organellen herschakelen
Met zieke schijfcellen in kweek toonde het team aan dat licht-geactiveerde nanothylakoïde-eenheden de energieniveaus verhoogden en het evenwicht verschoof van afbraak naar opbouw van de ondersteunende matrix van het weefsel. Belangrijker nog, ze herstructureerden de interne organisatie van de cellen. Extra energie stelde het endoplasmatisch reticulum in staat zijn calciumreserves weer te vullen, waardoor vrij calcium in de rest van de cel en in mitochondriën daalde. Stressmarkers in het endoplasmatisch reticulum namen af. Microscopen lieten zien dat de abnormale over-contacten tussen mitochondriën en het endoplasmatisch reticulum ontspanden naar een meer normale afstand. Mitochondriën herwonnen een gezondere membraanpotentiaal, openden hun permeabiliteitspoorten minder vaak, produceerden meer eigen ATP en genereerden minder schadelijke reactieve zuurstofmoleculen. Tegelijkertijd liet lipidenanalyse zien dat de vetzusamenstelling van het endoplasmatisch reticulum verschoof naar meer onverzadigde triglyceriden, die geassocieerd worden met meer fluïde, flexibele membranen. Die toegenomen vloeibaarheid maakt contactpunten tussen organellen waarschijnlijk dynamischer en minder verankerd in een schadelijke, te strakke staat. 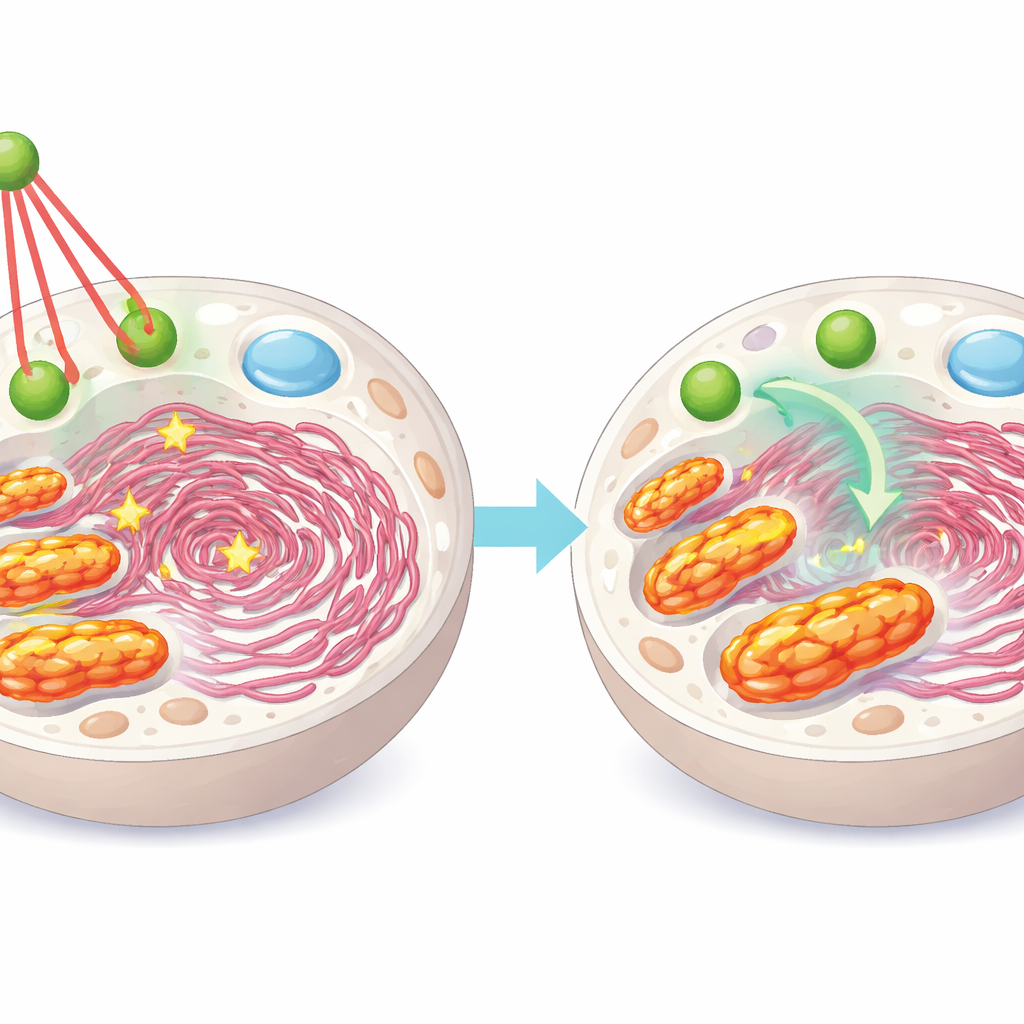
Van petrischaaltjes naar levende ruggen
Om te onderzoeken of deze plantgestuurde reparatiestrategie in echte dieren kon werken, gebruikten de wetenschappers rat- en konijnmodellen van schijfdegeneratie die waren veroorzaakt door naaldbeschadiging. Ze injecteerden de met membraan omhulde nanothylakoïde-eenheden in de beschadigde schijven en leverden rood licht. Bij ratten was extern licht voldoende om de oppervlakkige staartschijven te bereiken. Bij konijnen, waarvan de schijven dieper liggen, bouwde het team een klein implanteerbaar, draadloos gevoed lichtdiode-apparaat. Dit apparaat, verzegeld in een zachte, biocompatibele coating, kon op afstand via een smartphone worden ingeschakeld en geprogrammeerd. In beide diermodellen behielden met licht geactiveerde fotosynthetische deeltjes de schijven in betere conditie: ze behielden meer hoogte en water, hadden een gezondere weefselstructuur onder de microscoop en toonden meer van de sleutelmatrixeiwitten die schijven veerkrachtig houden. Op cellulair niveau verschenen dezelfde patronen: verminderde stresssignalen, genormaliseerde organelcontacten en beter bewaarde mitochondriën.
Een nieuwe manier om zonlicht in de geneeskunde te gebruiken
In gewone bewoordingen laat dit werk zien dat het mogelijk is een werkfragment van plantfotosynthese naar dierlijke cellen te verplaatsen en het te gebruiken als een levende microbatterij en chemische stabilisator. In plaats van één molecuul of pathway te targeten, duwt de benadering het hele interne netwerk van organellen zachtjes terug naar evenwicht — door energievoorziening te verbeteren, stress te verminderen, celmembranen te verzachten en krappe contacten tussen sleutelstructuren te versoepelen. In combinatie met draadloos gevoede implantaten die licht diep in het lichaam kunnen brengen, zou deze “fotosynthesetherapie” nieuwe wegen kunnen openen voor de behandeling van niet alleen degenererende tussenwervelschijven maar ook andere aandoeningen waarbij de interne organisatie en communicatie van celorganellen verstoord zijn.
Bronvermelding: Xia, C., Dai, Z., Wang, Y. et al. Natural photosynthetic system for restoring homeostasis of animal organelle interaction network. Nat Commun 17, 3087 (2026). https://doi.org/10.1038/s41467-026-69825-y
Trefwoorden: degeneratie van tussenwervelschijven, interactie tussen organellen, fotosynthetische nanodeeltjes, mitochondriën, draadloze lichttherapie