Clear Sky Science · nl
Cholecystokinine uit bètacellen stimuleert de ontwikkeling van obesitas-geassocieerd pancreasadenocarcinoom
Wanneer extra gewicht met de alvleesklier spreekt
Obesitas staat bekend om het verhogen van het risico op pancreaskanker, een van de dodelijkste vormen van kanker, maar het biologische “gesprek” dat overtollig lichaamsvet met tumoren verbindt is onduidelijk gebleven. Deze studie onthult een onverwachte boodschapper: een spijsverteringshormoon genaamd cholecystokinine, of CCK, dat wordt geproduceerd in de insulineproducerende cellen van de alvleesklier. Door te volgen hoe deze cellen veranderen onder metabole stress laten de auteurs zien hoe een hormoon dat bedoeld is om het lichaam te helpen juist kanker kan aanwakkeren, en ze suggereren nieuwe manieren om de ziekte te onderscheppen voordat die vat krijgt.
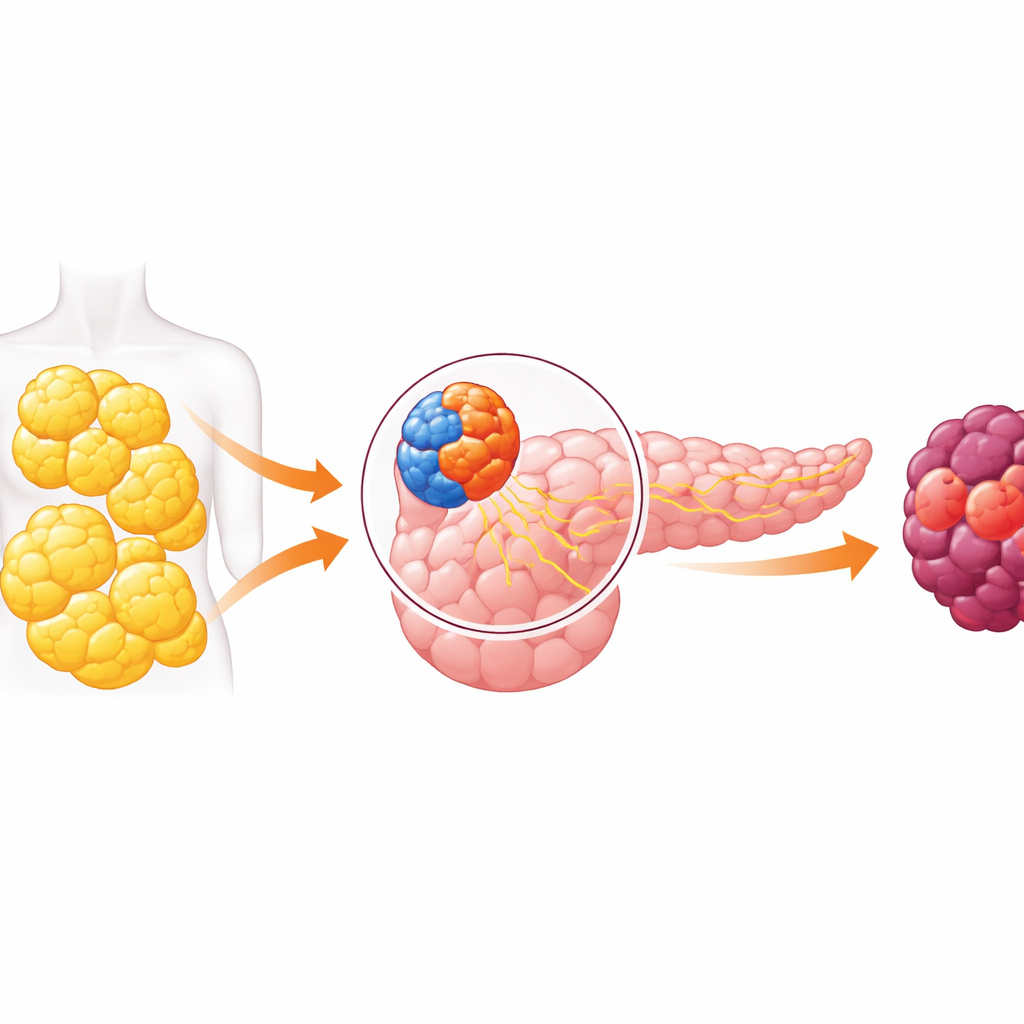
Een orgaan met twee gezichten en een gevaarlijke dialoog
De alvleesklier heeft twee hoofdrollen. De ene kant, het endocriene deel, bevat kleine eilandjes cellen die hormonen zoals insuline vrijgeven om de bloedsuikerspiegel te regelen. Het andere, het exocriene deel, maakt spijsverteringssappen en omvat de cellen waaruit meestal pancreaskanker ontstaat. Jarenlang gingen onderzoekers ervan uit dat deze compartimenten grotendeels geïsoleerd functioneerden. Recente studies hebben dat beeld omvergeworpen en laten zien dat signalen van hormoonproducerende cellen naburige spijsverteringscellen kunnen beïnvloeden. Dit artikel duikt in die kruisbestuiving en toont aan dat bij obesitas die communicatie het exocriene deel van de alvleesklier naar kanker kan duwen.
Stress in hormooncellen ontsteekt een nieuw signaal
Bij obesitas staan insulineproducerende bètacellen onder constante druk om te voldoen aan de stijgende vraag naar insuline. Met behulp van single-cell RNA-sequencing en geavanceerde computationele methoden volgden de onderzoekers individuele bètacellen terwijl muizen van slank via overgewicht naar ernstig obese gingen. Ze vonden dat een subset van onrijpe bètacellen toenam en geleidelijk hun gespecialiseerde insuline-identiteit verloor. Terwijl deze cellen stress ondervonden, namen merkers van eiwitvouwing en cellulaire schade toe, terwijl de insulineproductie afnam. Tegelijkertijd begonnen deze cellen hoge niveaus van CCK te produceren, een hormoon dat gewoonlijk met de darm geassocieerd wordt en dat spijsverteringscellen kan stimuleren om te groeien en te veranderen.
Van behulpzaam hormoon naar brandstof voor kanker
Om te testen of dit nieuw geproduceerde CCK slechts een bijproduct van stress was of een actieve motor van ziekte, creëerde het team muizen waarvan de bètacellen extra CCK produceerden, zelfs zonder obesitas. Deze dieren ontwikkelden pancreatische voorstadia van kanker en invasieve tumoren in vergelijkbare mate als obese muizen, ondanks een normaal gewicht en normale bloedsuikerwaarden. In tegenstelling daarmee daalde de tumorlast sterk wanneer CCK specifiek uit de alvleesklier van obese muizen werd verwijderd, ook al waren de dieren nog steeds zwaar en hadden ze hoge insulinespiegels. In verschillende muismodellen correleerden CCK-niveaus in de alvleesklier nauw met de hoeveelheid tumor, terwijl insulineniveaus de neiging hadden de tegenovergestelde richting op te bewegen. Dit wees op CCK — niet insuline — als het dominante hormoon dat in deze systemen obesitas met pancreaskanker verbindt.
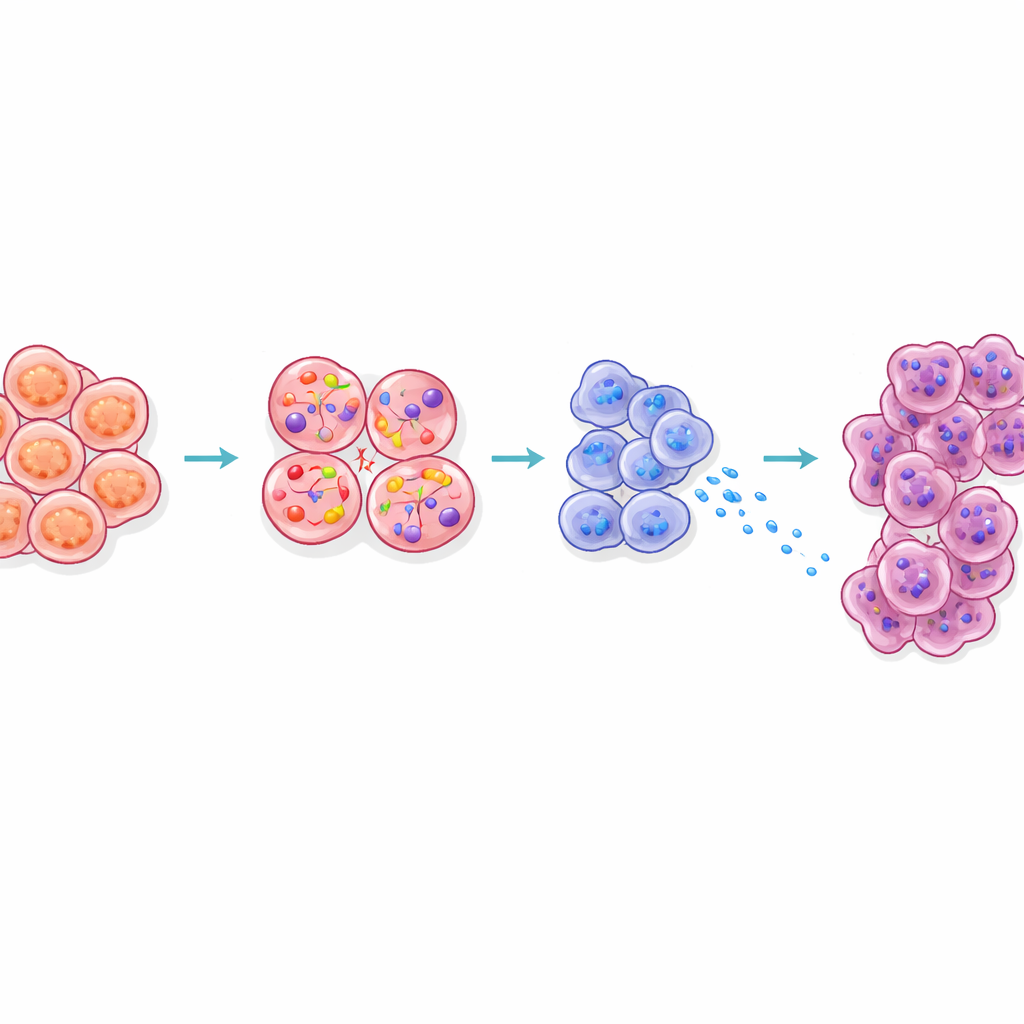
Hoe het signaal naburige cellen bereikt en klaarmaakt
De studie onderzocht ook hoe CCK uit bètacellen het omliggende weefsel hervormt. Acinaire cellen, die normaal spijsverteringsenzymen afscheiden, liggen direct naast de eilandjes in de alvleesklier. Bij obese muizen vertoonden acinaire cellen nabij eilandjes een stresshandtekening, produceerden ze meer spijsverteringsenzymen en eiwitten genaamd Reg, en schakelden ze over naar toestanden waarvan bekend is dat ze gemakkelijker getransformeerd kunnen worden tot kanker. Het blokkeren van CCK-signaalgeving bij obese muizen verminderde deze Reg-signalen. Drie-dimensionale beeldvorming toonde verder aan dat vroege precancereuze laesies bij obese dieren ongewoon dicht bij eilandjes ontstonden. Gezamenlijk suggereren deze bevindingen dat CCK, uitgestroomd van gestreste bètacellen, een “hete zone” rond eilandjes creëert waar spijsverteringscellen klaarstaan om in tumoren te veranderen.
Gedeelde patronen met menselijke diabetes en een sleutelchakelaar
Door muisgegevens te vergelijken met menselijk pancreasweefsel van personen met en zonder type 2 diabetes, vonden de auteurs opvallende parallellen: bètacellen van diabetische donoren vielen samen met dezelfde gestreste, minder rijpe toestanden die bij obese muizen werden gezien. Ze voerden vervolgens een regulatoir onderzoek uit om te achterhalen wat CCK in bètacellen activeert en identificeerden een stress-responsieve route gecentreerd op het eiwit cJun. Wanneer ze de upstream JNK–cJun-route blokkeerden in obese muizen of in bètacelachtige cellen in een cultuur, daalden de CCK-niveaus, en werd cJun in de buurt van een regulatorische regio van het CCK-gen aangetroffen. Dit suggereert dat chronische stress JNK–cJun activeert, wat op zijn beurt bètacellen doet omschakelen naar een CCK-producerende modus.
Wat dit betekent voor mensen met risico
Voor een niet-expert is de kernboodschap dat insulinecellen in de alvleesklier onder de belasting van obesitas en diabetes niet alleen falen — ze passen zich aan op een manier die per ongeluk naburige cellen aanmoedigt om kanker te vormen. Ze doen dit door CCK aan te zetten, een hormoon dat fungeert als groeisignaal en stressindicator voor naburige spijsverteringscellen, waardoor een vruchtbare bodem voor tumoren ontstaat. Omdat CCK uit de alvleesklier niet essentieel is voor het behoud van de bloedsuikerregulatie, zou het in principe mogelijk zijn om deze specifieke hormonale bron of zijn stress-geactiveerde schakelaar aan te pakken om het risico op pancreaskanker bij mensen met obesitas of type 2 diabetes te verminderen, zonder de algemene hormonale balans te ondermijnen. Het werk herformuleert pancreaskanker als een ziekte van verkeerd gerichte communicatie tussen de twee zijden van het orgaan en belicht nieuwe wegen voor vroege preventie.
Bronvermelding: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Trefwoorden: pancreaskanker, obesitas, bètacellen, cholecystokinine, type 2 diabetes