Clear Sky Science · nl
Vorming van een samenhangend SMG5-SMG6 PIN‑domein is essentieel voor NMD
Hoe cellen zich beschermen tegen foutieve boodschappen
Onze cellen lezen voortdurend genetische boodschappen (mRNA’s) om eiwitten te maken. Soms bevatten die boodschappen echter vroegtijdige stopcodons die tot verkorte, mogelijk schadelijke eiwitten zouden leiden. Het proces dat zulke foutieve boodschappen afbreekt heet nonsense‑mediated mRNA decay (NMD). Dit artikel onthult hoe twee sleutelproteïnen, SMG5 en SMG6, fysiek samenwerken om defecte boodschappen door te snijden, en verklaart daarmee een langbestaand raadsel over hoe cellulaire kwaliteitscontrole werkt.
De verborgen samenwerking ontdekken
Jarenlang wisten wetenschappers dat SMG6 RNA direct kan knippen, terwijl SMG5 werd beschouwd als katalytisch inactief en vooral een helper of steigerstructuur. Toch lieten experimenten in cellen iets raadselachtigs zien: SMG6 functioneerde niet goed zonder SMG5, en NMD viel stil als één van beide ontbrak. De auteurs gebruikten topniveau-structuurvoorspelling (AlphaFold), biochemische assays met gezuiverde eiwitten en genetische tests in menselijke cellijnen om deze tegenstrijdigheid op te lossen. Hun modellen voorspelden dat de staartregio’s van SMG5 en SMG6, de zogenaamde PIN‑domeinen, naast elkaar aannemen en samen een gezamenlijke structuur vormen. Deze samengestelde eenheid — aangeduid als een “cPIN” — werd voorgesteld als het werkelijke snijmechanisme in NMD. 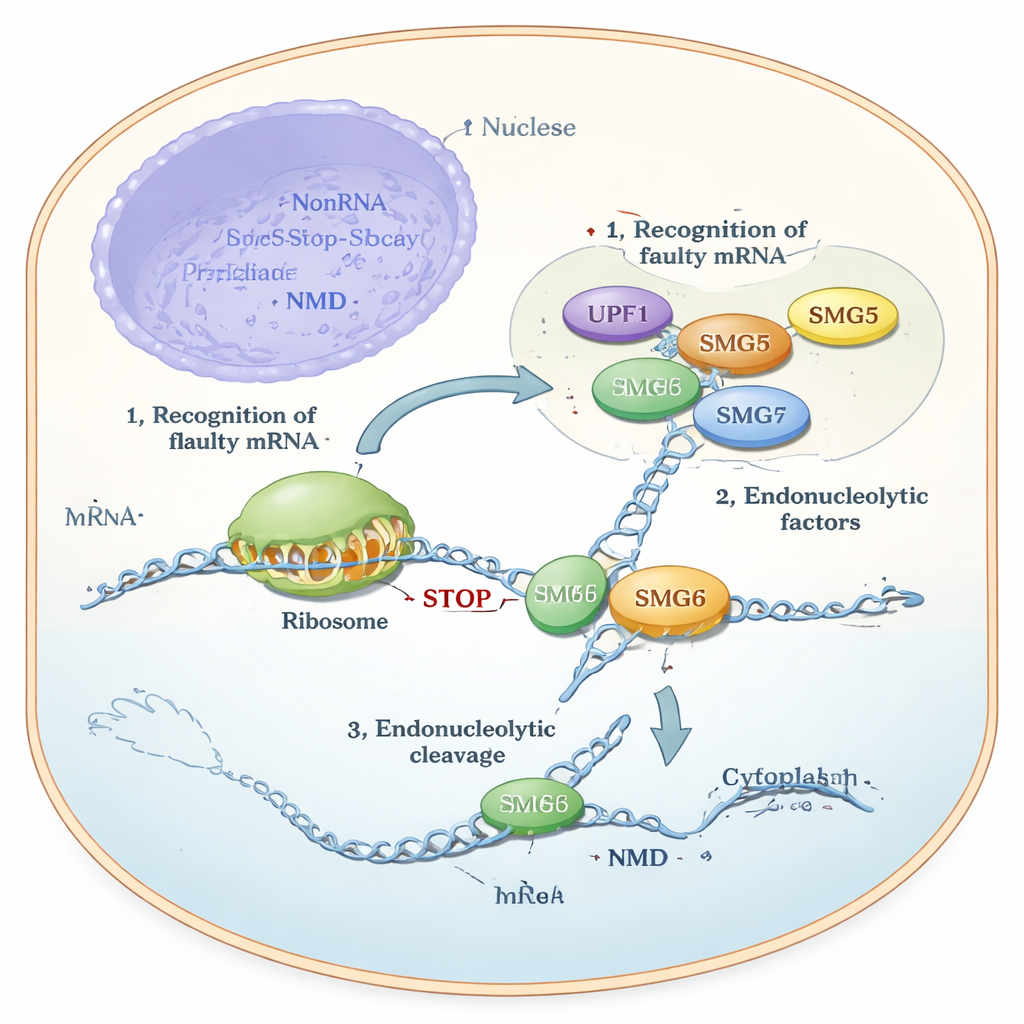
De moleculaire schaar in een reageerbuis herbouwen
Om de voorspelling te testen produceerde het team fragmenten van menselijke SMG5 en SMG6 in bacteriën en zuiverde die. Op zichzelf toonde SMG6 slechts zwakke knipactiviteit op een ontworpen RNA‑substraat, en SMG5 alleen vrijwel geen activiteit. Maar wanneer de twee fragmenten werden gemengd, nam de knipactiviteit sterk toe, zelfs onder omstandigheden waarbij verontreinigende enzymen onwaarschijnlijk waren. Hetzelfde effect trad op bij zowel lineaire als circulaire RNA‑testmoleculen, wat aangeeft dat de versterkte activiteit echt van het SMG5–SMG6‑paar afkomstig was. Chemische crosslinking en massaspectrometrie toonden verder aan dat de twee eiwitten dicht in contact komen, wat het idee van een directe, zij het mogelijk tijdelijke, samenwerking ondersteunt.
Het snijvlak compleet maken
De structurele modellen suggereerden precies hoe SMG5 SMG6 versterkt. SMG6 levert vier zure aminozuren die metalen ionen in het hart van het snijgebied vasthouden, zoals typisch is voor deze enzymfamilie. Verrassend genoeg plaatsten de modellen een extra zuur aminozuur van SMG5 direct naast deze residuen, waarmee het katalytische pocket effectief werd uitgebreid. Andere positief geladen residuen op SMG5 werden voorspeld het RNA‑backbone vast te grijpen en te helpen het voor knippen te positioneren. Wanneer de onderzoekers deze kritieke SMG5‑ of SMG6‑residuen muteerden, verloor het samengestelde complex veel van zijn knipkracht in vitro. Dezelfde mutaties konden NMD ook niet herstellen in genetisch gemanipuleerde menselijke cellen waar het normale eiwit was uitgeput, waarmee het structurele model sterk aan echte cellulaire functie werd gekoppeld. 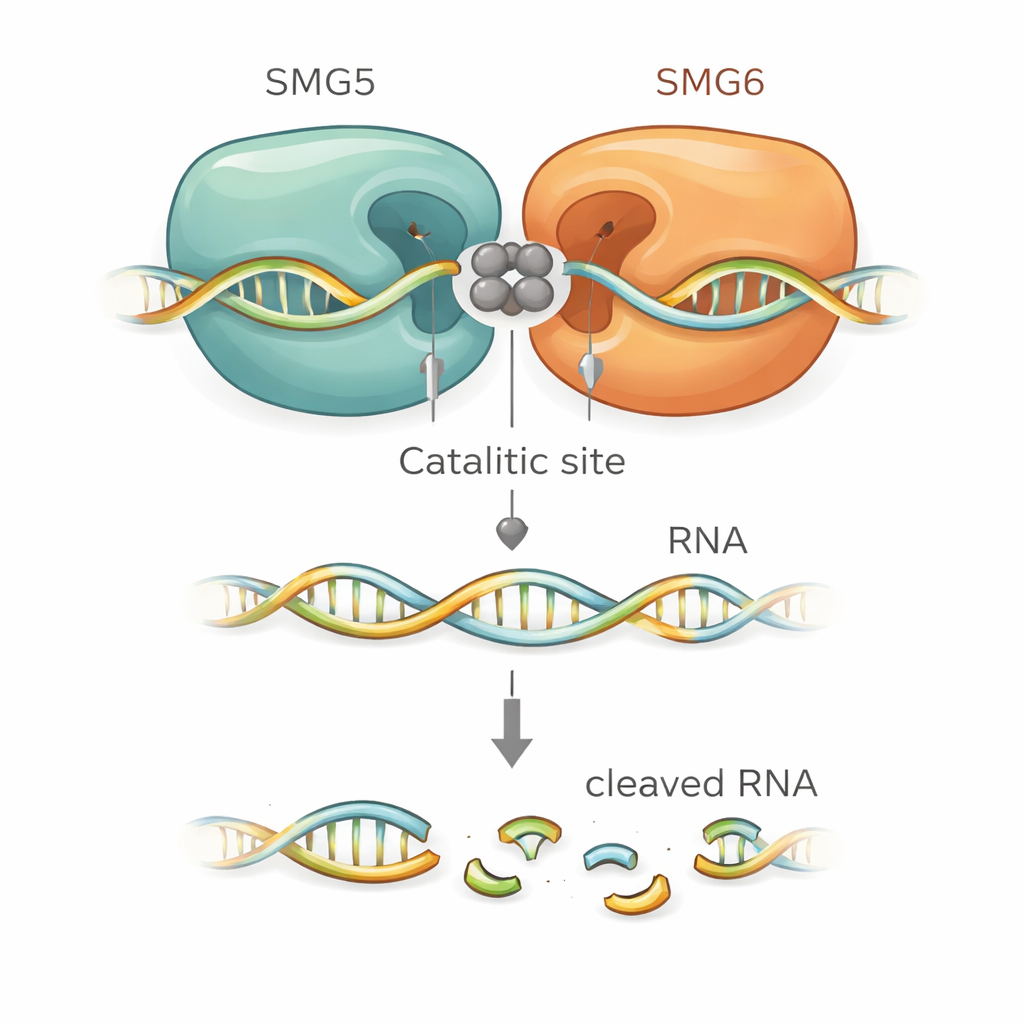
Aantonen dat beide partners essentieel zijn in cellen
Aangezien het volledig verwijderen van SMG5 of SMG6 dodelijk is voor cellen, gebruikte het team een “degron”‑systeem waarmee ze elk eiwit konden taggen zodat het snel met een klein molecuul kan worden afgebroken. Het combineren van deze snelle degradatie met RNA‑interferentie maakte vrijwel volledige verwijdering van SMG5, SMG6 of een centrale regulator genaamd UPF1 mogelijk. Genoom‑brede RNA‑sequencing toonde vervolgens wat er met NMD gebeurt wanneer elk factor wordt verwijderd. Het uitputten van SMG5 of UPF1 gaf vrijwel identieke veranderingen in cellulair RNA, waarbij foutieve, NMD‑gevoelige transcripties sterk ophoopten. Het verwijderen van SMG6 gaf een zeer vergelijkbaar, zij het iets milder, effect. Deze gegevens laten zien dat SMG5 en SMG6 geen optionele parallelle takken van de route zijn; ze werken samen met UPF1 als kerncomponenten van één hoofdafbraakpad.
Waarom dit belangrijk is voor cellulaire gezondheid
In eenvoudige bewoordingen toont de studie aan dat SMG5 en SMG6 in elkaar grijpen om één krachtig moleculair schaarpaar te vormen dat defecte genetische boodschappen doorsnijdt. SMG6 levert het grootste deel van het lemmet, maar SMG5 vult een ontbrekende rand aan en helpt het RNA op zijn plaats te houden, waardoor een zwakke knipper verandert in een efficiënte. Dit samengestelde “cPIN” verklaart waarom cellen beide eiwitten absoluut nodig hebben om hun RNA‑berichten schoon te houden. Door duidelijk te maken hoe de sleutelstap van NMD pas wordt geactiveerd wanneer foutieve boodschappen worden herkend, biedt het werk een helderder beeld van hoe cellen voorkomen dat toxische, verkorte eiwitten zich ophopen en hoe genexpressie nauwkeurig wordt bijgestuurd.
Bronvermelding: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Trefwoorden: nonsense-mediated mRNA decay, RNA-kwaliteitscontrole, SMG5 SMG6, mRNA‑bewaking, regulatie van genexpressie