Clear Sky Science · nl
Tumorcellen‑dorpen definiëren de onderlinge afhankelijkheid van tumor en micro‑omgeving bij leverkanker
Waarom kleine “dorpjes” binnen tumoren er toe doen
Kanker wordt vaak beschreven als een klomp meedogenloze cellen, maar deze studie naar leverkanker schetst een veel georganiseerder beeld. Binnen tumoren rangschikken de cellen zich in kleine “dorpjes” die samenwerken met nabije ondersteunende cellen, bloedvaten en immuuncellen. Begrijpen hoe die mini‑gemeenschappen ontstaan en functioneren kan verklaren waarom sommige tumoren agressiever zijn dan andere en aanwijzingen geven voor nieuwe manieren om ze te verstoren.
Tumoren cel voor cel bekijken in hun natuurlijke omgeving
De meeste moderne kankerstudies halen cellen uit de tumor en lezen hun genetische activiteit in een reageerbuis, waarmee cruciale informatie over de oorspronkelijke locatie van elke cel en haar buren verloren gaat. In dit werk combineerden onderzoekers twee krachtige benaderingen in monsters van zeven patiënten met primaire leverkanker. Ze gebruikten een hoog‑resolutie beeldvormingsplatform om RNA‑moleculen rechtstreeks in plakjes tumorweefsel te meten, waarbij meer dan 2,3 miljoen cellen in situ in kaart werden gebracht, en koppelden dit aan single‑cell RNA‑sequencing van dezelfde tumoren. Dat stelde hen in staat niet alleen te zien wat elke cel deed, maar ook waar ze zich binnen de tumor bevond en welke celtypen haar omringden. 
Ontdekking van onderscheidende “personality’s” van kankercellen
Door patronen in genactiviteit te analyseren, identificeerde het team een dozijn verschillende “toestanden” van maligne leverkankercellen. Sommige waren gericht op snelle deling, andere op herstel bij stress, reactie op immuunaanval, beweging en invasie van nabijgelegen weefsel, of het nabootsen van normale lever‑ of galwegcellen. Deze toestanden kwamen sterk overeen met patronen die in andere kankersoorten worden gezien, wat wijst op gemeenschappelijke thema’s in tumoren, maar met een lever‑specifieke inslag. Normale, niet‑kankerachtige epitheelcellen in dezelfde monsters toonden een veel beperktere reeks toestanden, wat benadrukt hoe ongewoon divers de tumorcellen waren geworden.
De buurt bepaalt wie de kankercellen worden
De onderzoekers vroegen zich vervolgens af hoe de lokale buurt deze kankerceltoestanden beïnvloedt. Voor elke maligne cel brachten ze alle naburige cellen in kaart binnen ongeveer de breedte van een mensenhaar en groeperden vergelijkbare buurtschappen in wat ze Spatial Dynamics Networks noemden. Sommige buurten zaten vol bloedvaten, andere werden gedomineerd door tumorcellen, terwijl weer andere rijk waren aan immuuncellen of fibroblasten (cellen die steunweefsel opbouwen). Kankercellen in een bepaalde toestand verschenen niet willekeurig. Bijvoorbeeld: cellen die een vormveranderingsproces ondergingen dat aan invasie gekoppeld is, bevonden zich vaak nabij dichtmazige bloedvatnetwerken, terwijl sterk delende cellen zich concentreerden in tumorrijke gebieden met weinig niet‑tumorcellen. Dit niet‑willekeurige patroon toont aan dat de micro‑omgeving en het gedrag van kankercellen nauw met elkaar verweven zijn.
Tumor “dorpjes” als samenwerkende ecosystemen
Om verder te gaan dan individuele cellen gebruikte het team een type deep‑learningmodel dat elke tumor behandelt als een graaf van verbonden cellen. Het model leerde zowel van de interne toestand van elke maligne cel als van het type buurt waarin ze zich bevond. Het clusteren van deze geleerde representaties onthulde acht terugkerende tumor‑“dorpjes.” Elk dorp mengde specifieke kankerceltoestanden met karakteristieke omgevingen—bijvoorbeeld: sommige dorpen combineerden bloedvatrijke gebieden met invasieve cellen, terwijl andere leken op “germinale centra” van snel delende tumorcellen. Toen de wetenschappers honderden extra leverkankerpatiënten in andere datasets bestudeerden, vonden ze dat patiënten wiens tumoren werden gedomineerd door bepaalde dorpen (gelabeld 3–8) doorgaans slechtere overleving hadden dan degenen met dorpen 1 en 2, wat suggereert dat de samenstelling van dorpen vastlegt hoe gevaarlijk het ecosysteem van een tumor is. 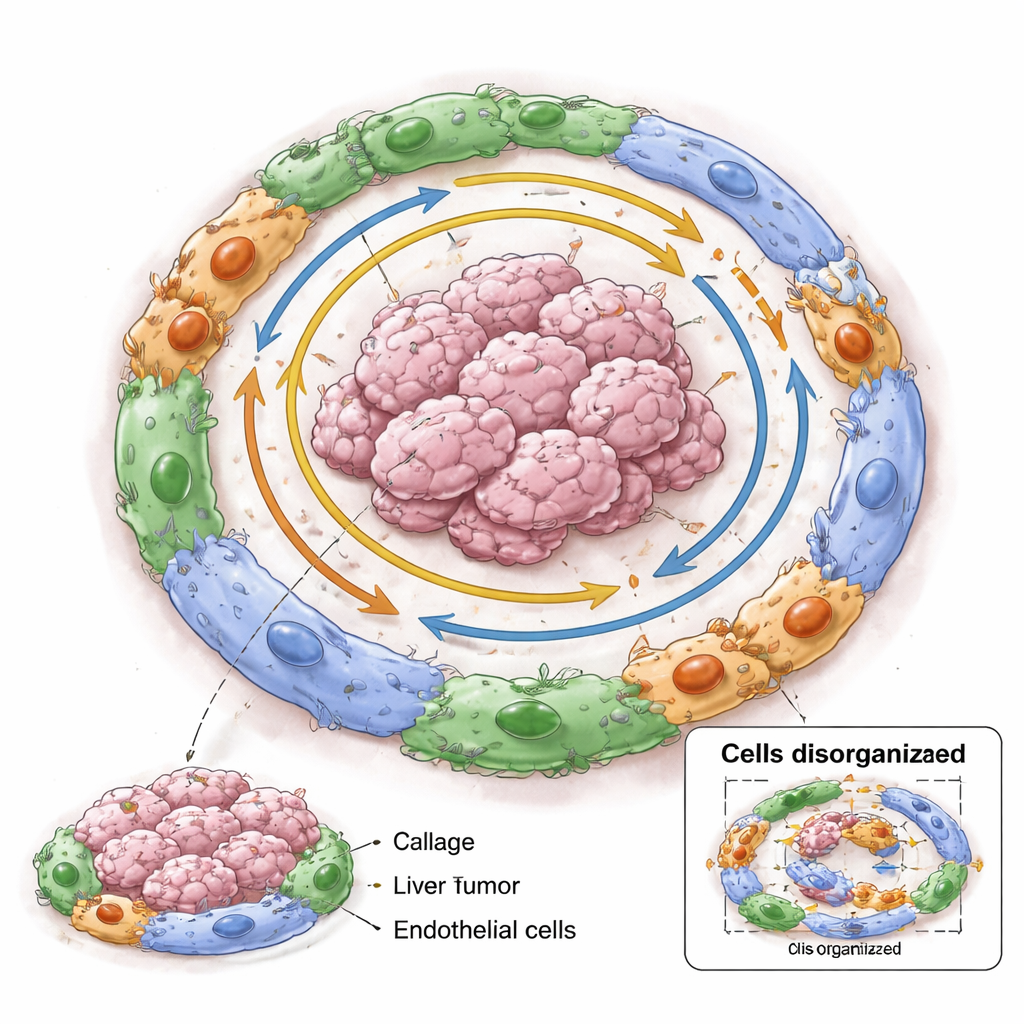
Moleculaire overeenkomsten tussen kankercellen en hun buren
Binnen elk dorp zochten de onderzoekers naar genparen—één actief in tumorcellen en één in nabije niet‑tumorcellen—die ruimtelijk samen op‑ en neer gingen. Deze “co‑afhankelijke” paren verschilden per dorp en verzwakten naarmate de afstand tussen cellen toenam, wat wijst op sterk lokaal begrensde moleculaire relaties. Een opvallend voorbeeld betrof een eiwit genaamd SPINK1, geproduceerd door tumorcellen, en collageenproducerende fibroblasten die bekendstaan als matrix cancer‑associated fibroblasts. SPINK1‑positieve tumorcellen werden vaak naast deze fibroblasten gevonden, en signalering tussen hen, waarschijnlijk via een bekende receptor genaamd EGFR, werd gekoppeld aan kenmerken van metastase. Toen de onderzoekers in hun modellen de buren van tumorcellen simuleerden te “schudden”, daalde het vermogen om dorpen correct te herkennen, vooral in dorpen rijk aan SPINK1‑gekoppelde interacties, wat suggereert dat deze moleculaire afspraken helpen de dorpsstructuur samen te houden.
Wat dit betekent voor patiënten
Voor een niet‑specialist is de kernboodschap dat levertumoren geen willekeurige hopen cellen zijn. Ze organiseren zich in kleine gemeenschappen—dorpjes—waar kankercellen en omliggende ondersteunende cellen van elkaar afhankelijk zijn om te groeien, uit te zaaien en behandeling te weerstaan. Sommige dorpstypen zijn verbonden met betere overleving, andere met slechtere, en elk kent zijn eigen reeks moleculaire afhankelijkheden. In de toekomst zouden therapieën niet alleen individuele kankercellen kunnen doden, maar specifieke dorpjes kunnen ontwrichten of uithongeren door de relaties tussen tumorcellen en hun buren te richten, waardoor de hele tumor mogelijk minder veerkrachtig wordt.
Bronvermelding: Liu, M., Hernandez, M.O., Castven, D. et al. Tumor cell villages define the co-dependency of tumor and microenvironment in liver cancer. Nat Commun 17, 1986 (2026). https://doi.org/10.1038/s41467-026-69797-z
Trefwoorden: leverkanker, tumormicro‑omgeving, ruimtelijke transcriptomica, intratumorale heterogeniteit, kankerceltoestanden