Clear Sky Science · nl
Niet-hydrolyseerbare acetyllysine-analogen om proteïneacetylatie in vitro en in cellen te bestuderen
Waarom kleine chemische labels op eiwitten ertoe doen
In elke cel worden eiwitten voortdurend aangepast met kleine chemische labels die werken als aan/uit-schakelaars of dimmers voor hun activiteit. Een van de belangrijkste van deze labels is acetylatie, die het gedrag van een eiwit kan veranderen zonder de onderliggende genetische code aan te passen. Precies begrijpen wat acetylatie op één specifieke plaats van één specifiek eiwit doet, is verrassend moeilijk gebleken, omdat cellen deze labels net zo snel weer kunnen verwijderen als ze ze aanbrengen. Deze studie introduceert een slim chemisch "plaatsvervanger" voor acetylatie die niet kan worden verwijderd, waardoor wetenschappers die schakelaars kunnen bevriezen en kunnen observeren wat er gebeurt.
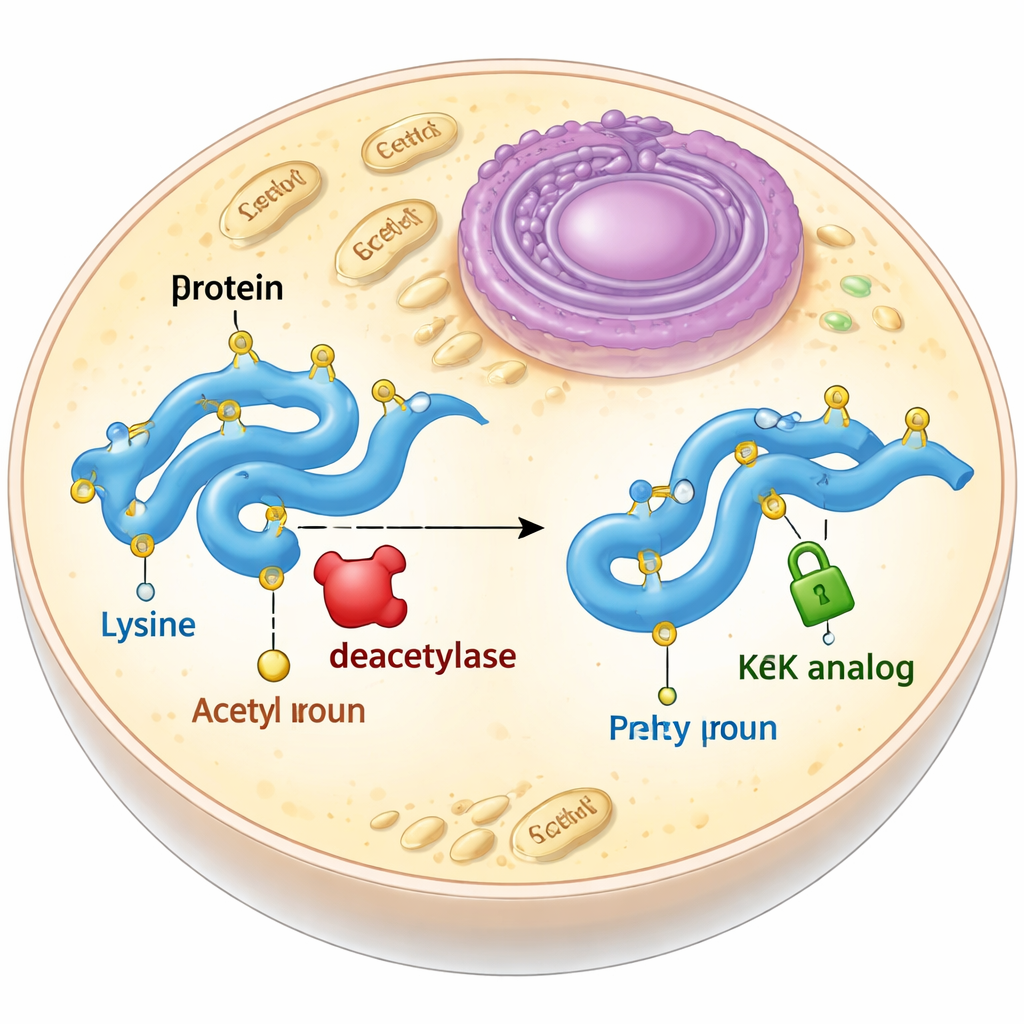
Een stabiele plaatsvervanger voor een vluchtig label
Acetylatie vindt meestal plaats op een bouwsteen van eiwitten die lysine heet. Wanneer een lysine geacetyleerd is, verliest hij zijn positieve lading en wordt zijn zijgroep iets langer. Biologen proberen dit vaak na te bootsen door lysine te muteren naar een ander aminozuur, glutamine, dat ongeladen maar korter is, of door echte acetyllysine toe te voegen met behulp van een uitgebreide genetische code. Beide benaderingen hebben nadelen: glutamine reproduceert niet volledig de vormveranderingen die acetylatie veroorzaakt, en echte acetyllysine wordt binnen de cel snel weer verwijderd door enzymen die deacetylases heten. De auteurs wilden acetyllysine-achtige verbindingen ontwerpen en testen die de juiste grootte en vorm behouden maar niet verwijderd kunnen worden.
Nieuwe chemische mimics testen op een modelproteïne
Het team richtte zich eerst op ubiquitine, een klein, goed bestudeerd eiwit dat zelf met veel verschillende labels wordt voorzien. Met geavanceerde genetische engineering plaatsten ze verschillende lysinevarianten op één positie in ubiquitine: natuurlijke acetyllysine, twee niet-verwijderbare analogen genaamd TFAcK en ketolysine (KeK), en gebruikelijke plaatsvervangers zoals glutamine, alanine en arginine. Vervolgens onderzochten ze hoe deze wijzigingen de vorm en functie van ubiquitine beïnvloedden. Hoge-resolutie NMR-metingen lieten zien dat acetyllysine, TFAcK en KeK bijna identieke structurele veranderingen veroorzaakten, vooral rond een centrale helix, terwijl glutamine en andere eenvoudige mutaties dat niet deden. Functionele tests met een enzym genaamd HDM2 toonden aan dat ubiquitine met acetyllysine, TFAcK of KeK zich vergelijkbaar gedroeg en verschilde van de glutamine-versie, wat benadrukt dat de lengte en omvang van de zijgroep—niet alleen de lading—cruciaal zijn.
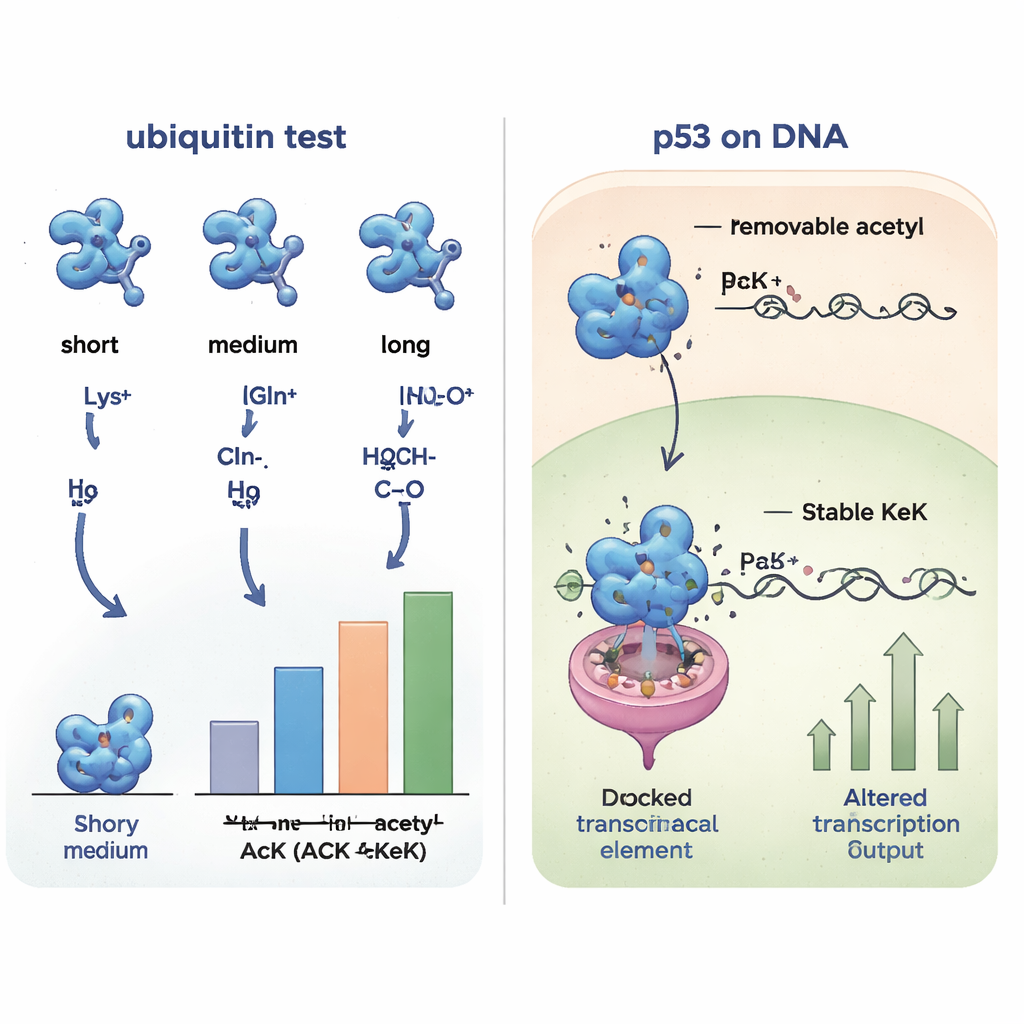
Eiwitpartners in de cel onderzoeken
Aangezien kleine structurele veranderingen kunnen bepalen met welke partners een eiwit interacteert, vergeleken de onderzoekers vervolgens hoe de verschillende ubiquitine-versies zich bonden aan andere eiwitten uit humane celextracten. Door bindingspartners te vissen en die te identificeren met massaspectrometrie, vonden ze dat ubiquitine dat acetyllysine, TFAcK of KeK bevatte zeer vergelijkbare interactiepatronen deelde, terwijl vormen met glutamine of alanine samen groepeerden en anders leken. Positief geladen varianten (lysine of arginine) vormden weer een andere groep. Deze systematische vergelijking toonde aan dat de niet-verwijderbare analogen TFAcK en vooral KeK zowel de structuur als het bindingsgedrag van echte acetylatie veel beter nabootsen dan de traditionele glutamine-substitutie.
Acetylatie vergrendelen op de tumorsuppressor p53
Om te zien of deze hulpmiddelen binnen levende cellen werken, richtten de auteurs zich op p53, een belangrijke tumorsuppressor die vaak de "bewaker van het genoom" wordt genoemd. Specifieke lysines in de DNA-bindende regio van p53 kunnen geacetyleerd worden, waardoor wordt gewijzigd welke genen het activeert, zoals genen die de celcyclus stoppen of apoptose induceren. Het team programmeerde menselijke cellen zo dat p53 acetyllysine, TFAcK of KeK op twee belangrijke lysineposities (120 en 164) zou opnemen, maar alleen wanneer het overeenkomstige niet-standaard aminozuur werd aangeleverd. Alle drie konden in p53 worden ingebouwd, maar gedetailleerde metingen toonden dat in cellen de acetyl- en TFAcK-groepen grotendeels werden verwijderd door deacetylases, terwijl KeK intact bleef. Bij het testen van de capaciteit van p53 om een rapportergen en het natuurlijke p21-gen te activeren, waren varianten met KeK op deze posities veel minder actief, wat overeenkomt met wat wordt verwacht wanneer acetylatie op die posities vergrendeld is, terwijl acetyllysine en TFAcK meer op normaal p53 leken omdat ze gedeacetyleerd waren.
Wat dit betekent voor het bestuderen van cellulaire beslissingen
Samengevat laat de studie zien dat KeK een getrouwe en niet-verwijderbare plaatsvervanger voor acetyllysine is: het reproduceert nauwgezet de structurele veranderingen, bindingsvoorkeuren en functionele consequenties van acetylatie, maar kan niet door cellulaire enzymen worden gewist. Voor niet-specialisten betekent dit dat onderzoekers nu een manier hebben om een normaal gesproken omkeerbare chemische schakel op één plaats van een eiwit te "bevriezen" en vervolgens te observeren hoe dat processen zoals genregulatie en celbestemming beïnvloedt. Dit zou het veel eenvoudiger moeten maken om de specifieke rollen van acetylatie te onderscheiden van die van andere overlappende modificaties, en kan uiteindelijk verduidelijken hoe verkeerd gereguleerde eiwitacetylatie bijdraagt aan ziekten zoals kanker.
Bronvermelding: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Trefwoorden: proteïneacetylatie, posttranslationele modificatie, ubiquitine, p53, uitbreiding van de genetische code