Clear Sky Science · nl
Dynamische transcriptomische herstructurering in getransplanteerde menselijke neurale voorlopercellen onthult mechanismen voor behoud van zicht in een rattenmodel van retinitis pigmentosa
Waarom het beschermen van afnemend zicht ertoe doet
Retinitis pigmentosa is een groep erfelijke aandoeningen die mensen geleidelijk het gezichtsvermogen ontnemen, vaak beginnend met nachtblindheid en voortschrijdend naar wettelijke blindheid. Omdat honderden verschillende genmutaties deze aandoening kunnen veroorzaken, is het lastig om elke mutatie afzonderlijk met gentherapie te behandelen. Deze studie onderzoekt een meer universele aanpak: het transplanteren van menselijke neurale voorlopercellen — onrijpe zenuwcellen gekweekt in het laboratorium — in het oog om de resterende lichtgevoelige cellen te beschermen. Inzicht in hoe deze getransplanteerde cellen zich precies gedragen en bijdragen aan het behoud van zicht kan toekomstige behandelingen vormgeven, niet alleen voor retinitis pigmentosa maar ook voor andere blindmakende aandoeningen.
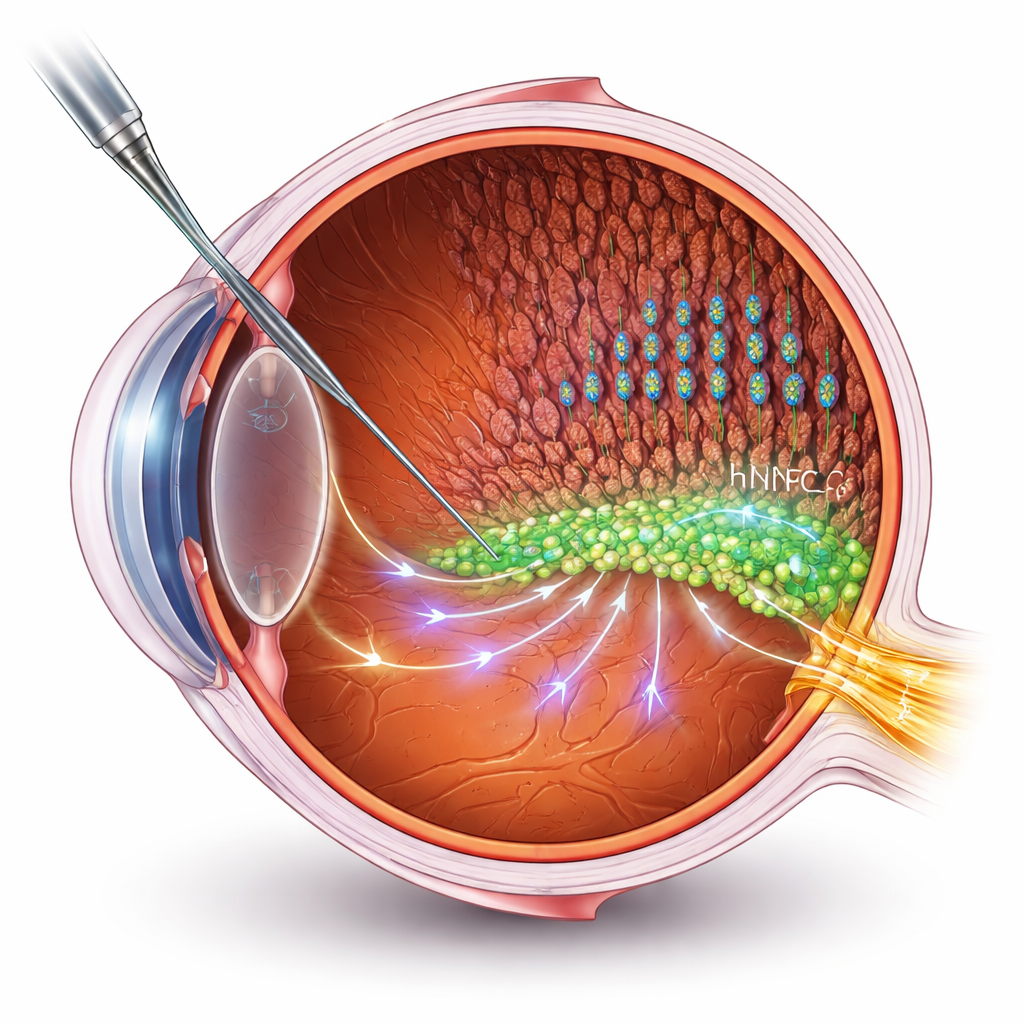
Cellen helpen in plaats van vervangen
Veel stamceltherapieën zijn gericht op het vervangen van dode of beschadigde cellen. Bij gevorderde retinale ziekten vormt het opbouwen van nieuwe verbindingen met de hersenen echter een grote technische uitdaging. Hier kiezen de onderzoekers een andere route: zij gebruiken menselijke neurale voorlopercellen (hNPCs) als “hulpcellen” die de eigen retinale cellen van de patiënt ondersteunen. Ze transplantaten hNPCs in de subretinale ruimte van een bekend rattenmodel van retinitis pigmentosa en maten vervolgens gezichtsfunctie met elektrische opnames en gedragsproeven. De behandelde ratten behielden betere visuele functie en meer intacte lagen van fotoreceptoren — de staafjes en kegeltjes die licht opvangen — dan onbehandelde dieren, ook al ging de degeneratie nog steeds langzaam door.
Hoe getransplanteerde cellen veranderen in het zieke oog
Om te zien wat er op moleculair niveau gebeurt, gebruikte het team single-cell RNA-sequencing, een techniek die in kaart brengt welke genen in duizenden individuele cellen worden geactiveerd. Ze volgden de getransplanteerde hNPCs op twee tijdstippen, ruwweg vroege en latere stadia na transplantatie. In plaats van te differentiëren tot nieuwe fotoreceptoren, rijpte het merendeel van de getransplanteerde cellen uit tot astrocytachtige ondersteunende cellen, terwijl een kleiner deel markerende eigenschappen van oligodendrocyten of onrijpe neuronen vertoonde. In de loop van de tijd stabiliseerden deze cellen, waarbij ze kenmerken aannamen die suggereren dat ze zijn afgestemd op overleving in een stressvolle, degenererende omgeving en op nauwe interactie met naburige retinale cellen.
Beschermende signalen, metabolisme en opruiming
De hNPCs produceerden een rijke mix van beschermende eiwitten, bekend als trofische factoren. Daartussen waren MANF en MYDGF, gekoppeld aan celoverleving, verminderde oxidatieve stress en gedempte ontsteking, evenals andere factoren zoals midkine en pleiotrophin die groei en migratie van neurale cellen ondersteunen. Deze moleculen leken zowel op de transplantatie zelf als op het omliggende netvlies te werken. Bij behandelde ratten vertoonden staafjes en kegeltjes genactiviteitspatronen die dichter bij gezonde controles lagen, met verbeterde ondersteuning voor visuele signalering en celonderhoud. De getransplanteerde cellen versterkten ook routes die betrokken zijn bij het opruimen van cellulair afval en het aanpassen van het metabolisme, wat suggereert dat ze helpen fotoreceptoren om te gaan met energiebehoeften en toxische bijproducten die zich tijdens de ziekte ophopen.
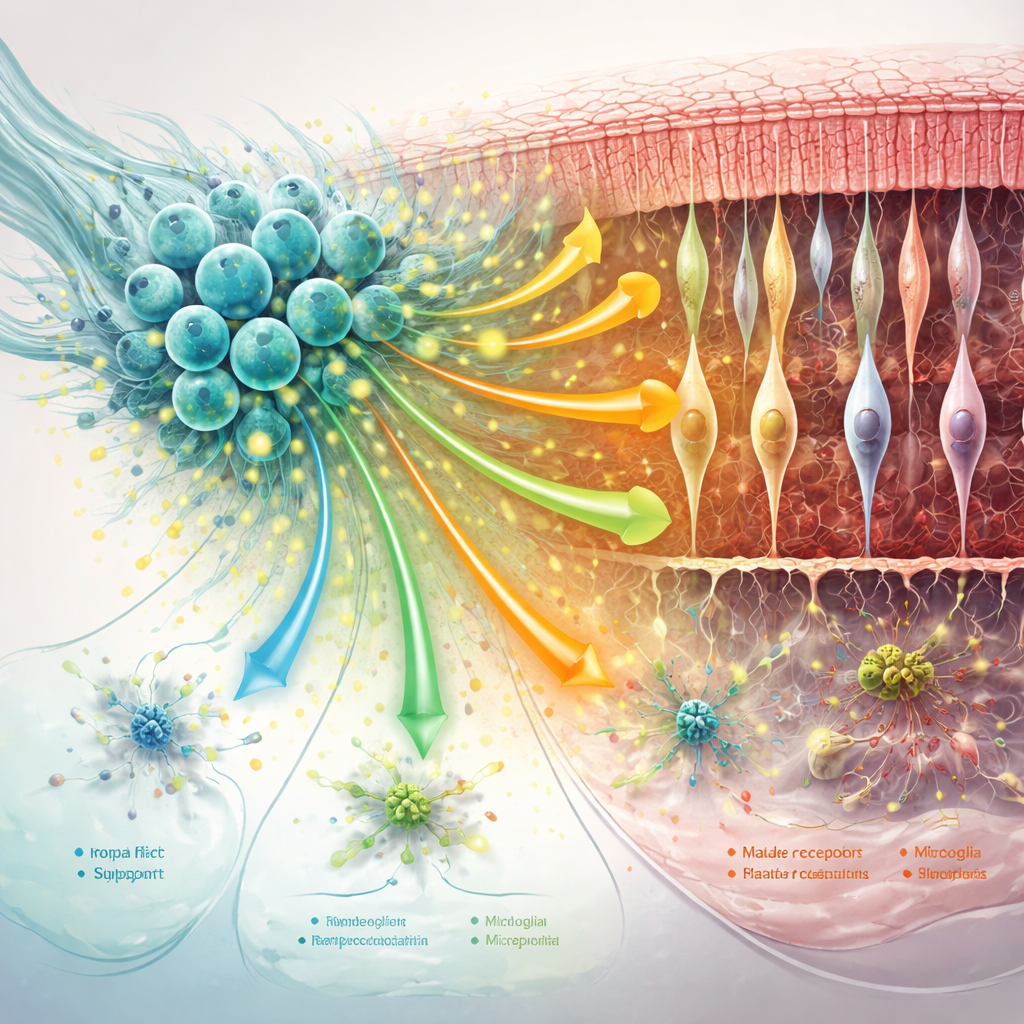
Kalmering van ondersteunende cellen en herschikking van de retinale omgeving
Het ondersteuningsnetwerk van het netvlies — Müller-glia, microglia en het omliggende eiwitmatrix — speelt een grote rol in het verergeren of vertragen van degeneratie. De studie vond dat hNPC-behandeling sleutelmarkeringen van schadelijke “reactieve” veranderingen in Müller-glia verminderde en microglia wegboostte van overdreven inflammatoire toestanden, vooral in eerdere tijdstippen. Tegelijkertijd werden communicatie-signalen die helpen synapsen te stabiliseren, cellen aan elkaar te laten hechten en het geraamte rond fotoreceptoren te onderhouden, versterkt. Naarmate de ziekte vorderde, vervaagden sommige van deze voordelen: de algehele cel-tot-celcommunicatie verzwakte, maakten bepaalde beschermende routes — waaronder MANF-gerelateerde signalering — een achteruitgang door, en namen ondersteunende cellen meer stress- en immuungerichte profielen aan.
Wat dit betekent voor toekomstige oogtherapieën
Voor niet-specialisten is de kernboodschap dat getransplanteerde menselijke neurale voorlopercellen kunnen fungeren als plaatselijke “eerste hulpverleners” in een degenererend netvlies. Ze bouwen het netvlies niet vanaf nul opnieuw op, maar ze geven beschermende moleculen af, passen het metabolisme aan, kalmeren schadelijke ontstekingen en helpen de lokale structuur intact te houden — allemaal factoren die het verlies van zicht vertragen. Deze beschermende werking neemt echter na verloop van tijd af naarmate de omgeving vijandiger wordt en de dialoog tussen transplantaat en gastheercellen verzwakt. De auteurs suggereren dat het versterken van sleutelcomponenten zoals MANF en het verbeteren van de gezondheid van het gastheer-netvlies — mogelijk via genetische engineering van het transplantaat of combinatietherapieën — essentieel kan zijn om een tijdelijke verlichting om te zetten in langdurig behoud van zicht.
Bronvermelding: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Trefwoorden: retinitis pigmentosa, stamceltherapie, retinale degeneratie, neuroprotectie, single-cell RNA-sequencing