Clear Sky Science · nl
Beperkingen van opeenvolgend klonen bij zoogdieren
Waarom het kopiëren van zoogdieren niet zo eenvoudig is als het lijkt
Al decennia boeit het idee om dieren tot in hun DNA te kopiëren het publiek, van schaap Dolly tot dromen over het terugbrengen van uitgestorven soorten. Maar kunnen zoogdieren zichzelf echt in stand houden door uitsluitend te klonen, generatie na generatie, zoals sommige planten en eenvoudige dieren doen? Deze studie volgde gedurende bijna 20 jaar één muizenlijn die volledig door klonen was voortgebracht om dat te onderzoeken. De resultaten laten zien waarom de natuur, ondanks onze technische vooruitgang, nog steeds sterk leunt op seks om zoogdieren op de lange termijn gezond te houden.
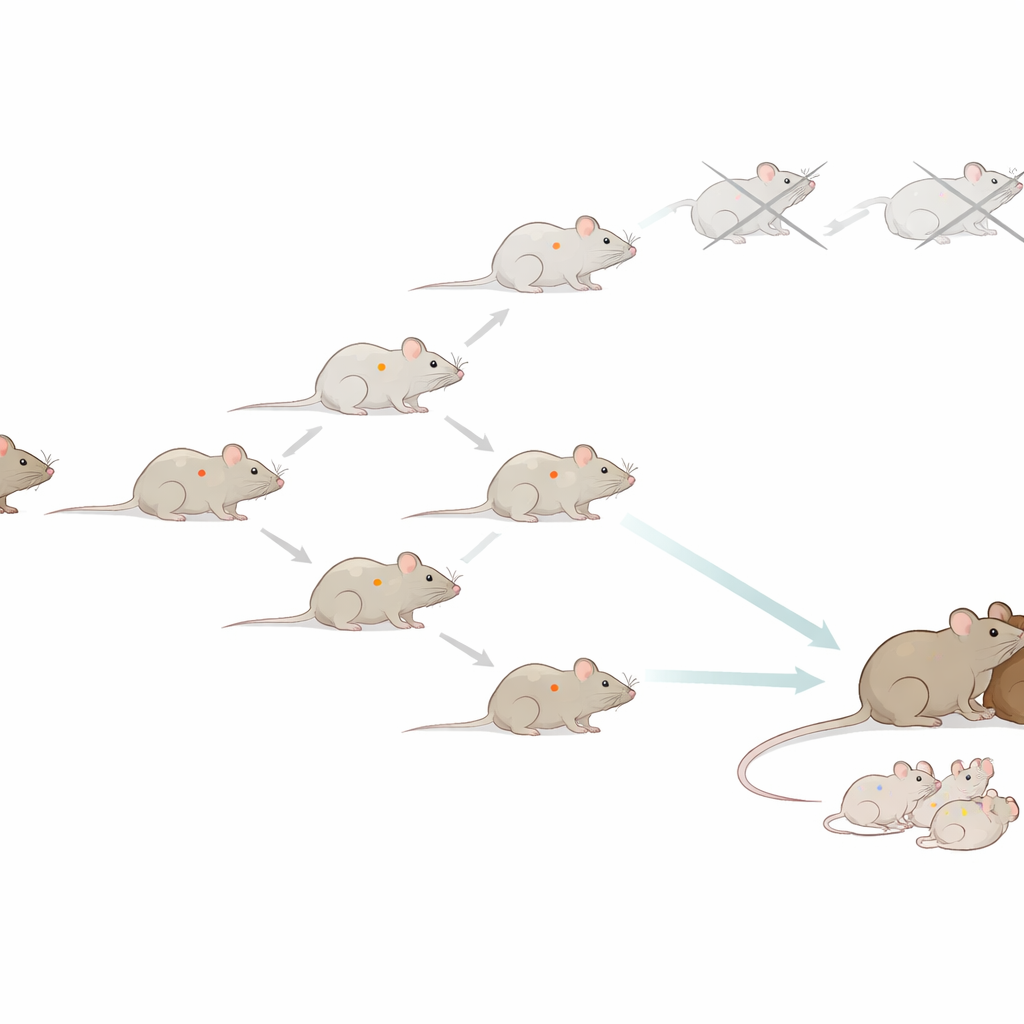
Een muizenlijn twintig jaar lang gevolgd
De onderzoekers begonnen met één vrouwelijke muis en gebruikten haar lichaamscellen om een gekloonde muis te maken. Toen die eerste kloon opgroeide, namen ze cellen daarvan om de volgende kloon te maken, en herhaalden dit proces steeds opnieuw. In totaal probeerden ze meer dan 30.000 kerntransferprocedures en produceerden ze meer dan 1.200 gekloonde dieren, waarmee ze 58 generaties bereikten vanaf de oorspronkelijke donor. Veel van deze muizen zagen er normaal uit en gedroegen zich ook zo, met levensduur rond twee jaar en vergelijkbaar gewicht. In het begin verbeterde het succespercentage van het klonen zelfs per generatie, wat suggereerde dat opeenvolgend klonen van zoogdieren op lange termijn praktisch zou kunnen zijn.
Gezonde lichamen, maar verborgen schade
Aan de oppervlakte leken de gekloonde muizen in orde. Hun interne organen en vooral hun placenta’s vertoonden de bekende eigenaardigheden van kloonexperimenten, zoals grotere placenta’s dan bij natuurlijk verwekte muizen, maar deze afwijkingen werden niet erger met elke generatie. Het team onderzocht ook hoe goed embryo’s zich in het lab ontwikkelden en keek naar patronen van chemische markeringen op de eiwitverpakking van DNA—eigenschappen die bij klonen vaak misgaan. Vroege embryo’s van laat-gene generatiekloons leken veel op die van de eerste gekloonde generatie. Dit suggereerde dat de bekende "herprogrammerings"-problemen van klonen niet gestaag opstapelden in de tijd.
Mutaties sluipen erin bij elke kopie
Het echte verhaal kwam aan het licht toen de wetenschappers de genomen van muizen uit verschillende kloongenaraties sequentieerden. Bij elke ronde van kopiëren verschenen nieuwe veranderingen in het DNA: gemiddeld ongeveer 70 enkellettermutaties en één tot twee structurele afwijkingen per generatie, waaronder grote herschikkingen en verlies van chromosomen. Veel van deze veranderingen leken op natuurlijke mutaties die bij gewone voortplanting voorkomen, maar het belangrijke verschil is dat bij klonen geen herschikking van chromosomen plaatsvindt door paring die schadelijke varianten kan uitfilteren. Na verloop van tijd, met name na ongeveer de 25e generatie, begonnen schadelijke mutaties—zoals verlies van een gehele X-chromosoom of breuken en verwisselingen tussen chromosomen—zich op te stapelen. Het aandeel mutaties dat waarschijnlijk belangrijke genen verstoort verdubbelde bijna in latere generaties.
Voedeilcellen onthullen het breekpunt
Om te zien hoe deze verborgen schade de voortplanting beïnvloedde, richtte het team zich op eicellen van laat-gene generatie gekloonde vrouwtjes. Wanneer deze eieren werden gestimuleerd om zich zonder sperma te ontwikkelen, groeide vrijwel geen enkel ei uit tot een gezond vroeg-embryo, wat aangeeft dat veel eieren dodelijke combinaties van mutaties droegen. Bevruchting met sperma van normale mannetjes verbeterde de ontwikkeling enigszins, maar het slagingspercentage daalde nog steeds scherp in latere generaties. Experimenten waarbij de kernen en het omringende cytoplasma werden verwisseld tussen eieren van normale en laat-gene generatiekloons toonden aan dat zowel het genetische materiaal als het eicelcytoplasma waren aangetast. Uiteindelijk, rond de 58e generatie, stierven alle gekloonde nakomelingen kort na de geboorte en kon de kloonlijn niet worden voortgezet.
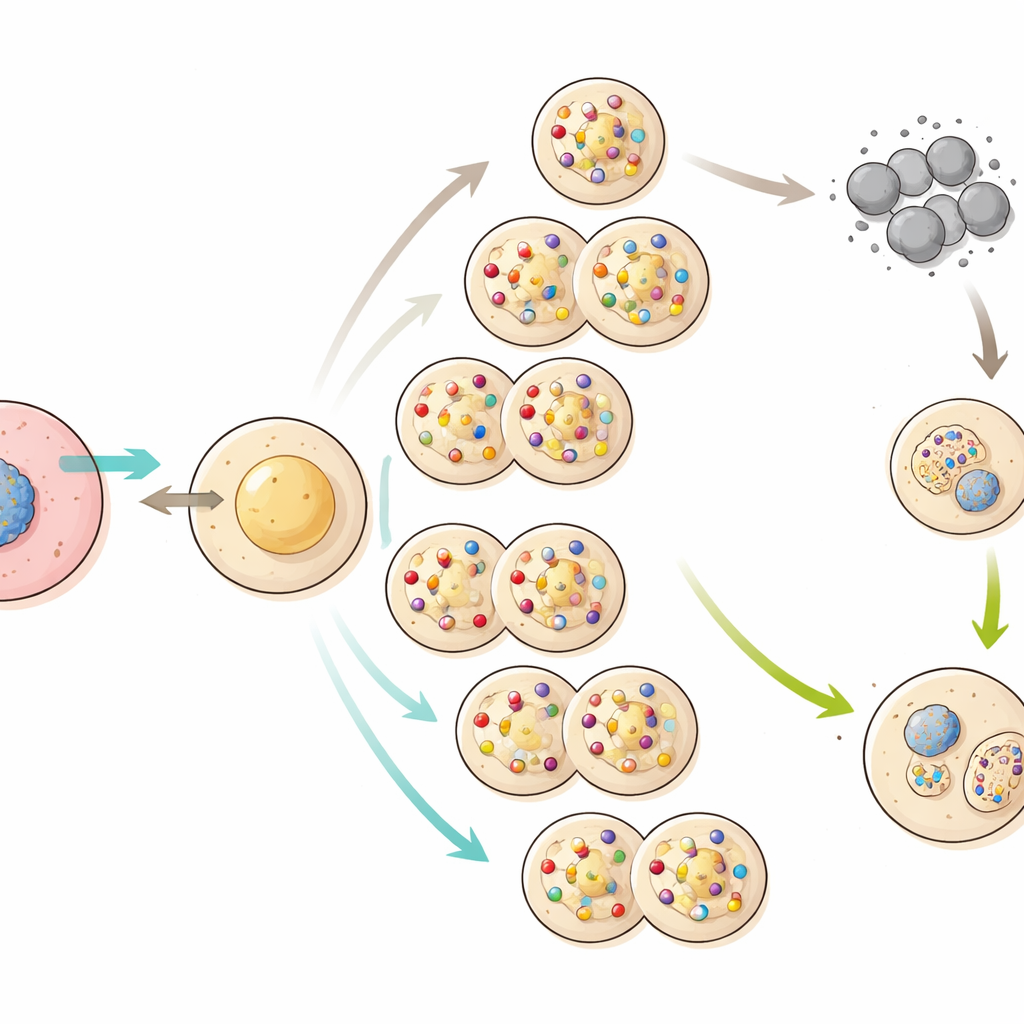
Seksuele voortplanting als reparatiesysteem
Toen de wetenschappers laat-gene generatie gekloonde muizen natuurlijk lieten paren met normale mannetjes, verscheen een ander patroon. Hoewel deze gekloonde moeders kleine worpen hadden, waren sommige van hun nakomelingen—en vooral hun kleinkinderen—veel gezonder. De placenta’s van de volgende generatie slonken weer richting normaal formaat en de algemene ontwikkeling verbeterde. Dit suggereert dat het mengen en herschikken van chromosomen tijdens de vorming van eicellen en zaadcellen, gevolgd door bevruchting, beschadigende combinaties van mutaties kan uit elkaar halen en veel van de ergste veranderingen kan wegfilteren. Met andere woorden: seks functioneerde als een ingebouwd schoonmaaksysteem dat puur klonen mist.
Wat dit betekent voor de toekomst van klonen
Door zorgvuldig één gekloonde muizenlijn over 57 succesvolle generaties te volgen, toont dit werk aan dat zoogdieren niet uitsluitend op klonen kunnen vertrouwen om een lijn permanent in stand te houden. Zichtbare gezondheid en normale levensduur kunnen een langzaam genetisch verval maskeren, terwijl mutaties zich ongemerkt opstapelen totdat de voortplanting faalt. Hoewel klonen een krachtig hulpmiddel blijft—voor het redden van bedreigde dieren, het vermeerderen van waardevol vee of het bewaren van genetische hulpbronnen—is het onwaarschijnlijk dat het seksuele voortplanting op lange termijn vervangt als overlevingsstrategie voor zoogdieren. De studie levert sterke experimentele ondersteuning voor het idee dat seks bij complexe dieren niet alleen gaat om het maken van nakomelingen, maar essentieel is voor het onderhoud van het genoom.
Bronvermelding: Wakayama, S., Ito, D., Inoue, R. et al. Limitations of serial cloning in mammals. Nat Commun 17, 2495 (2026). https://doi.org/10.1038/s41467-026-69765-7
Trefwoorden: dierklonen, genetische mutaties, muizenreproductie, <keyword>evolutie van seks