Clear Sky Science · nl
TCL1A bemiddelt DNA-methyleringsdefecten bij terugkerende hydatidiforme mola met pathogene varianten in NLRP7
Waarom dit belangrijk is voor de gezondheid van vrouwen
Sommige zwangerschappen gaan al heel vroeg mis en veranderen in een massa abnormaal placentaire weefsel in plaats van een zich ontwikkelend kind. Deze aandoening, een hydatidiforme mola genoemd, kan bij sommige vrouwen terugkeren en soms zelfs overgaan in kanker. Deze studie onderzoekt één belangrijke genetische oorzaak van deze zeldzame maar ernstige zwangerschappen en onthult hoe één defecte bewaking in de eicel de chemische “labels” die gezonde ontwikkeling sturen, kan verstoren.
Een zwangerschapsprobleem dat zijn oorsprong vindt in de eicel
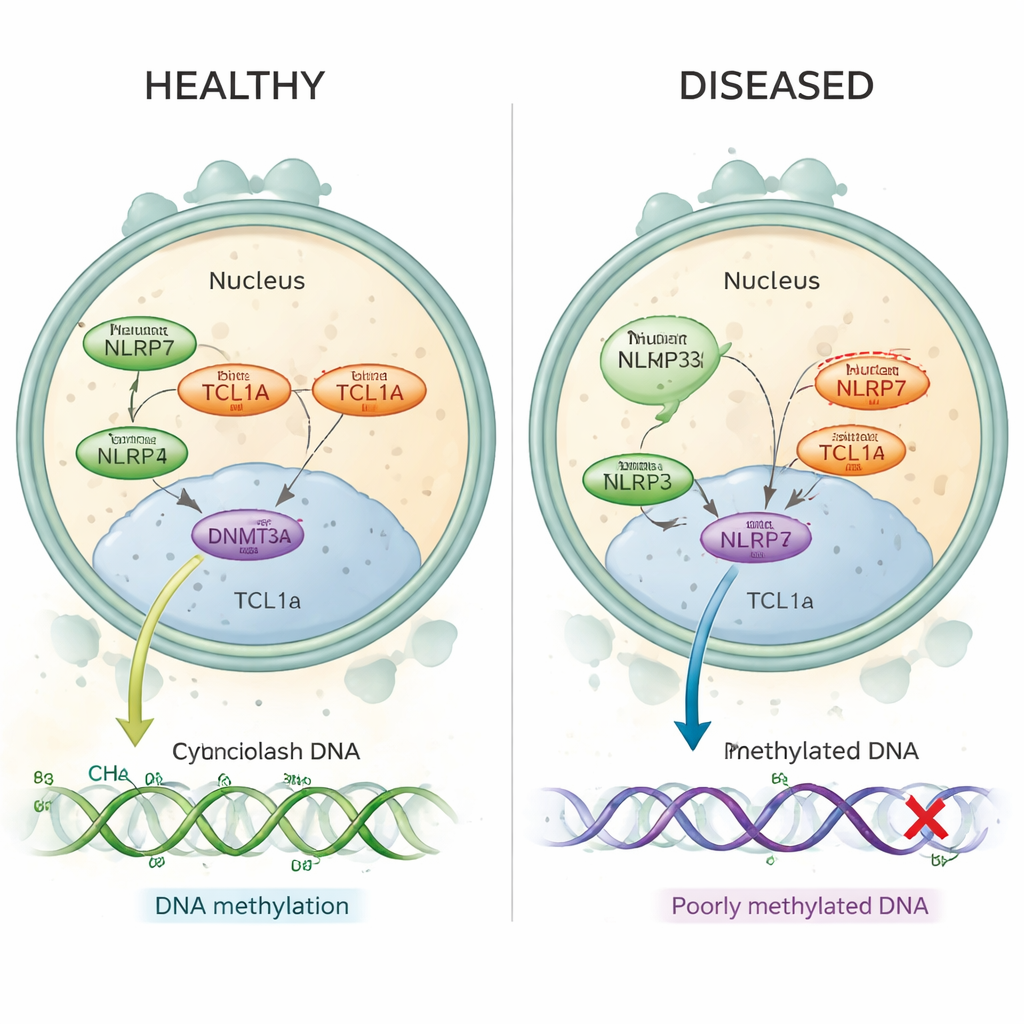
Terugkerende hydatidiforme mola is een aandoening waarbij vrouwen herhaaldelijk mola-zwangerschappen doormaken, vaak zonder normale zwangerschappen ertussen. Veel van deze gevallen blijken te worden veroorzaakt door schadelijke veranderingen in een gen dat NLRP7 heet en actief is in de eicel vóór en kort na bevruchting. Bij deze vrouwen ontbreken op belangrijke DNA-streken, die moederlijke “imprints” zouden moeten dragen, de normale methylatie‑merken — kleine chemische etiketten die helpen genen op het juiste moment aan of uit te zetten. Tot nu toe begrepen wetenschappers niet hoe een eiwit dat in het cytoplasma van de eicel zit, zoals NLRP7, methylatie kan controleren die plaatsvindt op het in de kern verpakte DNA.
Een ontbrekende partner vinden
Om dit raadsel op te lossen onderzochten de onderzoekers weggegooide menselijke eicellen en zeer vroege embryo’s van vruchtbaarheidsklinieken. Ze haalden NLRP7 en zijn bekende partners uit deze cellen en identificeerden andere eiwitten die ermee meeliften. Eén eiwit viel op: TCL1A, dat al bekend is uit bloedkankers als een eiwit dat de kern kan binnengaan en de DNA-methylerende enzymen DNMT3A en DNMT3B kan verstoren. TCL1A is ongewoon veel aanwezig in menselijke eicellen, wat suggereert dat het daar een belangrijke rol speelt. Gedetailleerde interactietests toonden aan dat TCL1A strak en specifiek bindt aan NLRP7, maar niet aan nauwe verwanten, en dat dit complex is ingebed in een groter eicelspecifiek structuur, het subcorticale maternale complex.
De moleculaire omhelzing zien
Het team gebruikte vervolgens cryo-elektronenmicroscopie om de driedimensionale structuur van het NLRP7–TCL1A-complex te visualiseren. Ze ontdekten dat twee NLRP7-moleculen een paar vormen en dat elk van hen een TCL1A-dimeer vastgrijpt langs een gebogen oppervlak van herhaalde motieven. Deze rangschikking verklaart waarom veel ziekteveroorzakende veranderingen in NLRP7 langs dat oppervlak geconcentreerd zijn: wijziging van sleutelcontactpunten verzwakt of vernietigt de omhelzing met TCL1A. Toen de onderzoekers meer dan 50 bekende patiëntvarianten in cellen nabootsten, destabiliseerden de meeste versies die aan terugkerende mola's gekoppeld zijn NLRP7 of verminderden ze sterk het vermogen ervan om aan TCL1A te binden.
Hoe verplaatste eiwitten DNA‑merken ontregelen
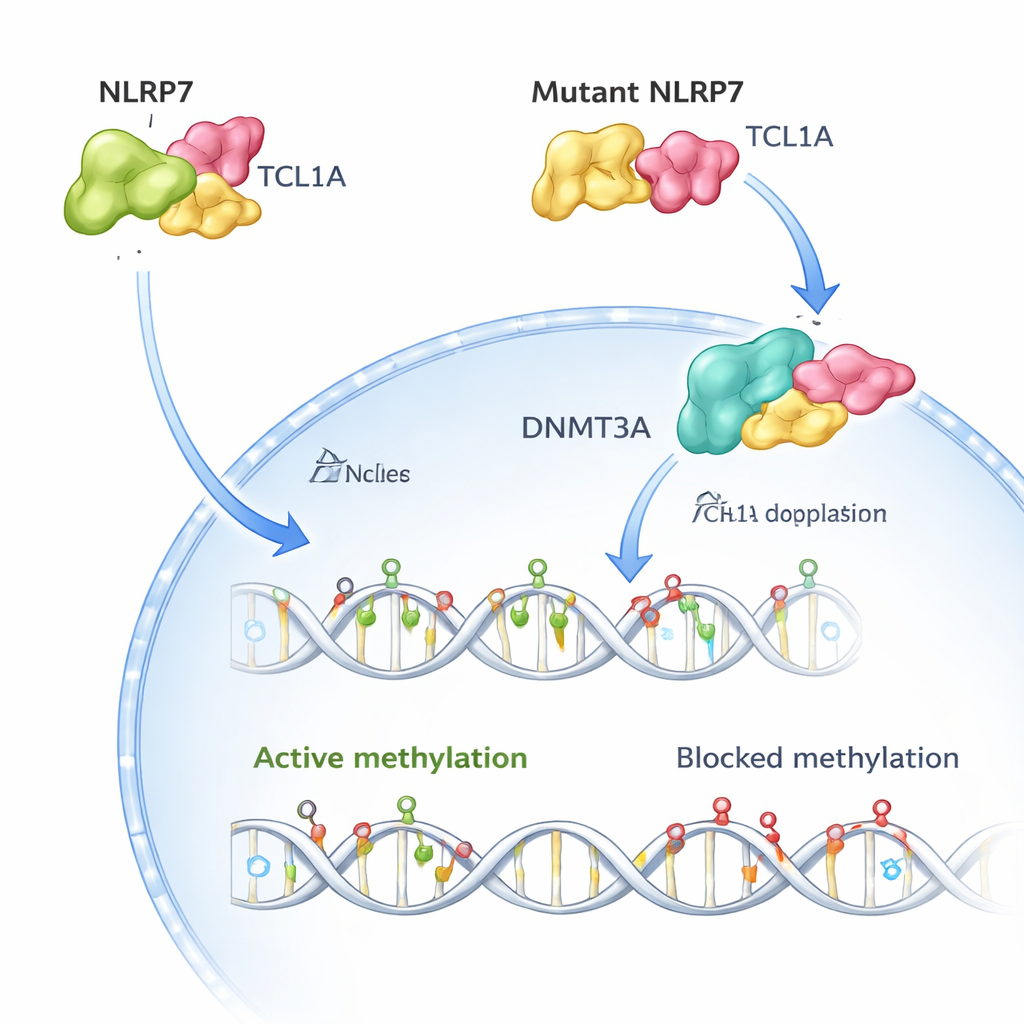
In gezonde menselijke eicellen bevinden zowel NLRP7 als TCL1A zich hoofdzakelijk in het cytoplasma, waarbij slechts een kleine hoeveelheid TCL1A de kern bereikt. De auteurs tonen aan dat NLRP7 effectief als poortwachter fungeert: wanneer het TCL1A kan vasthouden, blijft TCL1A buiten de kern. Wanneer NLRP7 gemuteerd is en niet goed meer kan binden, lekt TCL1A de kern in. Daar hecht het zich aan DNMT3A, het belangrijkste enzym dat nieuwe methylatie‑merken in eicellen aanbrengt, en dempt het diens activiteit. In stamcelmodellen die normaal methylatie winnen tijdens rijping, veroorzaakte overexpressie van TCL1A een dramatisch verlies van methylatie over het genoom, terwijl gelijktijdige expressie van NLRP7 dit defect gedeeltelijk herstelde. Gezamenlijk ondersteunen deze bevindingen een eenvoudig beeld: normaal houdt NLRP7 een methylatie-"rem" (TCL1A) vergrendeld in het cytoplasma zodat DNMT3A het DNA correct kan labelen; defect NLRP7 laat die rem in de kern glippen en blokkeert het proces.
Van mechanisme naar diagnose
Buiten het verklaren hoe terugkerende mola-zwangerschappen ontstaan, suggereert de studie een praktische manier om te beoordelen of een nieuw ontdekte NLRP7-verandering bij een patiënt daadwerkelijk schadelijk is. De auteurs vergelijken drie benaderingen — laboratoriumtesten van NLRP7–TCL1A-binding, computergebaseerde voorspellingen en standaard genetische scoreringsinstrumenten — en tonen aan dat verlies van TCL1A-binding sterk overeenkomt met varianten die ziekte veroorzaken. Ze ontdekken ook een eerder niet herkende schadelijke variant, L766R, in families met terugkerende mola’s, en bevestigen dat deze zowel het eiwit verzwakt als TCL1A naar de kern verkeerd leidt.
Wat dit in eenvoudige bewoordingen betekent
Dit werk onthult een moleculaire kettingreactie achter een zeldzame maar verwoestende zwangerschapsstoornis. In wezen hebben eicellen van getroffen vrouwen een kapot "lichaamsbeschermer"‑eiwit, NLRP7, dat er niet in slaagt zijn partner TCL1A buiten de kern te houden. Eenmaal binnen verstoort TCL1A het enzym dat essentiële chemische labels op DNA schrijft. Zonder die labels groeit de vroege placenta abnormaal en kan er geen baby ontstaan. Door deze route stap voor stap te traceren, verduidelijkt de studie waarom bepaalde genetische veranderingen bij moeders zwangerschappen herhaaldelijk kunnen saboteren en wijst ze op nauwkeurigere genetische counseling en diagnostiek voor vrouwen met terugkerende hydatidiforme mola’s.
Bronvermelding: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Trefwoorden: DNA-methylering, terugkerende hydatidiforme mola, NLRP7, TCL1A, genomische imprinting