Clear Sky Science · nl
GCN5 drijft de MASLD‑progressie aan via LXRα/SREBP1c‑signalering‑gemedieerde de novo lipogenese
Waarom dit leververhaal ertoe doet
Metabool disfunctie‑geassocieerde steatotische leverziekte (MASLD), voorheen non‑alcoholische vette leverziekte genoemd, treft nu ongeveer één op de vier mensen wereldwijd. Het ontwikkelt zich vaak sluipend, maar kan voortschrijden naar littekenvorming, leverkanker en ernstige metabole problemen. Deze studie onthult een moleknare “volume‑knop” die de schadelijke vetophoping in de lever stimuleert en laat zien hoe het terugdraaien ervan zowel de lever kan beschermen als bestaande hartmedicatie mogelijk veiliger kan maken.
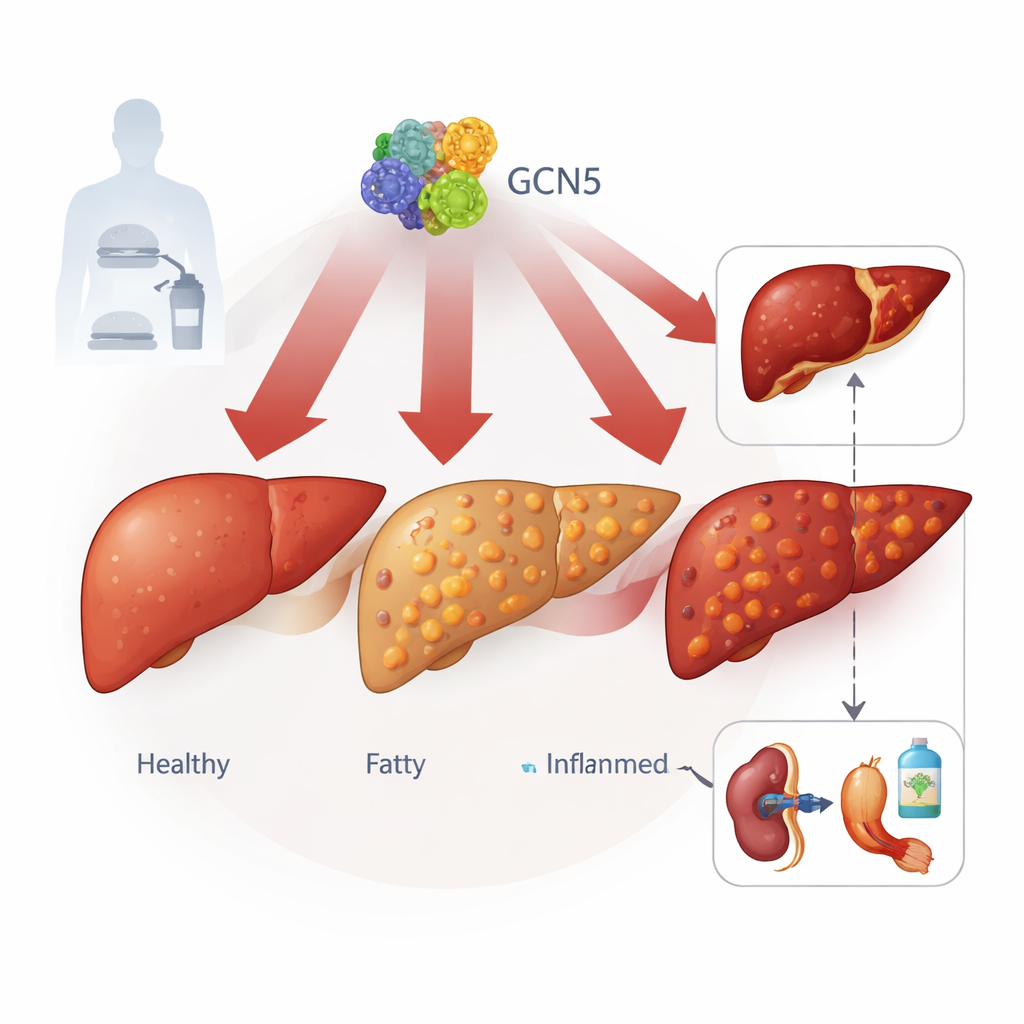
Een verborgen schakel in levercellen
De auteurs richten zich op een eiwit genaamd GCN5, vooral bekend als regulator van hoe strak DNA is verpakt. Door leverweefsel van meer dan 100 personen te bestuderen, variërend van gezond tot ernstige MASLD, en verschillende muismodellen van door dieet geïnduceerde vette lever, vonden ze dat GCN5‑niveaus in levercellen gestaag stijgen naarmate de ziekte verergert. Een nauw verwant eiwit, PCAF, toonde dit patroon niet, wat suggereert dat GCN5 een speciale rol speelt. Hoog GCN5 correleerde met meer levervet, hogere bloedlipiden en sterkere tekenen van leverbeschadiging, waarmee deze moleculaire schakel werd verbonden met de werkelijke ziektelast.
GCN5 omhoog of omlaag zetten in dieren
Om oorzaak en gevolg te testen verhoogde of verwijderde het team GCN5 genetisch specifiek in muislevercellen. Wanneer GCN5 werd opgevoerd, ontwikkelden muizen op een vetrijk dieet zwaardere, vettere levers, hogere bloedvetten en meer leverschade, ook al aten ze niet meer of kwamen ze niet meer aan in lichaamsgewicht. In kweek gekweekte levercellen gedroegen zich vergelijkbaar: extra GCN5 leidde tot grotere en talrijkere vetdruppels. Daarentegen waren muizen die zodanig ontworpen waren dat ze GCN5 alleen in hun levercellen misten sterk beschermd. In verschillende dieetmodellen die mensachtige MASLD en de meer ontstekingsrijke vorm nabootsen, stapelden deze dieren minder levervet op, hadden ze lagere bloedlipiden en leverenzymen, en ontwikkelden ze minder ontsteking en littekenvorming.
Hoe GCN5 de lever aanzet tot vetmaken
Dieper in de metabolismeanalyse maten de onderzoekers vele vetzuren en hun bouwstenen in de lever. Verlies van GCN5 verminderde vooral vetten die de lever van grond af aan maakt, een proces bekend als de novo lipogenese, terwijl die uit de voeding afkomstige meervoudig onverzadigde vetten grotendeels ongewijzigd bleven. Genexpressie‑ en isotopen‑tracerexperimenten lieten zien dat GCN5 bovenaan staat van een meesterregulator van vetvorming genaamd SREBP1c. Wanneer GCN5 actief was, werden genen die vetzuren bouwen en modificeren ingeschakeld en steeg het interne vetproductietempo van de lever. Het verwijderen of blokkeren van GCN5 draaide dit programma terug en verminderde de stroom koolstof van suiker naar nieuwgemaakt levervet.
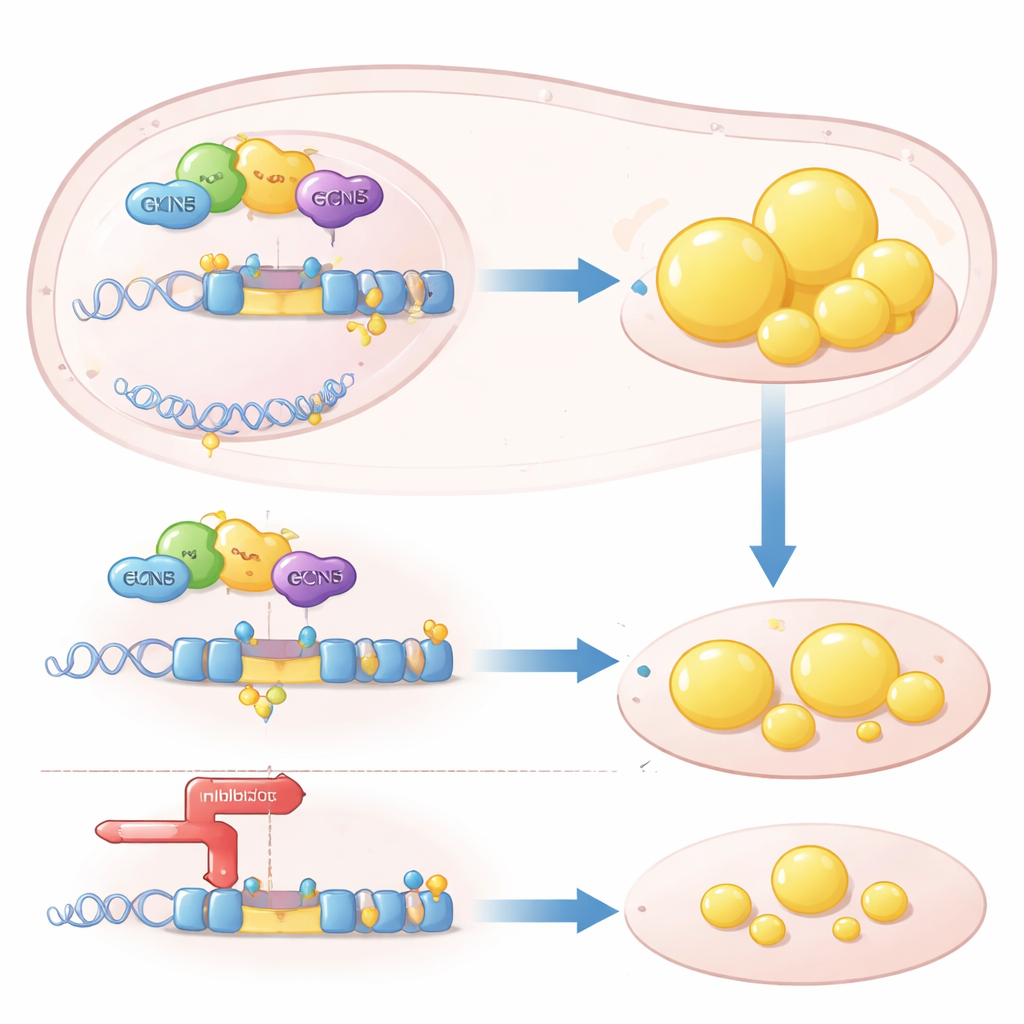
Een epigenetische hefboom op een sleutelvetgen
Mechanistisch werkt GCN5 als een “epigenetische” hefboom: het wijzigt chemisch histoneiwitten op het DNA om bepaalde genen gemakkelijker afleesbaar te maken. De auteurs toonden aan dat GCN5 wordt gerekruteerd naar het regelgebied van het SREBP1c‑gen samen met een nucleaire receptor genaamd LXRα, die cholesterolgerelateerde moleculen waarneemt. Eenmaal daar voegt GCN5 acetylgroepen toe aan histon H3, waardoor de lokale chromatine losser wordt en de transcriptie van SREBP1c wordt verhoogd. Dit effect was sterk selectief: GCN5 versterkte LXRα’s vermogen om SREBP1c aan te zetten, maar niet een ander LXR‑doel, ABCA1, dat helpt cholesterol uit weefsels te verwijderen. Zonder GCN5 kon LXRα niet efficiënt het SREBP1c‑promotergebied benaderen en stokte het downstream vet‑syntheseprogramma.
Een kandidaat‑medicijn en een veelbelovende combinatie
Het team testte vervolgens CPTH2, een kleinmoleculair remmer van GCN5 die zich concentreert in de lever. In muismodellen die al op vette diëten stonden, verminderde CPTH2 de levergrootte, vetinhoud en merkers van beschadiging zonder duidelijke toxiciteit of veranderingen in voedselinname. In gekweekte menselijke en muislevercellen verlaagde CPTH2 vetdruppels en triglyceriden alleen wanneer GCN5 aanwezig was, wat bevestigt dat de werking specifiek is. Belangrijk is dat CPTH2 in zowel cellen als muizen die met LXR‑activerende stoffen werden behandeld (ontworpen om cholesterolverwijdering te verbeteren en atherosclerose te bestrijden) selectief de ongewenste stijging van SREBP1c‑gedreven vetproductie blokkeerde, terwijl genen die reverse cholesterol transport bevorderen behouden bleven. In combinatie met een LXR‑agonist bij hoogvetgevoede muizen verlaagde CPTH2 schadelijke bloedlipiden en levercholesterol verder en voorkwam extra vetophoping in de lever.
Wat dit betekent voor patiënten
De studie positioneert GCN5 als een centrale drijver van levervetophoping bij MASLD door dieet‑ en hormonale signalen te koppelen aan de SREBP1c‑vetproductieschakelaar. Omdat GCN5 schijnbaar niet essentieel is voor de voordelige cholesterol‑clearingtak van LXR‑signalering, zouden middelen die GCN5 remmen—zoals CPTH2 of meer geavanceerde opvolgers—levervet en ontsteking kunnen temmen terwijl hartbeschermende therapieën hun werk blijven doen. Voor mensen met risico op zowel vette leverziekte als hart‑ en vaatziekten kan het gericht aanpakken van deze epigenetische schakel op termijn een manier bieden om de lever te beschermen zonder de voordelen van verbeterde cholesterolhuishouding op te geven.
Bronvermelding: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Trefwoorden: vette leverziekte, epigenetica, lipidenmetabolisme, levermetabolisme, nucleaire receptoren