Clear Sky Science · nl
Het N-Myc MB0–MBI-gebied gaat specifiek en dynamisch om met de N-lob van Aurora kinase A
Waarom dit belangrijk is voor kankerbehandeling
Veel agressieve kinderkankers zijn afhankelijk van een eiwit genaamd N-Myc om tumorcellen te laten groeien. N-Myc zelf is moeilijk met medicijnen te blokkeren omdat het zich meer gedraagt als een slappe streng spaghetti dan als een star slot waarin een sleutel past. Deze studie onthult, met ongekende detaillering, hoe N-Myc een ander eiwit — het enzym Aurora kinase A (AurA) — vastgrijpt om diens activiteit te versterken en zo kankercellen te helpen overleven. Door deze samenwerking in kaart te brengen, ontdekken de onderzoekers een realistische manier om die met kleine moleculen te verbreken.
Een flexibele onruststoker vindt een vaste partner
N-Myc behoort tot de MYC-familie van hoofdregelaars die celgroei, stofwisseling en celdeling aansturen. Wanneer deze schakelaars overproduceren, worden ze krachtige kankerverwekkers, vooral in tumoren van het zenuwstelsel zoals hoogrisico-neuroblastoom bij kinderen. In tegenstelling tot veel enzymen of receptoren vouwt N-Myc zich niet zelf tot een vaste 3D-structuur; het is een “intrinsiek gedesorganiseerd” eiwit dat constant beweegt en van vorm verandert. Die flexibiliteit maakt het aanpasbaar maar ook berucht moeilijk om met geneesmiddelen te adresseren. AurA is daarentegen een goed gestructureerd enzym dat helpt bij het organiseren van celdeling. Eerder werk toonde aan dat AurA N-Myc in tumorcellen helpt stabiliseren en dat de twee eiwitten fysiek met elkaar interageren, maar de precieze aard en het belang van de contactpunten bleef onduidelijk.
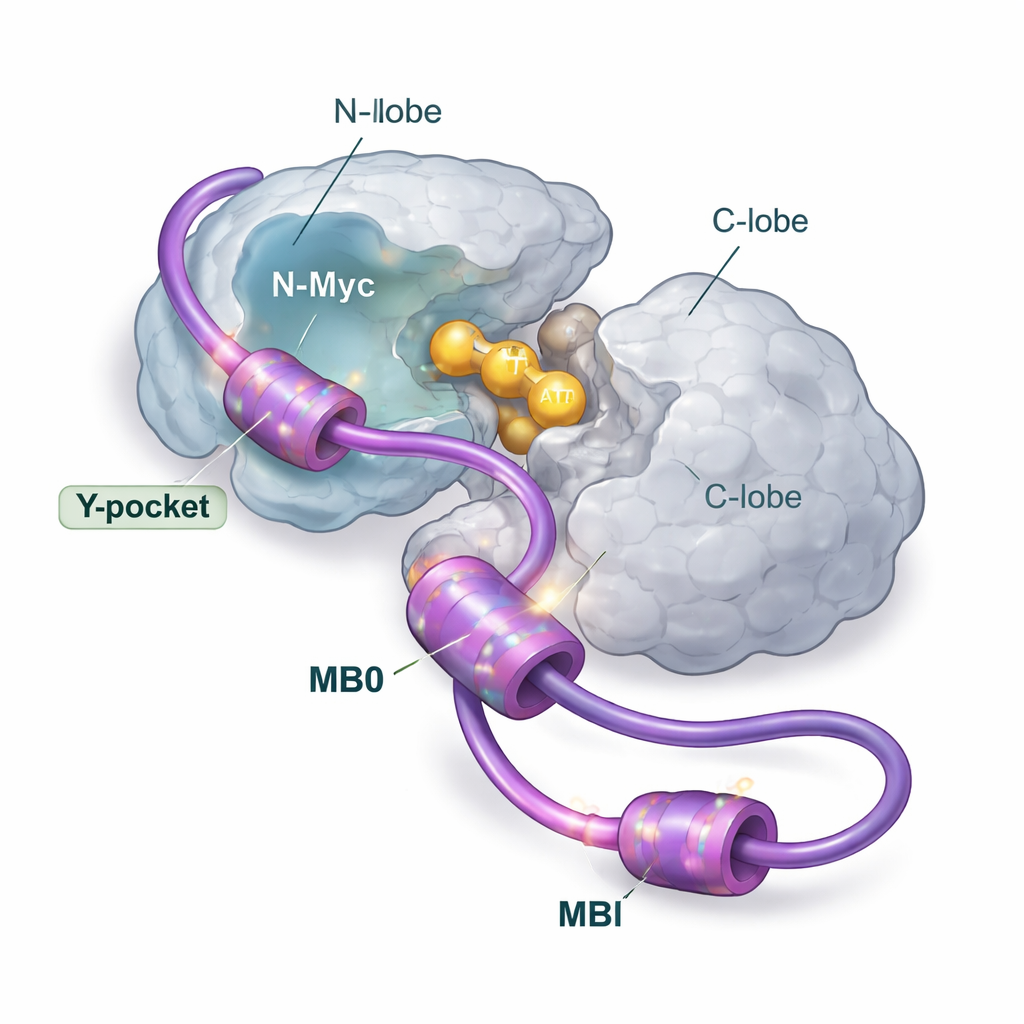
Meerdere grijppunten, één hoofdlandingsplaats
Met een breed arsenaal aan structurele en biofysische methoden — waaronder nucleaire magnetische resonantie, röntgenspreiding, massaspectrometrie, calorimetrie en computermodellering — ontleden de auteurs hoe N-Myc en AurA samenkomen in oplossing. Ze concentreerden zich op het voorste uiteinde van N-Myc, dat twee geconserveerde regio’s bevat die MB0 en MBI heten. Deze korte segmenten zijn rijk aan aromatische bouwstenen (zoals fenylalanine, tyrosine en tryptofaan) die de neiging hebben aan vette pocketjes op partner-eiwitten te blijven plakken. Het team laat zien dat N-Myc voornamelijk in een 1:1-complex aan AurA bindt, met MB0 en MBI als de primaire contactzones. Een andere N-Myc-stretch die eerder in kristalstructuren aandacht kreeg, blijkt slechts een kleine rol te spelen wanneer het volledige MB0–MBI-gebied aanwezig is.
Een dynamische handdruk die het enzym aanzet
In plaats van in één vergrendelde houding te schieten, blijft N-Myc grotendeels gedesorganiseerd wanneer het aan AurA gebonden is. De gegevens wijzen op een “wazig” complex: verschillende N-Myc-segmenten wisselen elkaar af bij het contact maken met verschillende plekken op de N-lob van AurA, vooral een groef die bekendstaat als het Y-pocket en een nabijgelegen lus die signalen naar de actieve plaats koppelt. Ondanks die losheid is het effect duidelijk — de binding van MB0 en MBI stabiliseert de AurA N-lob en verhoogt diens kinase-activiteit, wat betekent dat het efficiënter fosfaatgroepen overdraagt op zijn doelwitten. Toen de onderzoekers systematisch sleutel-aromatische residuen in MB0 en MBI vervingen door alanine, werd het N-Myc–AurA-complex zwakker, was het enzym minder gestabiliseerd en daalde de activiteit. Dit toont aan dat specifieke aromatische “ankers” in de anders losse N-Myc-keten essentieel zijn om AurA te activeren.
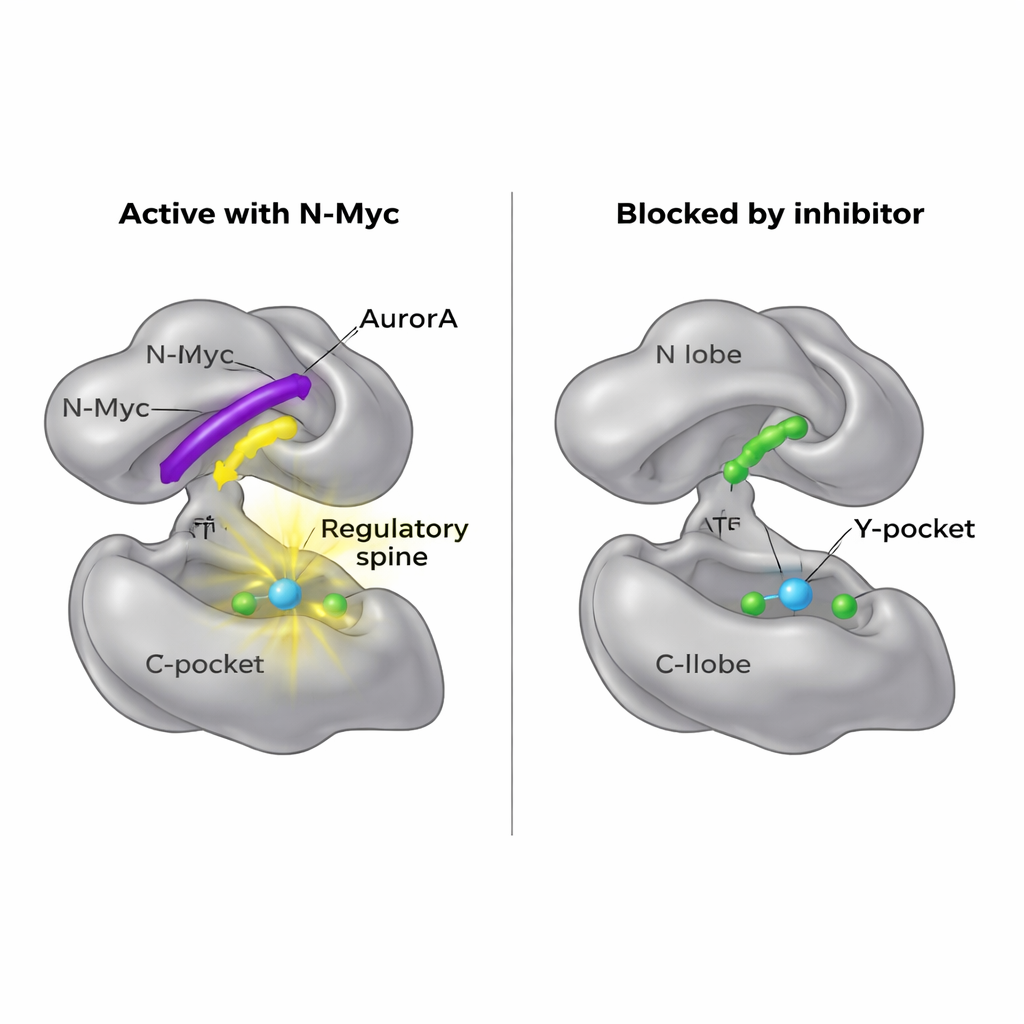
Een nieuw instappunt voor geneesmiddelen kraken
Aangezien N-Myc zelf moeilijk met medicijnen te treffen is, vroegen de onderzoekers zich af of ze in plaats daarvan diens aanlegplaats op AurA konden blokkeren. Hun structurele kaarten toonden dat MB0 en MBI hetzelfde algemene gebied van de N-lob bezetten dat een andere partner, TPX2, gebruikt om AurA te activeren. Een klein molecuul genaamd AurkinA staat al bekend om in het Y-pocket te klemmen en TPX2 te verdringen. In bindingsproeven concurreerde AurkinA effectief ook met N-Myc om de N-lob van AurA en voorkwam zo dat zowel N-Myc1–69 als N-Myc1–100-fragmenten zich hechtten. Dit resultaat laat zien dat het N-lob-oppervlak, en in het bijzonder het Y-pocket, een druggable hotspot is die niet alleen klassieke regulatoren zoals TPX2 controleert, maar ook gedesorganiseerde oncoproteïnen zoals N-Myc.
Wat dit betekent voor toekomstige therapieën
Dit werk herschikt het N-Myc–AurA-partnerschap als een dynamische, multi-contact omhelzing gecentreerd op de AurA N-lob, in plaats van een enkele stijve bindingsplaats. Voor niet-specialisten is de kernboodschap dat zelfs een vormloos kankereiwit als N-Myc indirect kan worden aangepakt door een stevig aanlegplekje op het partnerenzym te targeten. Door te laten zien dat bestaande N-lob-bindende verbindingen N-Myc van AurA kunnen wegduwen, opent de studie een duidelijk pad naar geneesmiddelen die deze interactie selectief verstoren. Zulke middelen zouden een cruciale ondersteuning voor N-Myc in hoogrisico kindertumoren kunnen verzwakken en, met verdere ontwikkeling, een nieuwe behandelroute bieden voor kankers die lang als “ongeneeslijk” werden beschouwd.
Bronvermelding: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Trefwoorden: N-Myc, Aurora kinase A, intrinsiek gedesorganiseerde eiwitten, neuroblastoom, eiwit–eiwit interactie-remmers