Clear Sky Science · nl
Gelijktijdige bevordering van fotokatalytische CH4‑conversie en H2O2‑productie via nanopore‑waterbeperking
Een broeikasgas omzetten in nuttige vloeistoffen
Methaan, het belangrijkste bestanddeel van aardgas, is zowel een waardevolle grondstof als een krachtig broeikasgas. Het zacht omzetten ervan in vloeibare chemicaliën en brandstoffen kan helpen de uitstoot te verminderen en tegelijk alledaagse producten zoals oplosmiddelen en desinfectiemiddelen te leveren. Deze studie toont een manier om met licht, water en zorgvuldig ontworpen nanodeeltjes methaan op te waarderen tot nuttige zuurstofhoudende vloeistoffen, terwijl tegelijkertijd waterstofperoxide wordt geproduceerd, een veelgebruikt desinfectiemiddel en een groen oxidatiemiddel.
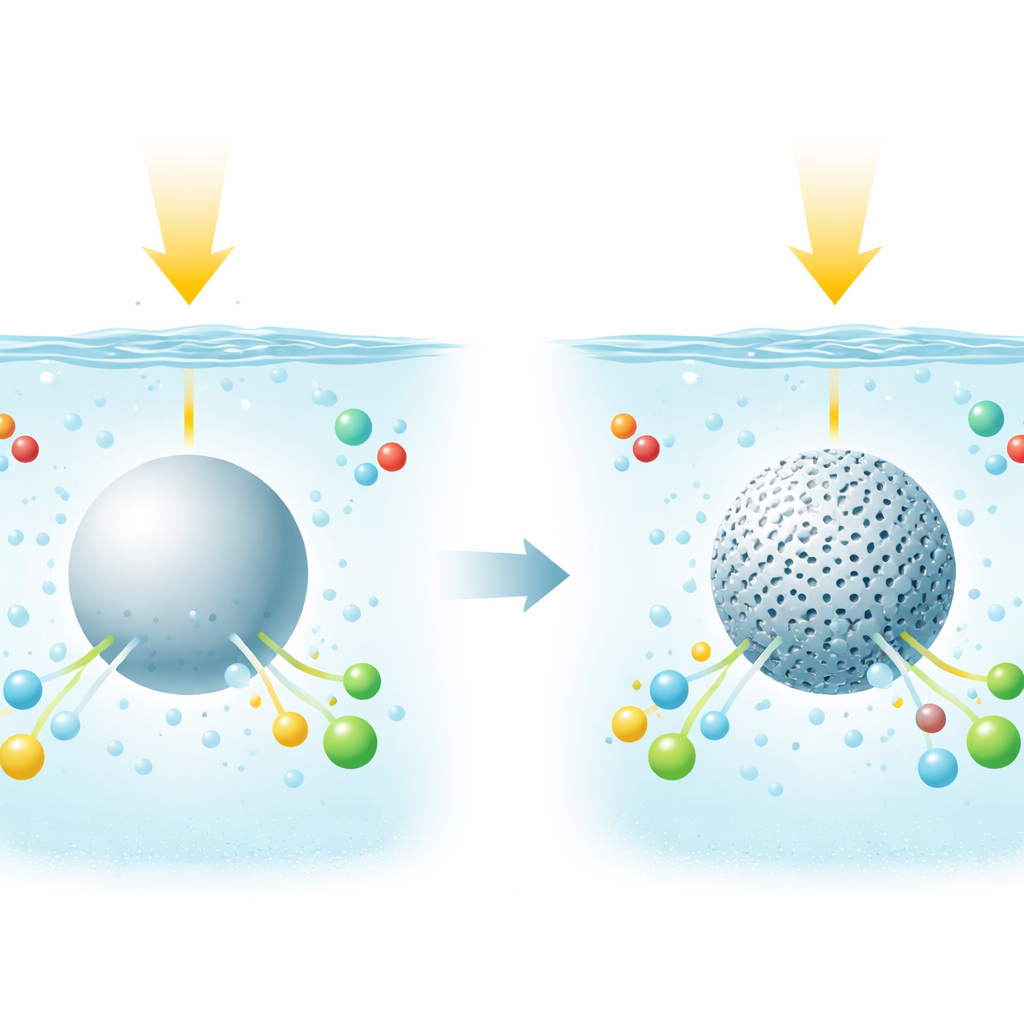
Waarom de structuur van water ertoe doet
Veel duurzame energiereacties vinden plaats in water, waar elektronen en protonen samen in strak georkestreerde stappen moeten bewegen. In gewoon vloeibaar water worden moleculen bijeengehouden in een voortdurend veranderend netwerk van waterstofbruggen, dat stilletjes bepaalt hoe gemakkelijk ladingen en atomen zich kunnen verplaatsen. De auteurs vroegen zich af: wat als je water zachtjes in zeer kleine ruimten kunt persen zodat dit netwerk verandert? Zou dat het makkelijker maken voor lichtgeactiveerde katalysatoren om methaan naar gewenste producten te leiden in plaats van het volledig te verbranden tot kooldioxide?
Een kleine kooi rond een actief kern
Om dit idee te testen bouwde het team kern‑schil deeltjes. In het centrum bevindt zich een goed bekende fotokatalysator, titaniumdioxide, versierd met kleine metalen deeltjes zoals goud of platina. Rond deze kern groeiden ze een dunne laag transparant silica met nanometerschaal poriën gevuld met water. Door de poriegrootte terug te brengen tot ongeveer 1,7 nanometer—slechts een paar watermoleculen breed—creëerden ze een geconfineerde waterlaag die de katalysatoroppervlakte omarmt. Belangrijk is dat lichtabsorptie en de basiseigenschappen van de katalysator vrijwel ongewijzigd bleven; wat veranderde was hoe water zich in deze kleine kanalen positioneerde en bewoog.
Van methaan en zuurstof naar vloeistoffen en peroxide
Wanneer deze deeltjes in water onder belichting in aanwezigheid van methaan en zuurstof werden gebruikt, verbeterde het geconfineerde‑waterontwerp de prestaties sterk. Vergeleken met dezelfde katalysator zonder de poreuze schil verdriedubbelde ongeveer de conversie van methaan en nam de productie van waterstofperoxide met ongeveer tweeëntwintig keer toe. Het proces leverde zuurstofhoudende vloeibare producten zoals methanol en verwante moleculen met hoge selectiviteit, wat betekent dat er veel minder verregaande oxidatie naar kooldioxide plaatsvond. Het effect was robuust: het trad op onder verschillende lichtbronnen, bleef behouden over vele reactiemodules en kon worden gereproduceerd met andere metalen en zelfs andere halfgeleiderkernen, wat aantoont dat de strategie breed toepasbaar is in plaats van een eenmalige truc.
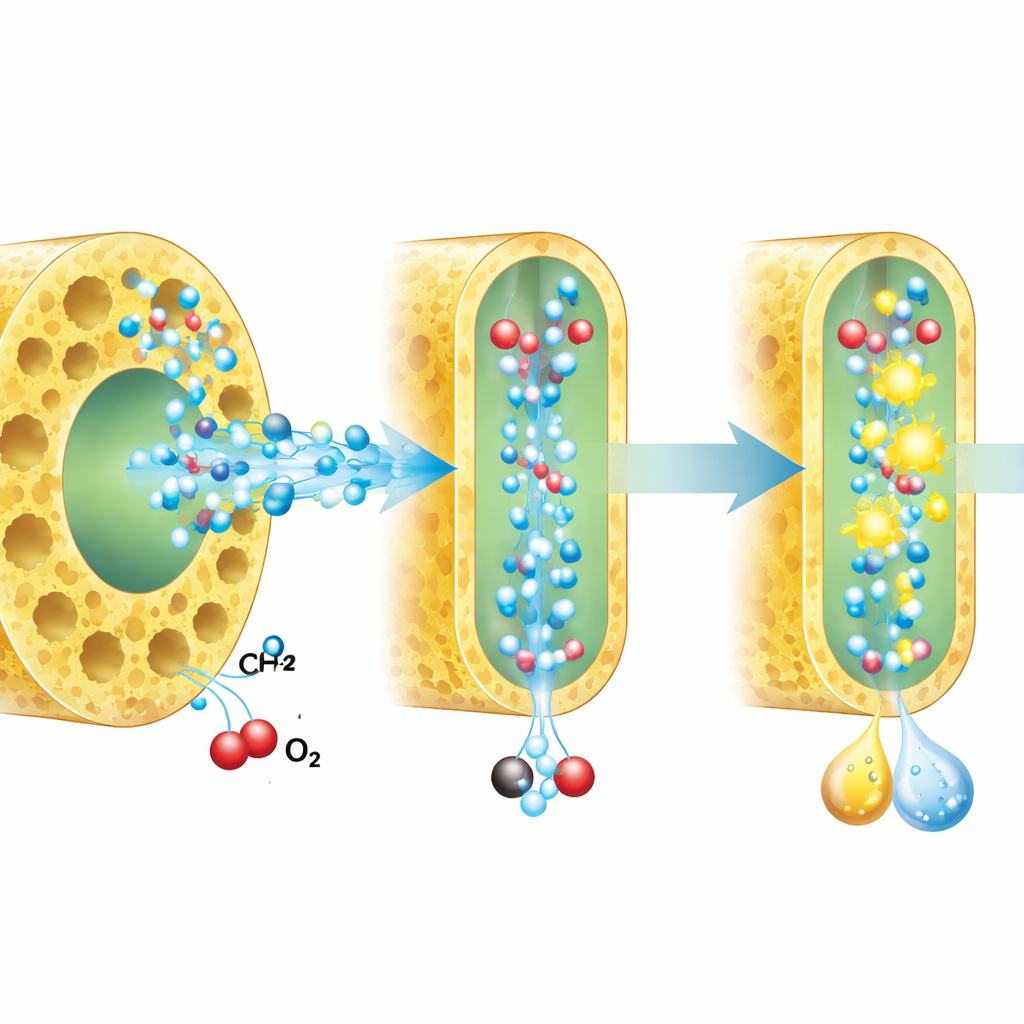
Hoe ingeknepen water het reactiepaden verandert
Om te begrijpen waarom confinering helpt, combineerden de onderzoekers spectroscopische metingen, radicalenvangstexperimenten, isotopenlabeling en computersimulaties. Ze ontdekten dat geconfineerd water een zwakker, meer lineair netwerk van waterstofbruggen vormt dan bulkwater. In deze veranderde omgeving worden sleutelreactieve soorten—kortlevende zuurstofdragende radicalen die methaan aanvallen—efficiënter gegenereerd en leven ze langer in de buurt van het katalysatoroppervlak. Tegelijk wordt het pad van zuurstofreductie gestuurd naar het direct vormen van waterstofperoxide in plaats van andere, minder bruikbare intermediairen. Isotoopstudies, waarbij waterstof werd vervangen door deuterium of zuurstofatomen opnieuw werden gelabeld, bevestigden dat de beweging van protonen meer centraal wordt in de langzame, bepalende stappen van zowel wateroxidatie als zuurstofreductie zodra water geconfineerd is.
Een nieuwe hendel voor schonere chemie
In alledaagse termen werkt de silica‑schil als een zorgvuldig ontworpen spons die water dwingt in smalle gangen rond de actieve katalysator, waardoor subtiel verandert hoe het samenhangt en hoe gemakkelijk protonen en elektronen kunnen bewegen. Deze herschikte micro‑omgeving maakt het eenvoudiger voor lichtgeprikkelde ladingen om methaan te bewerken tot waardevolle vloeistoffen en om zuurstof om te zetten in waterstofperoxide, in plaats van simpelweg de brandstof te verbranden. Het werk suggereert dat het afstemmen van het "gevoel" van water nabij vaste oppervlakken—zonder het actieve materiaal zelf te veranderen—een krachtig ontwerpgereedschap kan worden voor schonere chemische processen, van het omzetten van broeikasgassen tot het produceren van groene oxidanten en brandstoffen.
Bronvermelding: Lv, F., Wei, S., Wu, X. et al. Simultaneous promotion of photocatalytic CH4 conversion and H2O2 production via nanopore water confinement. Nat Commun 17, 2119 (2026). https://doi.org/10.1038/s41467-026-69719-z
Trefwoorden: fotokatalytische methaanoxidatie, nanoporöse kern‑schil katalysatoren, geconfineerd water, waterstofperoxideproductie, protongekoppelde elektronenoverdracht