Clear Sky Science · nl
Een ruimtelijk resoluut menselijk glioblastoom‑atlas onthult onderscheidende cellulaire en moleculaire patronen van anatomische niches
Waarom deze hersenkankerkaart ertoe doet
Glioblastoom is een van de dodelijkste hersentumoren, deels omdat elk gezwel een lappendeken is van verschillende celtypes en micro‑omgevingen. Standaardscans en laboratoriumtesten zien het gezwel meestal als één massa. Deze studie bouwt een hoogresolutie "atlas" die laat zien waar elk belangrijk celtype zich in menselijke glioblastomen bevindt, hoe deze cellen zich groeperen in onderscheiden buurten, en hoe sommige van die buurten mogelijk bijdragen aan tumorgroei en kortere overleving van patiënten.
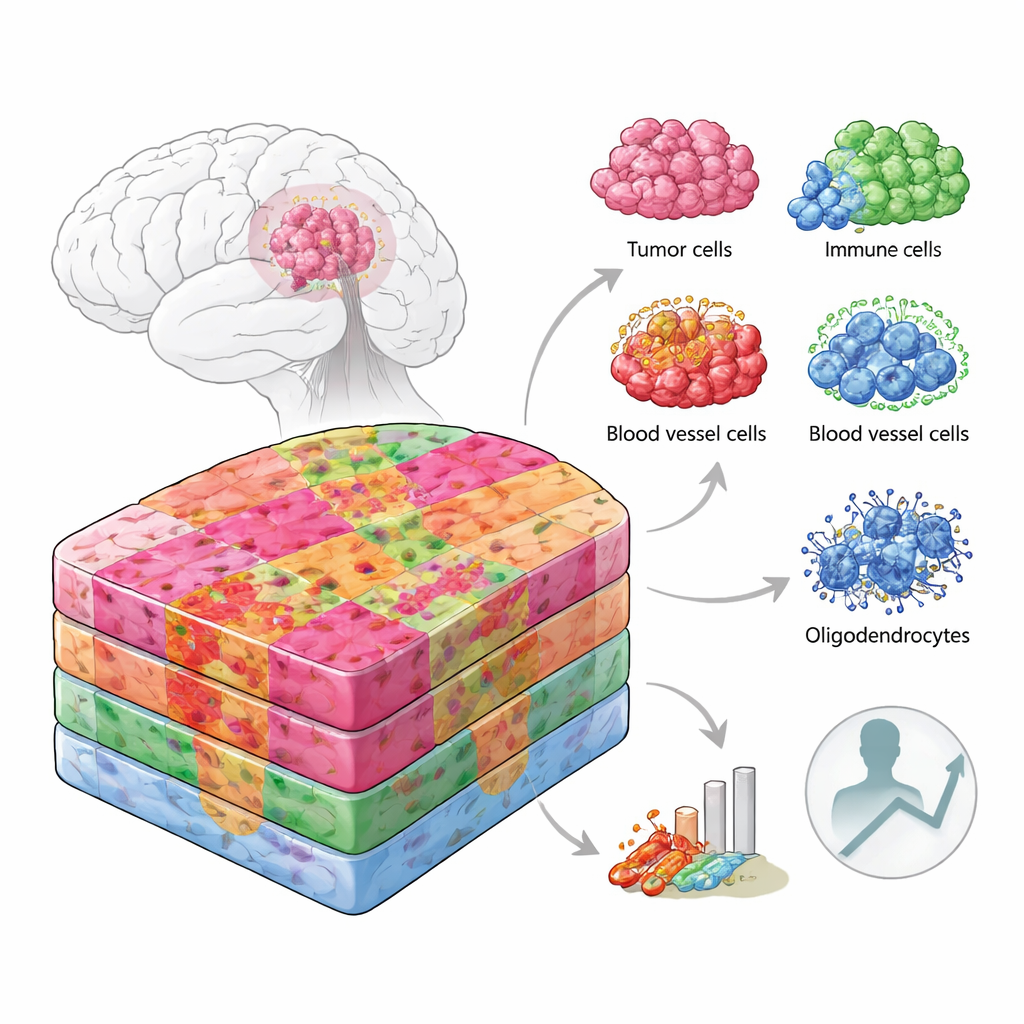
Gezien als stadsplattegronden
In plaats van een tumordwarsdoorsnede als uniform te behandelen, benaderden de onderzoekers het als een stadskaart, waarbij elk district zijn eigen inrichting en bewoners heeft. Ze combineerden meerdere geavanceerde technieken die genactiviteit uitlezen van duizenden kleine plekjes in tumormateriaal, en koppelden dit aan enkel‑celgegevens en eiwitmetingen. Belangrijk is dat ze dit niet alleen deden op vers‑bevroren monsters uit de operatiekamer, maar ook op routinematig gearchiveerd, in paraffine ingebed ziekenhuisweefsel — wat de meeste pathologielaboratoria bewaren. In totaal analyseerden ze meer dan 100.000 ruimtelijk gebarcodede regio’s en ruim 220.000 individuele cellen van patiënten van verschillende leeftijden en genetische achtergronden, met zowel de dichte tumorcore als de meer diffuse randen.
Verborgen buurten in glioblastoom
Door genactiviteit over hoge‑magnificatie microscoopbeelden heen te leggen, verdeelde het team elk gezwel in anatomische “niches”, zoals de voorhoede waar kankercellen gezond hersenweefsel binnendringen, de dichtbevolkte centrale zones, vasculair rijke gebieden, en regio’s rond dood of zuurstofarme weefsels. Elke niche bleek zijn eigen mengeling van celtypes te herbergen. De tumorrand in grijze stof was rijk aan neuronen en typische steuncellen, terwijl de rand in witte stof veel oligodendrocyten bevatte, de cellen die normaal zenuwvezels isoleren. Bepaalde vasculaire niches zaten vol gespecialiseerde bloedvat‑ en steuncellen, terwijl andere werden gedomineerd door immuuncellen en littekenachtig weefsel. Hypoxische zones nabij dood weefsel huisvestten vooral agressieve, mesenchymale‑achtige tumorcellen en macrophagen, met veel minder cellulaire diversiteit.
Een verrassende rol voor steuncellen
Een van de opvallendste bevindingen betrof oligodendrocyten, doorgaans gezien als rustige "isolatoren" in de hersenen. De atlas toonde vier onderscheiden oligodendrocyttoestanden, waaronder een eerder ondergewaardeerd type dat vrijwel uitsluitend in de kernen van glioblastomen leek voor te komen. Deze cellen waren vele van hun myeline‑gerelateerde genen kwijtgeraakt en schakelden in plaats daarvan genen aan die gekoppeld zijn aan ontsteking en stress, en leken op ziekte‑geassocieerde oligodendrocyten die gezien worden bij multiple sclerose en andere hersenaandoeningen. Ruimtelijk gezien clustereerde deze immuun‑achtige oligodendrocytpopulatie in een "immuun–gliale niche" naast geactiveerde microglia, macrophagen, afwijkende bloedvatcellen en mesenchymale‑achtige tumorcellen, maar opvallend genoeg niet in de meest zuurstofarme regio’s.
Microscopische patronen koppelen aan patiëntuitkomst
De auteurs onderzochten vervolgens of de genprogramma’s die deze oligodendrocyttoestanden definiëren terug te vinden zijn in grote verzamelingen tumorstalen met gekoppelde patiëntgegevens. In twee onafhankelijke glioma‑cohorten correleerde een signatuur van conventionele, myeline‑producerende oligodendrocyten met betere overleving, zelfs na correctie voor leeftijd en belangrijke genetische risicomarkers. Daarentegen ging de immuun‑geactiveerde oligodendrocyt‑signatuur samen met slechtere overleving en was prominenter in agressieve, therapie‑resistente tumoren, vooral in teruggekeerde tumoren die ontbraken aan een veelvoorkomende methylatieverandering gerelateerd aan DNA‑herstel. Dit suggereert dat de manier waarop oligodendrocyten in het gezwel worden herprogrammeerd, en hun positie ten opzichte van tumor‑ en immuuncellen, invloed kan hebben op hoe de ziekte op behandeling reageert en hoe waarschijnlijk recidief is.
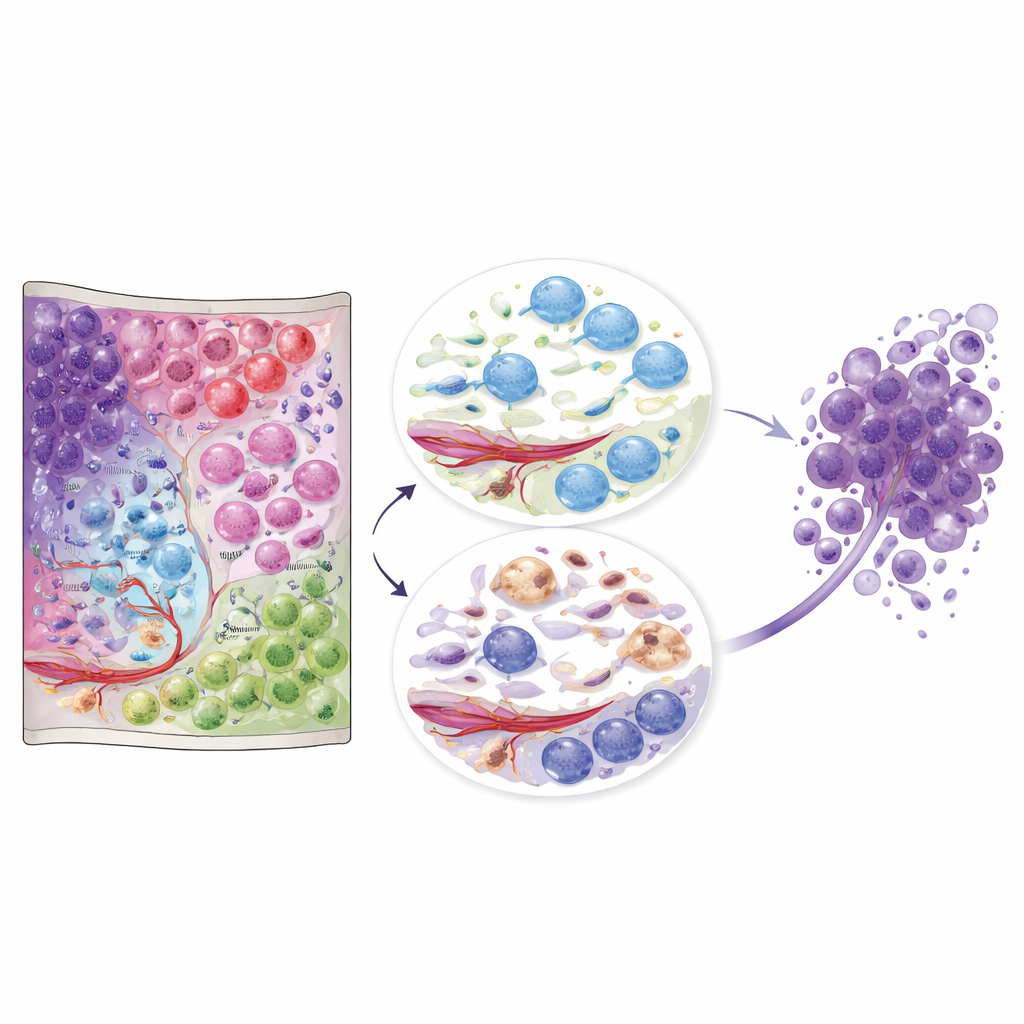
Wat deze atlas betekent voor toekomstige zorg
Samen veranderen deze gegevens glioblastoom van een vage massa in een gedetailleerd landschap van elkaar beïnvloedende celgemeenschappen. Voor niet‑specialisten is de kernboodschap dat locatie en buren ertoe doen: dezelfde grote celtypes gedragen zich heel anders afhankelijk van de niche die ze bezetten. De openbaar beschikbare atlas biedt een referentie die andere onderzoekers en clinici kunnen gebruiken om hun eigen monsters in deze ruimtelijke context te plaatsen. Op de lange termijn zouden therapieën niet alleen ontworpen kunnen worden om tumorcellen te doden, maar ook om schadelijke niches te verstoren — zoals immuun‑littekenregio’s of immuun‑geactiveerde oligodendrocytzones — die lijken bij te dragen aan tumoroverleving en terugkeer.
Bronvermelding: Sonpatki, P., Park, H.J., Xing, Y.L. et al. A spatially resolved human glioblastoma atlas reveals distinct cellular and molecular patterns of anatomical niches. Nat Commun 17, 2951 (2026). https://doi.org/10.1038/s41467-026-69716-2
Trefwoorden: glioblastoom, ruimtelijke transcriptomica, tumormicro‑omgeving, oligodendrocyten, hersenkankeratlas