Clear Sky Science · nl
Spatial perturb-seq: single-cell functionele genomica binnen intacte weefselarchitectuur
Genen in actie zien in levende hersencircuits
Veel hersenaandoeningen, van Alzheimer tot Parkinson, worden in verband gebracht met risicogenen, maar we weten nog weinig over hoe die genen individuele cellen in de levende hersenen beïnvloeden. Deze studie introduceert een krachtige methode om te observeren wat er gebeurt wanneer specifieke genen in enkele cellen worden uitgeschakeld, terwijl die cellen in hun natuurlijke omgeving binnen hersenweefsel blijven. De aanpak, Spatial Perturb-Seq genoemd, helpt genetisch risico te koppelen aan verstoord cellulair gedrag en aan cel-tot-celcommunicatie in de intacte hersenen.
Een nieuwe manier om veel genen tegelijk te testen
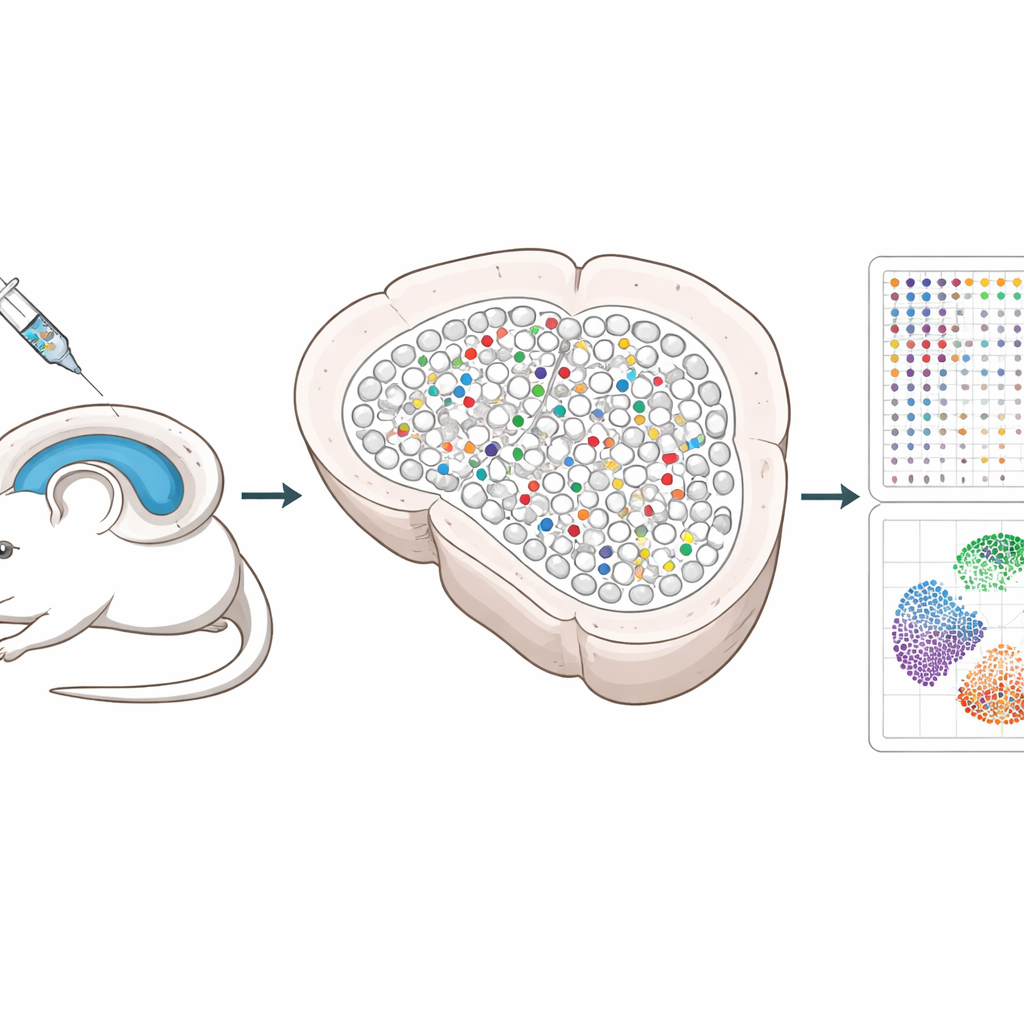
De onderzoekers bouwden een systeem dat CRISPR-genbewerkingsinstrumenten gebruikt, toegediend via onschadelijke virussen in de hippocampus, een hersengebied dat belangrijk is voor geheugen. Elk virus draagt drie gidsen die een gekozen gen uitschakelen, samen met een unieke DNA-"barcode" en een fluorescerende marker zodat bewerkte cellen later opgespoord kunnen worden. Door deze virussen te mengen en in lage dosis te injecteren, worden slechts een klein, verspreid deel van de cellen bewerkt, terwijl de meeste buren onaangetast blijven. Dit spaarzame patroon stelt wetenschappers in staat de veranderingen binnen bewerkte cellen te scheiden van veranderingen in naburige gezonde cellen.
De kaart van de hersenen intact houden
Traditionele single-cell methoden vereisen dat weefsels worden gefragmenteerd, waardoor de precieze positie van cellen verloren gaat en kwetsbare neuronen soms verdwijnen. Spatial Perturb-Seq leest in plaats daarvan genactiviteit direct uit dunne hersensneden, zodat de locatie van elke cel behouden blijft. Met een technologie genaamd Stereo-seq legde het team volledige genexpressieprofielen vast voor meer dan 200.000 cellen, terwijl ze ook de CRISPR-barcodes uitlazen en de coördinaten van elke cel in het weefsel registreerden. Ze gebruikten vervolgens geavanceerde beeldgebaseerde algoritmen om elke cel af te bakenen en computationele hulpmiddelen om celtypen en lokale buurten te identificeren, met speciale focus op hippocampale neuronen en hun nauwe contacten.
Hoe bewerkte cellen hun buren beïnvloeden
Met de weefselkaart in handen vergeleken de wetenschappers bewerkte neuronen met onbewerkte neuronen en, apart, met de onbewerkte buren rond elke bewerkte cel. Dit stelde hen in staat "cel-autonome" effecten (binnen de bewerkte cel) te onderscheiden van "niet-cel-autonome" effecten (in de omliggende microomgeving). Het knock-outten van 18 verschillende genen, vele verbonden met het risico op neurodegeneratieve aandoeningen, leverde uiteenlopende patronen van genveranderingen op binnen de bewerkte neuronen. Sommige ingrepen, zoals die gericht op het gen Cfap410, veroorzaakten ook sterke verschuivingen in genactiviteit in nabijgelegen cellen, wat wijst op veranderde lokale signalering en ondersteuning.
Aanwijzingen voor pathways bij neurodegeneratie
Verschillende genen gaven bijzonder interessante inzichten. Het uitschakelen van Lrrk2, een belangrijk risicogen voor de ziekte van Parkinson, veroorzaakte grote veranderingen in de bewerkte neuronen, waaronder verlaagde niveaus van Bc1, een RNA-molecuul dat belangrijk is voor het afstemmen van eiwitproductie bij synapsen. Tegelijk lieten de buurcellen gewijzigde expressie zien van genen die betrokken zijn bij synapsstructuur, eiwittransport en calciumhuishouding, wat suggereert dat Lrrk2-gerelateerde problemen zich door lokale circuits voortplanten. Het knock-outten van een ander gen, Srf, verstoorde een netwerk van genen dat verband houdt met neuronale groei en plasticiteit, en verzwakte specifieke ligand–receptor signaleringsroutes tussen neuronen, wat duidt op verstoorde cel-tot-celcommunicatie. Door deze signaleringsparen systematisch te scoren, kon het team vaststellen welke communicatieroutes voor elk gen het meest werden aangetast.
Flexibele tools om genetische effecten in kaart te brengen
Om te laten zien dat Spatial Perturb-Seq niet is vastgepind op één platform, paste het team het ook aan voor een beeldgebaseerd systeem genaamd Xenium. Daar lezen vooraf ontworpen probepanelen en aangepaste barcodeprobes geselecteerde genen en barcodes rechtstreeks in het weefsel uit. Hoewel deze gerichte benadering minder genen dekt dan het gehele-transcriptoom Stereo-seq, kwamen patronen van genveranderingen voor belangrijke ingrepen zoals Lrrk2 en Srf goed overeen tussen de twee methoden en met een grote externe hersenatlas. Deze kruiscontrole ondersteunt de robuustheid van de waargenomen gen- en buurt-effecten.
Wat dit betekent voor onderzoek naar hersengezondheid
In gewone bewoordingen stelt Spatial Perturb-Seq wetenschappers in staat om veel verschillende genen in individuele hersencellen uit te schakelen en vervolgens te observeren hoe die cellen en hun directe buren reageren, terwijl het bedradingsdiagram van het weefsel intact blijft. Dit maakt het mogelijk te traceren hoe genetische risicofactoren niet alleen individuele cellen verstoren, maar ook de gesprekken tussen hen, die cruciaal zijn voor een gezonde hersenfunctie. Naarmate sequencen goedkoper wordt en grotere experimenten worden uitgevoerd, kan deze aanpak helpen onthullen welke genen en lokale circuits het belangrijkst zijn in vroege stadia van aandoeningen zoals Alzheimer, Parkinson en ALS, en zo leidend zijn voor meer gerichte behandelstrategieën.
Bronvermelding: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
Trefwoorden: spatiële genomica, CRISPR-screens, single-cell sequencing, neurodegeneratie, cel-celcommunicatie