Clear Sky Science · nl
Efficiënte methanol-upcycling naar ethyleenglycol en glycolaldehyde via divergent C−C-koppelingsynthese
Een eenvoudige brandstof omzetten in nuttige bouwstenen
Methanol, een eenvoudige alcohol die kan worden geproduceerd uit kooldioxide, aardgas, steenkool of biomassa, is al een belangrijke brandstof en grondstof voor de chemie. Deze studie laat zien hoe lichtstralen en zorgvuldig ontworpen nanomaterialen methanol kunnen transformeren tot complexere, waardevollere moleculen—terwijl tegelijkertijd waterstofgas vrijkomt als een schone energiedrager. Het werk onthult een nieuwe manier om één beginmateriaal naar twee verschillende nuttige producten te sturen door slechts te variëren in hoe individuele metaalatomen op een kleine katalysatoroppervlakte zijn gerangschikt. 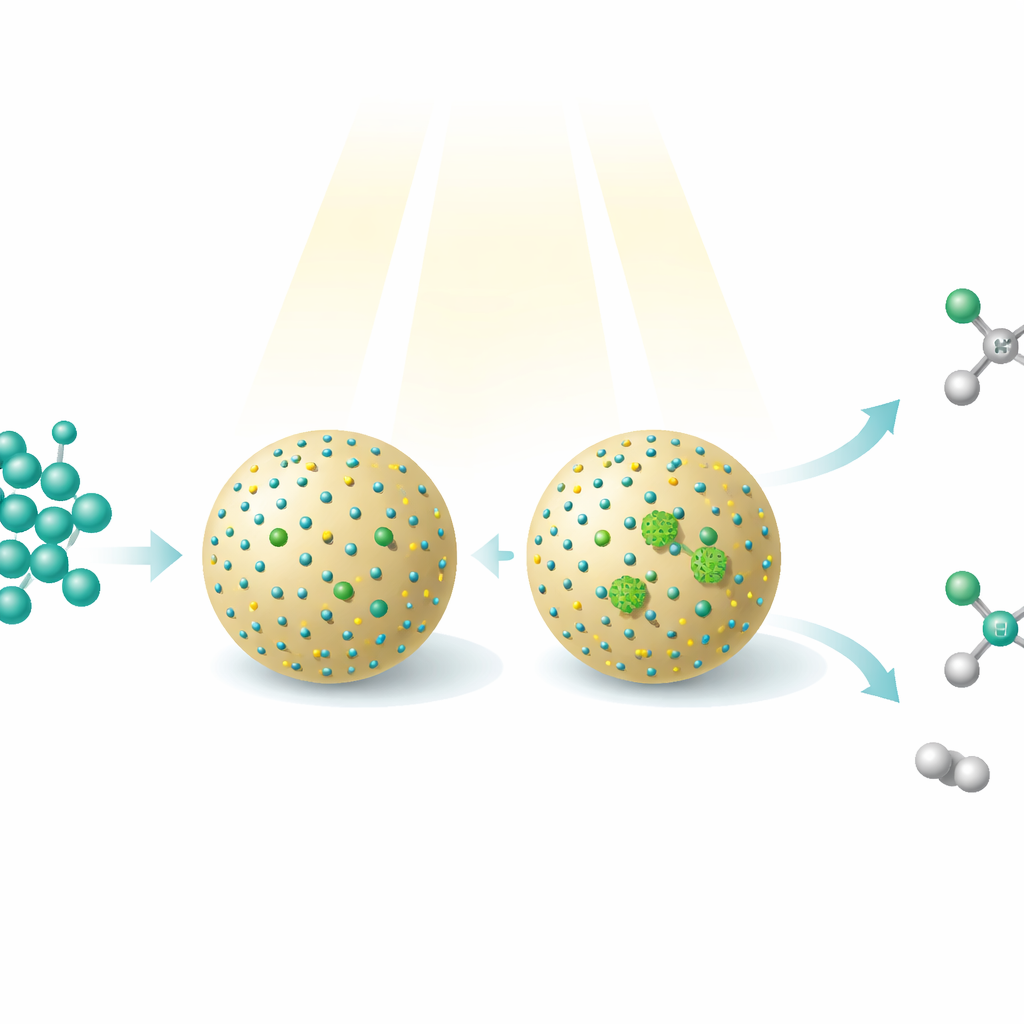
Waarom het upgraden van methanol ertoe doet
Terwijl de wereld zoekt naar alternatieven voor olie, is methanol naar voren gekomen als een aantrekkelijk vloeibaar middel om energie en koolstof op te slaan. De meeste industriële processen die methanol omzetten in grotere moleculen zijn echter grove instrumenten: ze vereisen hoge temperaturen, zijn afhankelijk van fossiele routes en produceren vaak veel ongewenste bijproducten. Chemici willen methanolmoleculen met hoge precisie koppelen zodat ze selectief precies de gewenste verbindingen kunnen maken. Dit onder milde omstandigheden doen met licht in plaats van warmte zou de integratie van chemische productie met hernieuwbare energie vergemakkelijken.
Licht-geactiveerde nanospheren doen het werk
De onderzoekers bouwden een fotokatalysator—letterlijk een door licht aangedreven katalysator—door kleine cadmium-sulfide kwantumdots op bolvormige silica-deeltjes te bevestigen. Deze kwantumdots absorberen licht en genereren energierijke elektronen en gaten die waterstofatomen van methanol kunnen afscheuren, waardoor zeer reactieve fragmenten ontstaan. Nikkelaatomen werden vervolgens op de kwantumdots gedeponeerd op twee verschillende manieren. In het ene materiaal bestond het nikkel grotendeels uit geïsoleerde enkele atomen; in het andere vormde het nikkel zeer kleine clusters van enkele atomen. Hoewel de totale samenstelling nauwelijks veranderde, beïnvloedde dit subtiele verschil in nikkelarrangement ingrijpend welke reacties zich op het oppervlak voordeden.
Twee nikkelontwerpen, twee zuivere producten
Wanneer de katalysator met enkele nikkelaatomen aan licht werd blootgesteld in methanol, gaf deze de voorkeur aan het koppelen van twee identieke methanol-afgeleide fragmenten, wat voornamelijk leidde tot ethyleenglycol—een tweewaardig alcohol dat veel wordt gebruikt in antivries en kunststoffen. Deze route bereikte ongeveer 90% selectiviteit, wat betekent dat bijna alle omgezette methanol als dit ene product eindigde, terwijl waterstofgas in overeenkomende hoeveelheden werd geproduceerd uit de verwijderde waterstofatomen. Daarentegen geleidde de katalysator met nikkelclusters dezelfde methanolfragmenten langs een andere weg. Hier werd een deel van het methanol verder geoxideerd tot een kortlevend formaldehyde-achtig intermediair, dat vervolgens met een ander fragment combineerde om glycolaldehyde te vormen, een ander twee-koolstofverbinding met vele toepassingen in fijnchemie en mogelijk in biogebaseerde processen. Deze route leverde glycolaldehyde met 96% selectiviteit, eveneens samen met waterstof. De silica-drager hielp de kwantumdots licht efficiënter te benutten en maakte de deeltjes robuuster bij vele gebruikscycli. 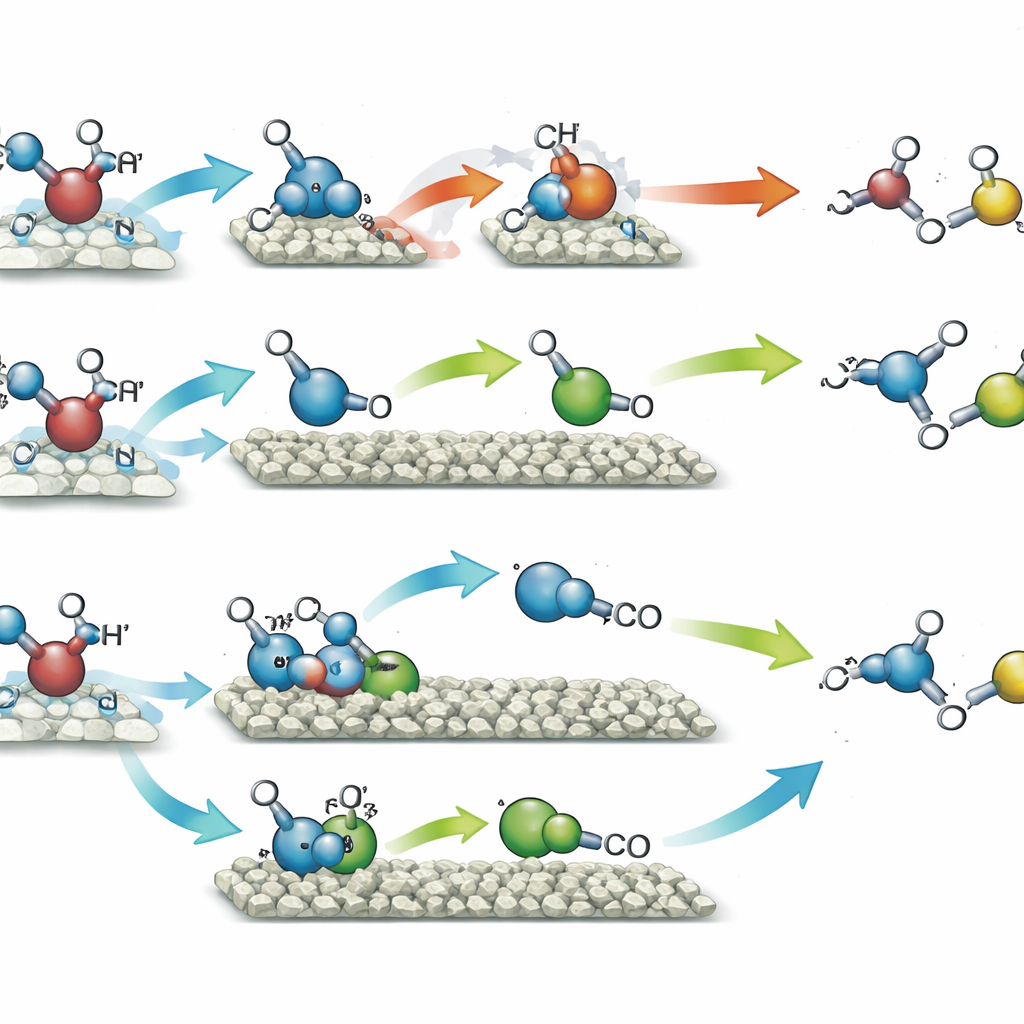
Een kijkje onder de motorkap van de reactie
Om te begrijpen waarom de twee nikkelarrangementen zich zo verschillend gedroegen, combineerde het team een reeks geavanceerde metingen met computersimulaties. Elektronparamagnetische resonantie-experimenten toonden aan dat beide katalysatoren onder licht methanol-gebaseerde radicalen genereerden, maar de clusterkatalysator bevorderde ook het breken van de zuurstof–waterstofbinding, wat leidde tot meer diverse reactieve fragmenten en tot het formaldehyde-intermediair. Tijdgerelateerde tests bevestigden dat dit intermediair in concentratie opkwam en vervolgens daalde terwijl het werd verbruikt om glycolaldehyde te maken. Kwantumchemische berekeningen brachten de energiekosten van elke kleine stap in kaart. Op enkele nikkelaatomen was het direct koppelen van twee identieke radicalen om ethyleenglycol te vormen de gemakkelijkste route. Op nikkelclusters hechtte diezelfde koppeling het product te sterk, waardoor loslating moeilijk werd, terwijl de route die eerst het asymmetrische intermediair vormde en vervolgens glycolaldehyde werd energetisch voorkeursmatig.
Een nieuwe hefboom voor schonere chemische productie
In gewone bewoordingen laat dit werk zien dat "waar" elk nikkelatoom zit op een oppervlak van nanometerschaal kan bepalen "wat" methanol wordt wanneer het door licht wordt beschenen. Door te schakelen tussen enkele atomen en kleine nikkelclusters kunnen de onderzoekers het hoofdproduct laten omslaan van ethyleenglycol naar glycolaldehyde, beide efficiënt en schoon gemaakt samen met waterstofbrandstof. Deze strategie van katalysatoren atomair opbouwen biedt een veelbelovende route om eenvoudige, hernieuwbare grondstoffen zoals methanol te upgraden naar een reeks nuttige chemicaliën zonder afhankelijk te zijn van aardolie, harde condities of afvalvolle nevenreacties.
Bronvermelding: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Trefwoorden: methanol-upcycling, fotokatalyse, nikkel single-atomen, ethyleenglycol, glycolaldehyde