Clear Sky Science · nl
Exon-inclusiesignaturen maken nauwkeurige schatting van splicingfactoractiviteit mogelijk
De verborgen redactieaantekeningen van de cel lezen
Elke cel in ons lichaam bewerkt voortdurend zijn RNA-boodschappen voordat die in eiwitten worden omgezet. Deze bewerking, splitsing genoemd, helpt bepalen of een cel gezond blijft of kankercellig wordt. De studie achter dit artikel laat zien dat wetenschappers door zorgvuldig te kijken welke RNA-delen worden behouden of overgeslagen — zogenaamde exon-inclusiesignaturen — de activiteit van de moleculaire "redacteuren" die splitsing aansturen nauwkeurig kunnen afleiden, zelfs in complexe aandoeningen zoals kanker.
Hoe cellen hun boodschappen knippen en plakken
Genen worden niet in één doorlopende reeks afgelezen. Cellen verwijderen in plaats daarvan niet-coderende segmenten en naaien coderende stukken, bekend als exonen, aan elkaar om de uiteindelijke RNA-boodschappen te vormen. Gespecialiseerde eiwitten, splicingfactoren genoemd, begeleiden dit knip-en-plakproces en beslissen welke exonen worden opgenomen. Hun gedrag wordt beïnvloed door vele lagen van regulatie: hoeveel van hun eigen RNA en eiwit wordt geproduceerd, hoe ze chemisch worden aangepast, waar ze zich in de cel bevinden en hoe ze met andere eiwitten interageren. Omdat zoveel hendels het gedrag van splicingfactoren kunnen veranderen, is het meten van slechts één type data — zoals genexpressie — vaak niet genoeg om te onthullen wat deze factoren werkelijk doen.
Exonpatronen omzetten in activiteitsmetingen
Geïnspireerd door eerder werk aan transcriptiefactoren, stellen de auteurs een andere strategie voor: in plaats van te proberen splicingfactoren direct te meten, lezen ze hun activiteit af uit hun effecten. Wanneer een splicingfactor verandert, verschuift de inclusie van zijn target-exonen in herkenbare patronen. Het team verzamelde honderden experimenten waarin individuele splicingfactoren werden onderdrukt, uitgeschakeld of overgeëxprimeerd, en gebruikte deze gegevens om "empirische netwerken" op te bouwen die elke factor koppelen aan de exonen die hij duidelijk beïnvloedt. Vervolgens pasten ze een computationeel kader genaamd VIPER aan om een nieuwe exon-inclusiesignatuur te lezen en te scoren hoe actief elke splicingfactor moet zijn om het waargenomen patroon te verklaren.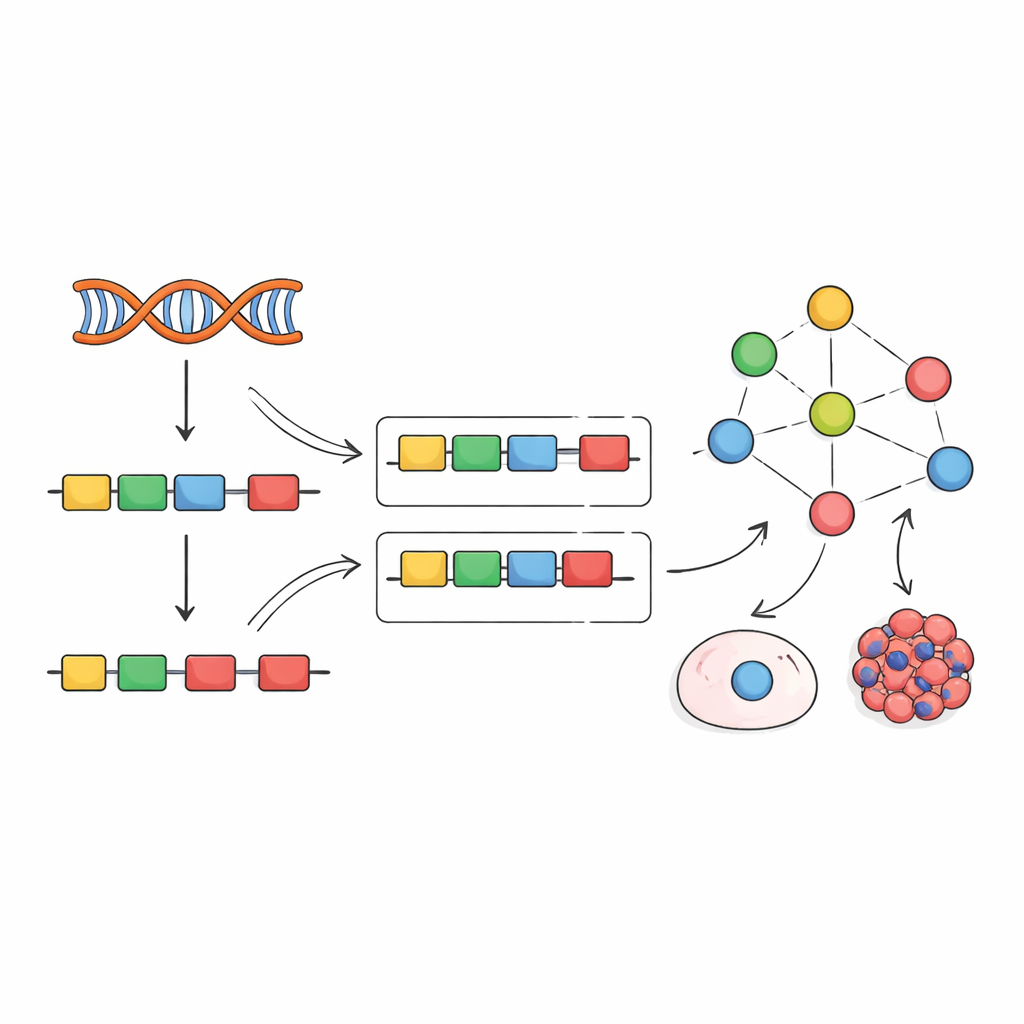
De methode testen in realistische verstoringen
Om te kijken of deze benadering werkt, evalueerden de onderzoekers verschillende manieren om netwerken op te bouwen en activiteitscores te berekenen. Empirische netwerken, rechtstreeks afgeleid van perturbatie-experimenten en gecombineerd met VIPER’s enrichmentsanalyse, presteerden duidelijk beter dan alternatieven die alleen op statistische inferentie waren gebaseerd. De methode identificeerde in de meeste tests correct welke splicingfactor experimenteel was verstoord, zelfs tussen verschillende celtypen en studies. Ze pakte ook subtielere regelmechanismen op. Zo veroorzaakt een kankergeneesmiddel genaamd Indisulam de afbraak van het splicingfactoreiwit RBM39 terwijl het RBM39-RNA omhooggaat in wat lijkt op een compensatiepoging. Traditionele expressieanalyse zou misleidend suggereren dat RBM39 actiever is, maar de exon-gebaseerde activiteitsscore toonde terecht een sterk functieverlies, in overeenstemming met de bekende werking van het geneesmiddel.
Verborgen splicingprogramma’s in kanker blootleggen
Met dit gereedschap richtten de auteurs zich op The Cancer Genome Atlas en analyseerden exonniveaugegevens van meerdere tumortypen en overeenkomende gezonde weefsels. Ze ontdekten twee brede en terugkerende splicingprogramma’s. Het ene programma bestaat uit splicingfactoren die in tumoren doorgaans actiever zijn en geassocieerd zijn met slechtere overleving van patiënten — een oncogeen-achtig programma. Het andere omvat factoren die systematisch minder actief zijn in tumoren en gekoppeld zijn aan betere uitkomsten, wat doet denken aan tumorrepressoren. Deze programma’s beïnvloeden genen die betrokken zijn bij fundamentele kankerkenmerken zoals snelle celdeling en het vermogen van tumoren om aan het immuunsysteem te ontsnappen. Bijvoorbeeld, sommige exonen die door het tumorrepressor-achtige programma worden gereguleerd, lijken te beïnvloeden hoe goed patiënten reageren op immuuncheckpointherapieën, wat wijst op nieuwe markers of interventiepunten.
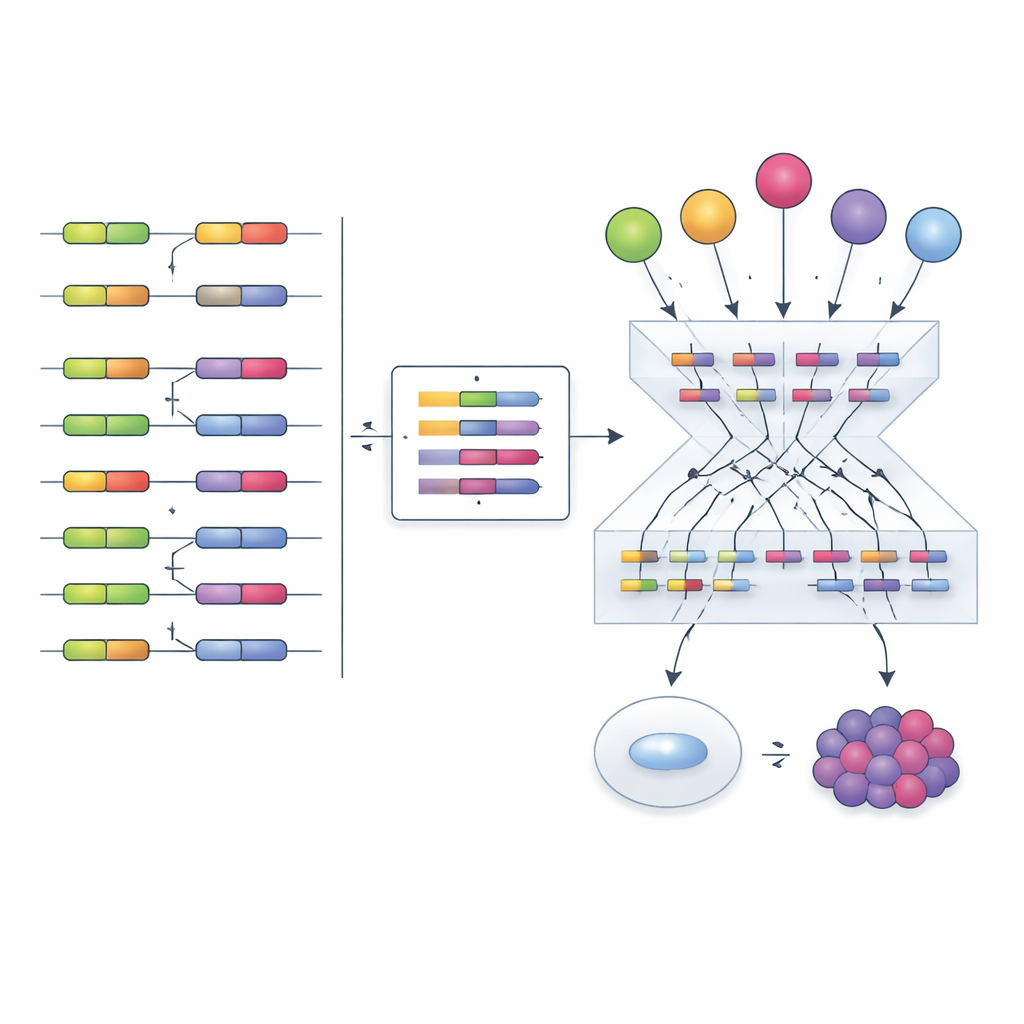
Splicingveranderingen volgen op weg naar kanker
Het team onderzocht ook een stapsgewijs model van menselijke cellen die zich ontwikkelen van normaal naar geïmmortaliseerd, tumormvormend en uiteindelijk metastaserend. Ze vonden dat het oncogeen-achtige splicingprogramma actiever wordt naarmate cellen kankerbevorderende mutaties verwerven, terwijl het tumorrepressor-achtige programma vervaagt. Door meerdere datalagen te integreren — RNA-niveaus, eiwitabundantie, chemische modificaties en splicingveranderingen binnen de splicingfactoren zelf — identificeerden ze een gerichte set kandidaat-moleculaire gebeurtenissen die deze programverschuivingen kunnen aansturen, en boden ze een geprioriteerde lijst voor toekomstige experimentele tests.
Waarom dit belangrijk is voor patiënten en toekomstig onderzoek
In wezen toont de studie aan dat het complexe gedrag van splicingfactoren kan worden teruggebracht tot een enkele, interpreteerbare activiteitscore, afgeleid uit hoe exonen worden opgenomen of overgeslagen. Dit maakt het mogelijk om splicingregulatie te bestuderen in grote patiëntengroepen en uiteenlopende experimenten met alleen standaard RNA-sequencinggegevens, zonder dure multi-omicsprofilering. Voor de niet‑specialist is de kernboodschap dat patronen in hoe genen worden geknipt en geplakt rijke informatie dragen over de verborgen controlesystemen van de cel, en dat het decoderen van deze patronen nieuwe kankerveroorzakers kan onthullen, de prognose kan verbeteren en het zoeken naar meer gerichte behandelingen kan sturen.
Bronvermelding: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Trefwoorden: RNA-splitsing, splicingfactoren, kanker-genomica, transcriptomica, eiwitactiviteitsinferentie