Clear Sky Science · nl
LOAd703-geïnduceerde genetische modulatie van het tumor-micro-omgeving in combinatie met atezolizumab bij gemetastaseerd kwaadaardig melanoom: een fase I/II-studie
Waarom deze nieuwe melanoomstudie ertoe doet
Voor mensen met gevorderd huidmelanoom dat niet meer reageert op de huidige krachtige immunotherapieën, zijn de behandelmogelijkheden beperkt en vaak zwaar. Deze studie onderzoekt een ander idee: een genetisch aangepast virus direct in tumoren injecteren, samen met een bestaande immuunversterkende geneesmiddel, om de afweer van het lichaam te activeren en weer controle over de kanker te krijgen. De vroege resultaten suggereren dat deze benadering veilig toegediend kan worden en mogelijk een aanzienlijk deel van de patiënten helpt van wie de ziekte eerder resistent was tegen de standaardzorg.
Een hardnekkige huidkanker die behandelingen slim ontwijkt
Melanoom is een van de meest voorkomende ernstige huidkankers in westerse landen, en de incidentie is de afgelopen decennia sterk gestegen. Moderne immuuncheckpointmiddelen — die de rem van T-cellen wegnemen — hebben de uitkomsten drastisch verbeterd en de vijfjaarsoverleving bij gevorderd melanoom voor ongeveer de helft van de patiënten verhoogd. Toch stoppen veel tumoren na verloop van tijd met reageren. Vaak zijn deze resistente kankers omgeven door een “koud” milieu van cellen en moleculen dat immuuncellen buiten houdt of uitzet. Het vinden van manieren om deze tumor-micro-omgeving te herbedraden zodat T‑cellen de kanker weer kunnen herkennen en aanvallen, is een belangrijke onderzoeksprioriteit.
Een virus ontworpen om het tumormilieu te herprogrammeren
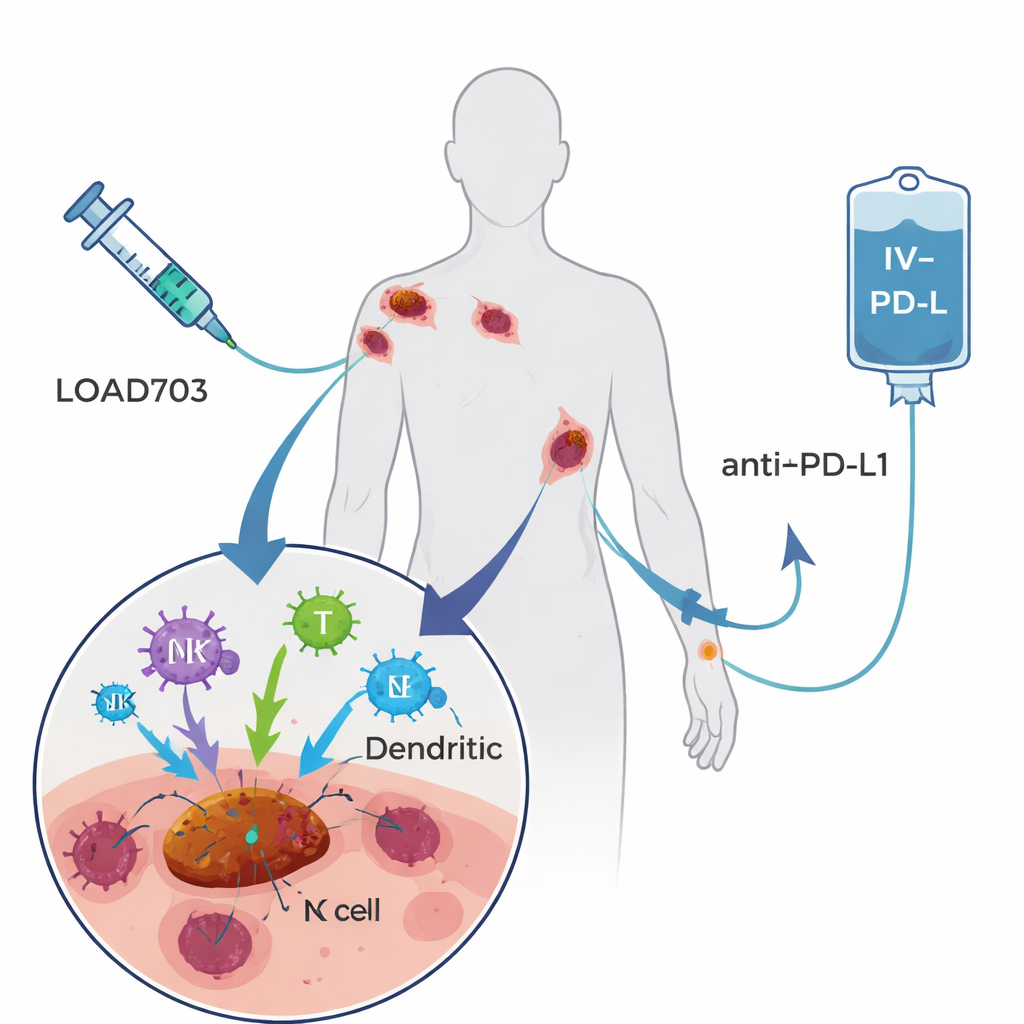
De hier geteste behandeling, LOAd703 genoemd, is een gemodificeerde adenovirus — een type verkoudheidsvirus — dat is geprogrammeerd om twee taken uit te voeren. Ten eerste heeft het de voorkeur om zich te vermeerderen in en tumorcellen te vernietigen, een strategie die bekendstaat als oncolytische virotherapie. Ten tweede draagt het genetische instructies voor twee krachtige immuunstimulerende signalen die op geïnfecteerde cellen worden geplaatst. Deze signalen, CD40L en 4-1BBL, helpen professionele immuunwachters (dendritische cellen) zich te rijpen en tumorfragmenten te presenteren, en versterken en breiden T‑cellen en natural killer-cellen uit die tegen kanker vechten. Patiënten in de trial kregen LOAd703 elke drie weken rechtstreeks in een of meer tumoren geïnjecteerd, samen met atezolizumab, een gevestigde antilichaamtherapie die via de ader wordt toegediend en de PD-L1-rem op T‑cellen blokkeert. De hoop was dat het virus tumoren in in‑het‑lichaam vaccinfabrieken zou veranderen, terwijl het antilichaam de hernieuwde T‑cellen actief zou houden.
Wie behandeld werd en hoe het hen verging
De fase I/II-trial schreef 24 mensen in met stadium IV-melanoom dat duidelijk was voortgeschreden ondanks ten minste één eerdere PD‑1-remmende behandeling; velen hadden meerdere lijnen van immunotherapie en gerichte middelen gekregen. Er werden twee virusdoseringen getest. Over het geheel genomen werd de combinatie goed verdragen. De meest voorkomende bijwerkingen die aan het virus werden gekoppeld — koorts, rillingen, misselijkheid en griepachtige symptomen — waren meestal mild en van tijdelijke aard. Slechts twee patiënten kregen ernstigere maar omkeerbare reacties bij de hogere dosis, en niemand hoefde de behandeling te staken vanwege virusgerelateerde problemen. Bij het beoordelen van tumorresponses hadden vier patiënten (17%) meetbare krimp van hun tumoren, en meer dan de helft had gedurende enige tijd ten minste stabiele ziekte. Twee jaar na deelname aan de studie waren bijna de helft van de deelnemers nog in leven, inclusief enkele wiens scans langdurige controle of volledige verdwijning van detecteerbare ziekte lieten zien na het beëindigen van de therapie.
Signalen dat het immuunsysteem opnieuw werd geactiveerd
Om te zien wat er in tumoren en in het bloed gebeurde, analyseerde het team weefselbiopten en bloedmonsters die vóór de behandeling en ongeveer negen weken na aanvang werden genomen. In de geïnjecteerde tumoren zagen ze een hogere activiteit van genen die gelinkt zijn aan type‑1 immuunresponsen, inclusief merkers van geactiveerde T‑cellen en natural killer‑cellen, en moleculen die deze cellen helpen de tumoren vanuit nabijgelegen bloedvaten binnen te komen. Signalen geassocieerd met antigeenpresentatie — het proces waarbij tumorfragmenten aan T‑cellen worden getoond — namen ook toe, wat suggereert dat de virale therapie de tumor-micro-omgeving van onderdrukkend naar meer immuunvriendelijk aan het veranderen was. In het bloed stegen verschillende immuungerelateerde eiwitten, inclusief PD‑L1 zelf, na de therapie, wat consistent is met een brede activering van immuunroutes. Patiënten die langer overleefden, vertoonden vaker genpatronen die horen bij robuuste T‑cel functies en antivirale bescherming, terwijl degenen met kortere overleving patronen lieten zien die geassocieerd zijn met onderdrukkende celtypen en signalen voor weefselherschikking.
Wat dit kan betekenen voor toekomstige zorg
Dit was een kleine, eenarmige studie zonder controlegroep, dus de overlevings- en responderende cijfers moeten voorzichtig worden geïnterpreteerd. Desondanks wijzen de combinatie van goede verdraagbaarheid, immuunactivatie in tumoren en bemoedigende ziektecontrole bij sterk voorbehandelde patiënten erop dat genetisch gemodificeerde oncolytische virussen zoals LOAd703 kunnen helpen om melanoom opnieuw gevoelig te maken voor checkpointremming — of zelfs tumoren op zichzelf onder controle te houden. De resultaten ondersteunen grotere, gecontroleerde trials, mogelijk door het virus te combineren met aanvullende immuungerichte middelen, om te verduidelijken welke patiënten het meest profiteren en hoe deze strategie het beste in de behandeling van melanoom kan worden geïntegreerd.
Bronvermelding: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Trefwoorden: melanoom, immunotherapie, oncolytisch virus, tumor-micro-omgeving, resistentie tegen remmers van controlepunten