Clear Sky Science · nl
Op drug ingekapselde medicijnen stellen fotokatalytische dubbele ontgrendeling van stikstofmonoxide en verdovende middelen mogelijk voor antibacteriële analgesie
Germ bestrijden en pijn tegelijk
Bacteriële infecties vormen niet alleen een bedreiging voor onze gezondheid; ze doen ook pijn—en veel. Standaardbehandelingen richten zich meestal op de ziekteverwekkers, terwijl patiënten aangewezen blijven op afzonderlijke pijnstillers die snel kunnen uitgewerkt raken of bijwerkingen veroorzaken. Deze studie introduceert een lichtgestuurd middel dat erop gericht is bacteriën te doden en pijn in één gecoördineerde stap te verlichten, en biedt daarmee een voorproefje van slimmer en comfortabeler infectiezorg.
Een idee voor een twee-in-één geneesmiddel
De onderzoekers baseerden hun aanpak op tetracaïne, een bekend plaatselijk verdovingsmiddel dat wordt gebruikt om huid en zenuwen te verdoven. Ze hechtten chemisch stikstofmonoxide, een klein gasmolecuul dat bekendstaat om zijn sterke antibacteriële en ontstekingsremmende werking, aan tetracaïne. Zo ontstond een “prodrug” genaamd TTC-NO die grotendeels inactief is totdat hij wordt geactiveerd. TTC-NO werd vervolgens samen met een lichtgevoelige hulpstof ingepakt in kleine polaire bolletjes, micellen genoemd, die zich in waterige omgevingen zoals bloed of weefselvloeistof kunnen verplaatsen. 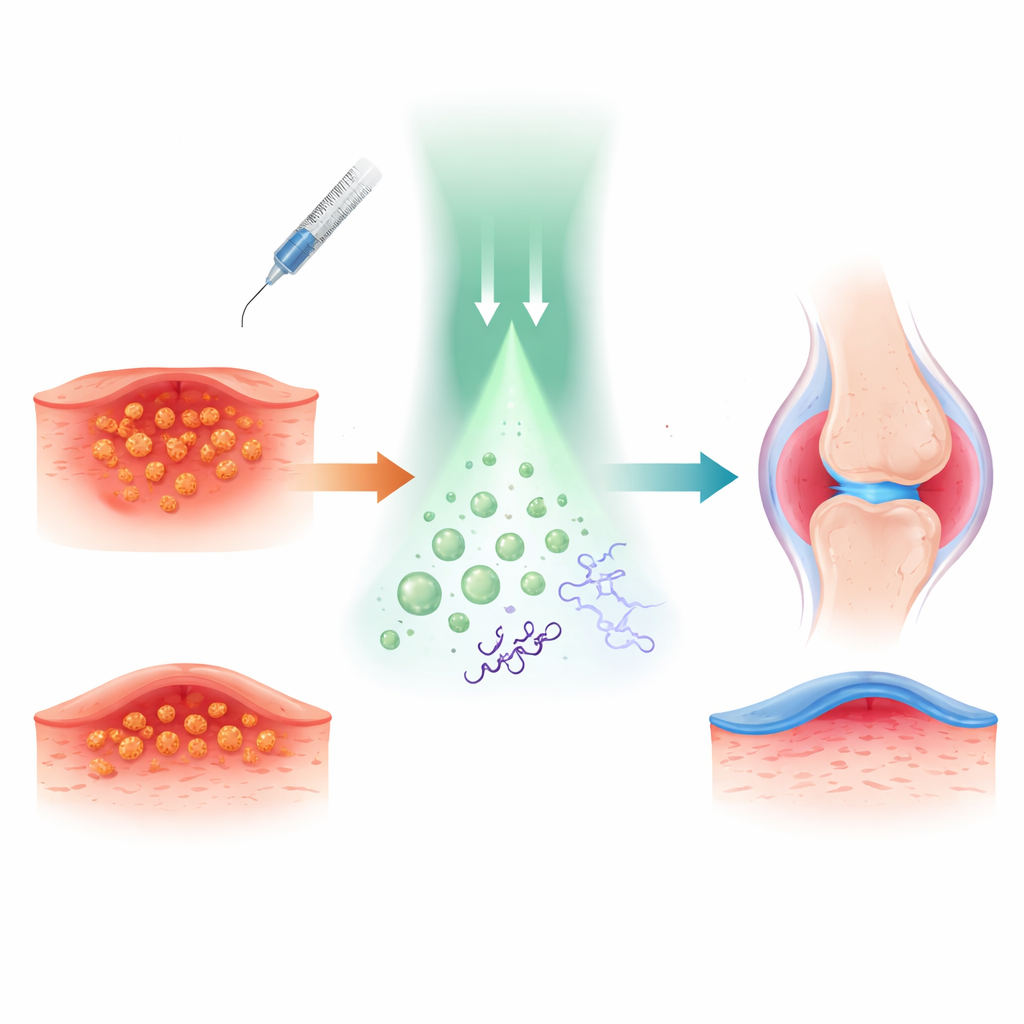
Het middel inschakelen met zacht licht
Om te begrijpen hoe deze lichtschakelaar werkt, bestudeerde het team de chemie in oplossing. Ze toonden aan dat een fotokatalysator op basis van iridium een elektron kan overdragen aan TTC-NO wanneer deze met groen licht wordt beschenen. Dit verzwakt een specifieke binding, waardoor stikstofmonoxide vrijkomt en tetracaïne terugkeert naar zijn actieve vorm. Metingen met spectroscopie en chromatografie bevestigden dat TTC-NO onder deze omstandigheden vrijwel volledig wordt omgezet in tetracaïne en stikstofmonoxide, terwijl het in het donker nagenoeg onveranderd blijft. Wanneer beide componenten in micellen waren ingekapseld, bleven de deeltjes stabiel, ongeveer 80 nanometer in diameter, en gaven ze alleen hun inhoud vrij bij bestraling, wat aantoont dat het concept van een “drug-caged drug” van buiten het lichaam met licht te regelen is.
Geïnfecteerde wonden sneller laten genezen
Het team ging vervolgens verder met muizen met huidwonden die opzettelijk waren geïnfecteerd met methicilline-resistente Staphylococcus aureus (MRSA), een vervelende ziekenhuisbacterie. Sommige wonden kregen standaardbehandelingen zoals een antibioticum of een groeifactor, terwijl andere werden behandeld met de TTC-NO-micellen, met of zonder licht. Wanneer het licht werd ingeschakeld, verminderde het TTC-NO-systeem het aantal bacteriën sterk, dempte het de ontsteking, stimuleerde het de groei van nieuwe bloedvaten en bevorderde het collageenvorming—allemaal essentieel voor goed herstel. Wonden die op deze manier werden behandeld, sloten sneller en vollediger dan die welke alleen tetracaïne of micellen in het donker kregen, en hun effectiviteit was vergelijkbaar met een eerstekeuzepenicilline. Belangrijk is dat veiligheidscontroles geen wezenlijke schade aan organen of bloedchemie lieten zien.
Pijn verlichten en zenuwsignalen kalmeren
Omdat infectie en weefselschade pijnbanen sterk activeren, maten de onderzoekers zorgvuldig pijngerelateerd gedrag in hetzelfde wondmodel. Traditionele tetracaïne verhoogde tijdelijk de kracht die nodig is om een pijnreactie teweeg te brengen, maar werkte slechts enkele uren. Daarentegen bood TTC-NO in micellen, geactiveerd door licht, verlichting tot wel 12 uur. Microscopisch onderzoek van zenuwklusters nabij het ruggenmerg en activiteitsopnamen in de sensorische cortex van de hersenen toonden dat de gecombineerde behandeling het vuren van pijngevoelige neuronen dempte, lang nadat pure tetracaïne zijn effect had verloren. Verdere experimenten suggereerden dat de langere werkingsduur voortkomt uit het verminderen van de bacteriële last en ontsteking door stikstofmonoxide, en niet alleen uit het verdoven van de zenuwen.
Pijnlijke geïnfecteerde gewrichten beschermen
De onderzoekers testten het systeem ook bij muizen met septische artritis, een ernstige MRSA-infectie in het kniegewricht die zwelling, botverlies en hevige pijn veroorzaakt. Lichtgeactiveerde TTC-NO-micellen verminderden de gewrichtsbreedte, verlaagden het aantal bacteriën en beschermden de botstructuur zoals zichtbaar in hoogresolutie-scans. De niveaus van schadelijke ontstekingsmoleculen in het bloed daalden, terwijl beschermende signaalmoleculen toenamen. Behavioristisch konden behandelde muizen sterkere mechanische druk op de getroffen poot verdragen en bewogen ze vrijer in een open arena, opnieuw met langdurigere verlichting dan alleen tetracaïne. Zenuw- en hersenmetingen weerspiegelden deze gedragsverbeteringen en wezen op een brede demping van pijnbanen zonder duidelijke lokale of systemische toxiciteit. 
Wat dit voor patiënten zou kunnen betekenen
Samengevat toont het werk een enkel lichtgeactiveerd nanosysteem dat zowel hardnekkige bacteriële infecties kan opruimen als de bijbehorende pijn aanzienlijk kan verminderen. Door een verdovingsmiddel chemisch te "cagen" binnen een structuur die stikstofmonoxide afgeeft en het in micellen te verpakken, bereiken de auteurs een op aanvraag en gelokaliseerde vrijgave van twee nuttige middelen met behulp van mild zichtbaar licht. In diermodellen van huidwonden en gewrichtsinfecties versnelt dit ontwerp de genezing en verlengt het de pijnverlichting voorbij wat een conventioneel plaatselijk verdovingsmiddel kan bieden. Hoewel er nog veel tests nodig zijn voordat toepassing bij mensen mogelijk is, benadrukt de studie hoe slimme, omschakelbare geneesmiddelen infectiebehandelingen in de toekomst zowel effectiever als comfortabeler kunnen maken.
Bronvermelding: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Trefwoorden: stikstofmonoxide-therapie, lichtgeactiveerde geneesmiddelen, antibacteriële analgesie, nanogeneeskunde, MRSA-infecties