Clear Sky Science · nl
T-cellen die gericht zijn op het Dickkopf-1–A2-complex kunnen worden gebruikt om HLA-A2+ solide en hematologische kankers te behandelen
Nieuwe hoop voor moeilijk behandelbare kankers
Veel krachtige nieuwe immunotherapieën werken goed bij bloedkankers, maar stuiten op problemen bij solide tumoren zoals alvleesklier-, long- en borstkanker. Deze studie introduceert een speciaal ontworpen T‑cel die zich richt op een moleculaire “vlag” die op een breed scala aan kankers voorkomt maar grotendeels afwezig is in normale weefsels, en opent daarmee de mogelijkheid voor één behandeling die zowel bloed- als solide tumoren veilig kan aanvallen bij patiënten met een veelvoorkomend immuunprofiel.
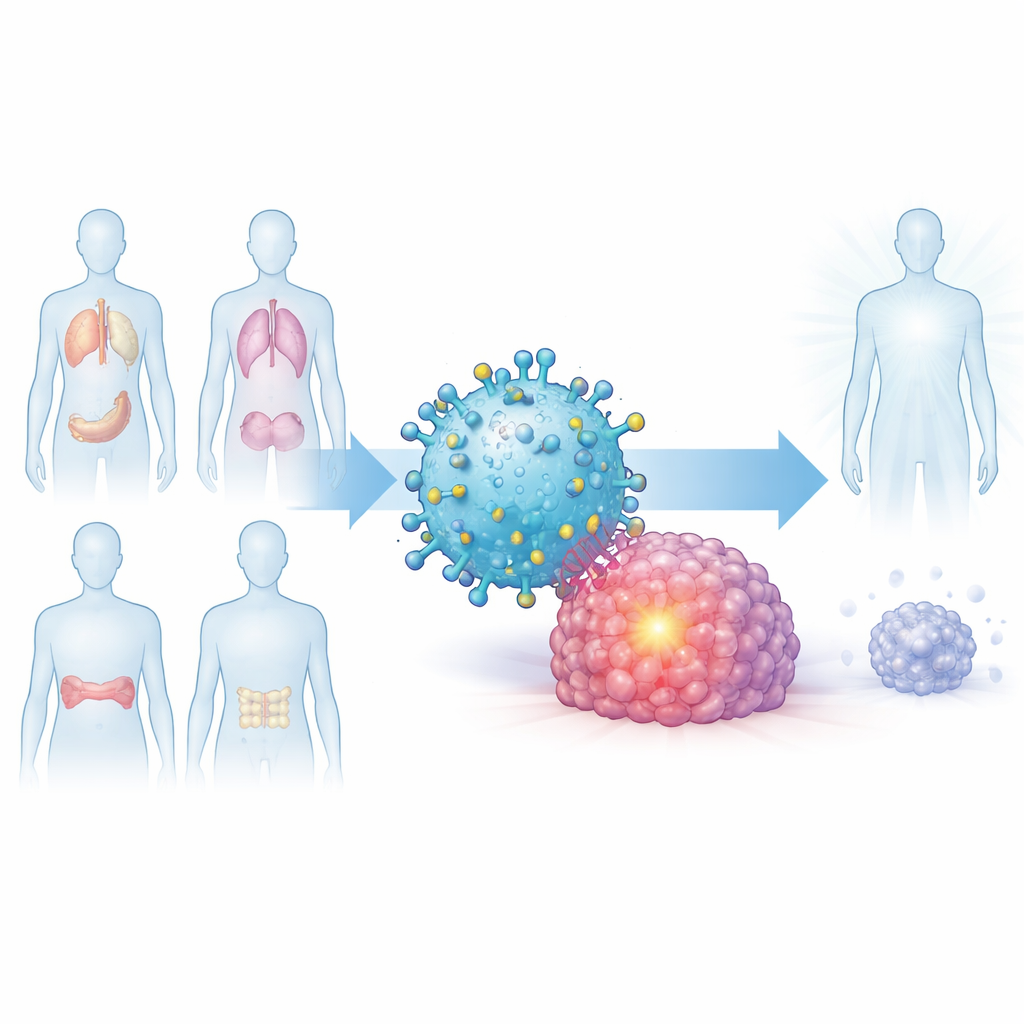
Een veelvoorkend signaal gedeeld door veel tumoren
De onderzoekers begonnen met de vraag of er een gedeelde moleculaire eigenschap is die in verschillende kankers verschijnt maar zelden in gezonde organen. Ze richtten zich op een eiwit genaamd Dickkopf-1, of DKK1, dat helpt bij het reguleren van groeisignalering en in hoge niveaus wordt aangetroffen bij multipel myeloom, alvleesklierkanker, longkanker en agressieve triple-negatieve borstkanker. Door grote openbare genbanken te doorzoeken en tumorstalen te onderzoeken, lieten ze zien dat DKK1 veel overvloediger is in veel tumoren dan in bijbehorende normale weefsels, en dat patiënten van wie de tumoren meer DKK1 maken vaak een slechtere overleving hebben.
Een tumordoekje veranderen in een precies doelwit
Aangezien DKK1 normaal gesproken buiten cellen circuleert, is het niet meteen een evidente greep voor T‑cellen, die korte eiwitsnippers herkennen die door HLA-moleculen aan het celoppervlak worden gepresenteerd. Eerder werk had een korte DKK1-fragment geïdentificeerd dat wordt weergegeven door een zeer veelvoorkomend HLA-type dat bekend staat als HLA‑A2. Het team had al een antilichaam, genoemd C2, ontwikkeld dat dit DKK1-fragment herkent wanneer het door HLA‑A2 op het tumoroppervlak wordt gehouden, maar niet op de meeste gezonde cellen. In de huidige studie bouwden ze een chimerische antigeenreceptor (CAR) met het herkenningsdeel van dit antilichaam, gekoppeld aan interne T‑celsignaleringscomponenten, zodat gewone T‑cellen kunnen worden geherprogrammeerd om het DKK1–HLA‑A2‑combinatie te herkennen, aangeduid als het DKK1‑A2‑complex.
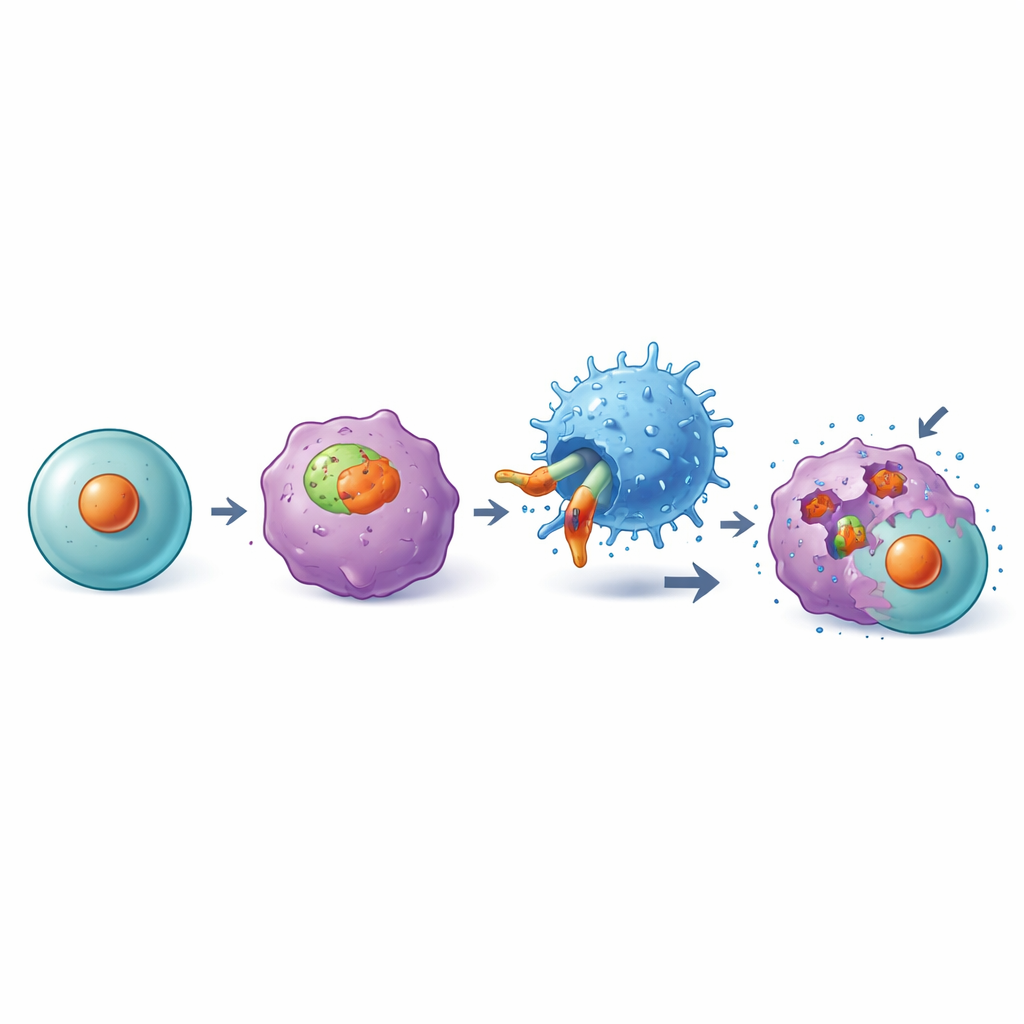
Gemanipuleerde T‑cellen die tumoren opsporen en vernietigen
De wetenschappers testten deze DKK1‑A2 CAR‑T‑cellen vervolgens tegen een breed paneel menselijke kankercellijnen in het laboratorium, waaronder cellen van multipel myeloom, alvleesklier, long en triple-negatieve borstkanker. Telkens wanneer tumorcellen zowel DKK1 als HLA‑A2 toonden, vermenigvuldigden de gemodificeerde T‑cellen zich krachtig, gaven ze krachtige immuunsignalen af en doodden ze de kankercellen efficiënt. Wanneer DKK1 uit de tumorcellen werd verwijderd of wanneer cellen HLA‑A2 misten, vielen de CAR‑T‑cellen niet meer aan, wat aantoont dat hun activiteit zeer specifiek is voor het beoogde doelwit.
Effectiviteit aantonen in levende modellen
Om te onderzoeken of deze benadering gevestigde kankers in levende organismen kon verkleinen, gebruikte het team meerdere muismodellen met menselijke tumoren. DKK1‑A2 CAR‑T‑cellen controleerden of elimineerden multipel myeloom dat in het beenmerg groeide, alvleeskliertumoren die in de alvleesklier waren geïmplanteerd, longkanker die zich via de bloedbaan had verspreid en agressieve borstkankers, terwijl standaard CD19‑gerichte CAR‑T‑cellen die als controle werden gebruikt weinig effect hadden. De therapie werkte ook tegen tumoren gekweekt uit echte patiënten‑alvleesklierkankers die in muizen werden getransplanteerd, wat de menselijke ziekte beter nabootst. Een gehumaniseerde versie van de CAR, ontworpen voor klinisch gebruik, liet nog betere langdurige controle zien, deels omdat deze T‑cellen een geheugenachtige toestand aannamen waardoor ze bleven bestaan en opnieuw konden reageren wanneer tumoren terugkeerden.
Veiligheidscontroles op gezond bloed en organen
Elke gerichte therapie moet gezonde weefsels sparen. De auteurs kleurden daarom tientallen soorten normaal menselijk weefsel en vonden dat, afgezien van de amandelen, het DKK1‑A2‑complex praktisch afwezig was. In laboratoriumtests beschadigden de DKK1‑A2 CAR‑T‑cellen geen bloed‑ of beenmergcellen van gezonde HLA‑A2‑positieve donoren, in tegenstelling tot CD19 CAR‑T‑cellen die, voorspelbaar, normale B‑cellen vernietigden. In muismodellen die waren aangepast om menselijk DKK1 en HLA‑A2 tot expressie te brengen, raakten de nieuwe CAR‑T‑cellen geen belangrijke bloedcelpopulaties of bloedplaatjes kwijt en veroorzaakten ze minder tekenen van gevaarlijke cytokinerelases dan sommige bestaande CAR‑ontwerpen, wat wijst op een gunstig veiligheidsprofiel.
Wat dit voor patiënten zou kunnen betekenen
Samengevat wijzen de bevindingen erop dat het DKK1‑A2‑complex een veelbelovend “midden‑in‑het‑vizier” is dat op veel moeilijk behandelbare kankers verschijnt maar grotendeels afwezig blijft in normale weefsels. Met DKK1‑A2 uitgeruste T‑cellen konden diverse tumoren herkennen en vernietigen in preklinische modellen, met beperkte toxiciteit. Als deze resultaten zich vertalen naar mensen, zou deze benadering een nieuwe, gedeelde immunotherapie kunnen bieden voor patiënten met HLA‑A2‑positief multipel myeloom, alvleesklier-, long- en bepaalde borstkankers, waarmee de reikwijdte van CAR‑T‑behandeling voorbij bloedkankers wordt uitgebreid naar solide tumoren.
Bronvermelding: Zhang, Y., Xiong, W., Qian, J. et al. T cells engineered against Dickkopf-1-A2 complex can be used to treat HLA-A2+ solid and hematologic cancers. Nat Commun 17, 2818 (2026). https://doi.org/10.1038/s41467-026-69621-8
Trefwoorden: CAR-T-celtherapie, DKK1, alvleesklierkanker, multipel myeloom, immunotherapie voor solide tumoren