Clear Sky Science · nl
Isolabele radicaal-kation en dication van dialumeen
Waarom dit aluminiumverhaal ertoe doet
Chemici zoeken voortdurend naar goedkopere, meer overvloedige metalen die de verfijnde taken kunnen uitvoeren die nu worden vervuld door edelmetalen zoals palladium of platina. Deze studie toont aan dat aluminium – een metaal dat bekender is van frisdrankblikjes en vliegtuigen – in ongewoon reactieve vormen kan worden gedwongen die zich een beetje gedragen als kleine elektronische schakelaars. Het begrijpen en beheersen van deze exotische aluminumspecies kan uiteindelijk helpen bij het ontwikkelen van nieuwe katalysatoren voor schonere chemische processen en materialen.
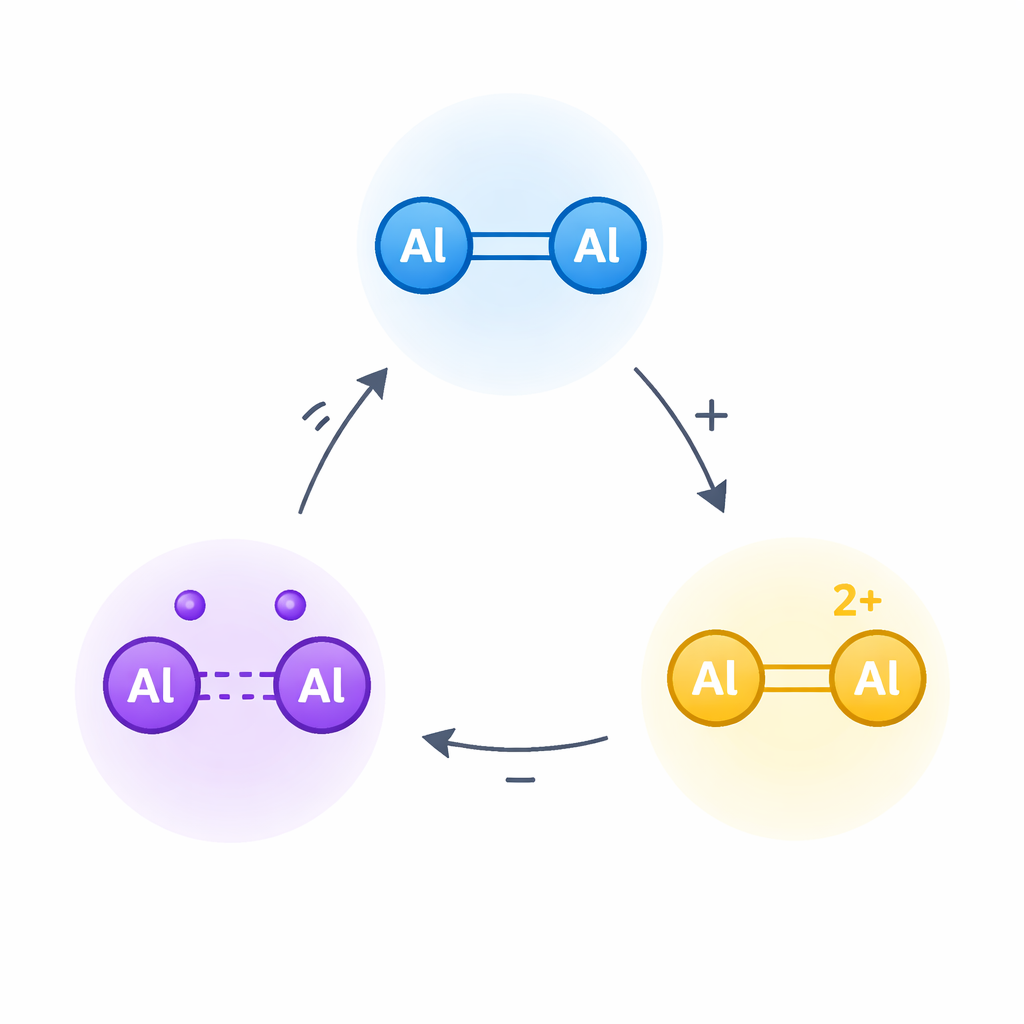
Een vertrouwde binding omzetten in een elektronische schakelaar
Het werk draait om dialumeen, een molecuul waarin twee aluminiumatomen een dubbele binding delen, enigszins vergelijkbaar met de koolstof–koolstof-dubbele binding in gewone alkenen. In organische moleculen kunnen zulke dubbele bindingen stapsgewijs worden geoxideerd tot radicaal-kationen en vervolgens dicationen — sterk geladen, zeer reactieve vormen die ten grondslag liggen aan veel reacties in de elektrochemie en materiaalkunde. De auteurs vroegen zich af of de aluminium–aluminium-dubbele binding in dialumeen door een vergelijkbare tweestapsoxidatie geduwd kon worden, ook al is aluminium sterk elektronegatiefontvankelijk en zouden dergelijk geladen soorten uitzonderlijk onstabiel moeten zijn.
Ontwerpen van een beschermend moleculair kader
Om deze reactiviteit te temmen, bouwde het team een dialumeen omgeven door volumineuze siliciumgebaseerde groepen en sterke elektrondonerende "carbene"-liganden. Deze werken als zachte bepantsering en elektronische kussens: ze beschermen de tere aluminium–aluminiumkern tegen ongewenste reacties en helpen waar nodig elektronendichtheid te leveren. Beginnend met dit neutrale dialumeen, aangeduid als 1, gebruikten ze zorgvuldig gekozen oxiderende middelen om eerst één elektron en vervolgens een tweede te verwijderen, waarmee een aluminium-gecentreerd radicaal-kation (2) en daarna een dication (3) werden gegenereerd. Röntgenkristallografie leverde momentopnames van alle drie toestanden, en liet zien hoe de aluminium–aluminiumbinding geleidelijk verlengt en van karakter verandert naarmate elektronen worden weggenomen.
Aantonen van een echte drieweg-redoxcyclus
Belangrijke metingen bevestigden dat het radicaal-kation werkelijk een ongepaard elektron draagt dat gecentreerd is tussen de twee aluminiumatomen, en niet op de omringende liganden. Electron paramagnetic resonance (EPR)-spectroscopie toonde een duidelijk signaal dat overeenkomt met één elektron gedeeld door beide aluminiumcentra. Computationele studies ondersteunden dit beeld en gaven aan dat het resterende bindingselektron een overwegend aluminium–aluminiumorbitaal bezet. Wanneer het tweede elektron wordt verwijderd om de dication te vormen, verzwakt de binding richting een enkelvoudige binding en hoopt positieve lading zich op bij het alumpaar. Belangrijk is dat de onderzoekers aantoonden dat al deze veranderingen omkeerbaar zijn: het teruggeven van elektronen met een reductans regenereert eerst het radicaal-kation en daarna het oorspronkelijke dialumeen, en het mengen van neutrale en tweevoudig geladen vormen levert via comproportionering het radicaal-kation op. Samen demonstreren deze reacties een robuuste, isoleerbare drietoestands-redoxcyclus op een eenvoudig aluminium–aluminium-eenheid.
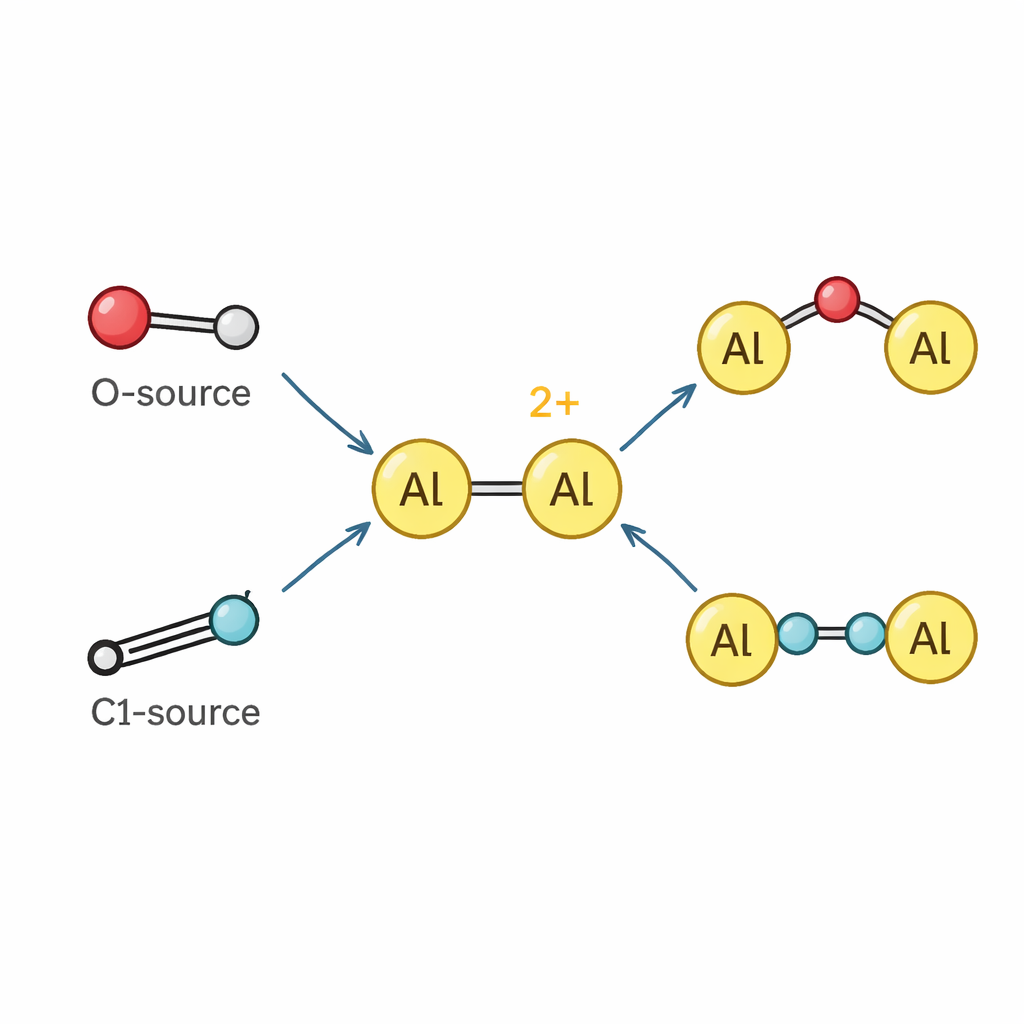
Aluminium laten optreden als een overgangsmetaal
Met de dication in handen onderzocht het team hoe deze reageert met andere moleculen. Doordat de aluminiumatomen sterk elektronarm zijn, gedraagt de dication zich als een krachtige Lewis-zuur en bindt gemakkelijk basische partners zoals pyridine en verwante moleculen om nieuwe dialuminiumcomplexen te vormen. Verder dan eenvoudige binding kan de dication chemische bindingen splijten en daarin inserteren. Het onttrekt zuurstofatomen uit distikstofmonoxide en pyridine N-oxide, en vormt stabiele species waarbij een zuurstofatoom de twee aluminiumcentra overbrugt of wordt opgenomen in een korte aluminium–zuurstof–siliciumketen die doet denken aan een klein fragment van een zeolietrooster. Het reageert ook met isocyaniden — kleine koolstof–stikstofeenheden gebruikt als een-atoom bouwstenen — om deze aan elkaar te koppelen tot langere N–C–C–N-fragmenten die tussen twee aluminiumatomen spannen, wat een zeldzaam voorbeeld laat zien van isocyanide "homologatie" aangedreven door een hoofdgroepkation.
Wat dit vooruit betekent
In alledaagse termen hebben de onderzoekers een aluminium–aluminiumbinding omgezet in een bestuurbare driepositionele elektronische schakelaar die kan worden geschakeld tussen neutrale, enkelvoudig geladen en tweevoudig geladen toestanden, elk met onderscheidende vormen en reactiviteiten. De tweevoudig geladen versie is bijzonder veelzijdig en onttrekt elektronen en kleine fragmenten uit andere moleculen op manieren die gewoonlijk worden geassocieerd met duurdere overgangsmetalen. Door te laten zien dat dergelijk gedrag mogelijk is met aluminium en dat de verschillende toestanden betrouwbaar wederzijds kunnen worden omgezet, opent dit werk de deur naar het ontwerpen van nieuwe, duurzame katalysatoren en functionele materialen opgebouwd uit een van 's werelds meest voorkomende metalen.
Bronvermelding: Liu, X., Kostenko, A., Körber, E. et al. Isolable radical cation and dication of dialumene. Nat Commun 17, 1937 (2026). https://doi.org/10.1038/s41467-026-69607-6
Trefwoorden: aluminiumkatalyse, redox-schakelbare moleculen, hoofdgroepchemie, radicaal-kationen, activatie van kleine moleculen