Clear Sky Science · nl
Treg-γδ T-cel-as bepaalt seksuele dimorfie in hepatocarcinogenese
Waarom sommige leverkankers mannen harder treffen
Artsen weten al lang dat leverkanker ongeveer tweemaal zo vaak mannen treft als vrouwen, maar de oorzaken reiken verder dan alleen verschillen in geslachtshormonen. Deze studie duikt in de immuuncellen die in levertumoren leven en onthult een verborgen wisselwerking tussen twee typen T-cellen die helpt verklaren waarom mannelijke levercellen kwetsbaarder zijn — en hoe deze kennis kan wijzen op nieuwe, meer gerichte behandelingen.
Het immunologische touwtrekken binnen levertumoren
Leverkanker, met name hepatocellulair carcinoom, groeit in een complex milieu van immuuncellen, bloedvaten en littekenweefsel. De auteurs vergeleken tumoren van mannen en vrouwen, zowel bij patiënten als in muismodellen, en vonden een opvallende onbalans: mannelijke tumoren zaten vol met meer regulatorische T-cellen, of Tregs, een celtype dat normaal helpt overmatige immuunreacties te dempen. Tegelijk waren de totale aantallen van andere veelvoorkomende T-cellen niet veel verschillend tussen de sexes. Omdat hoge Treg-niveaus geassocieerd waren met slechtere overleving, vermoedde het team dat deze cellen niet louter toeschouwers waren, maar actieve medeplichtigen die tumoren helpen ontsnappen aan immuunaanvallen. 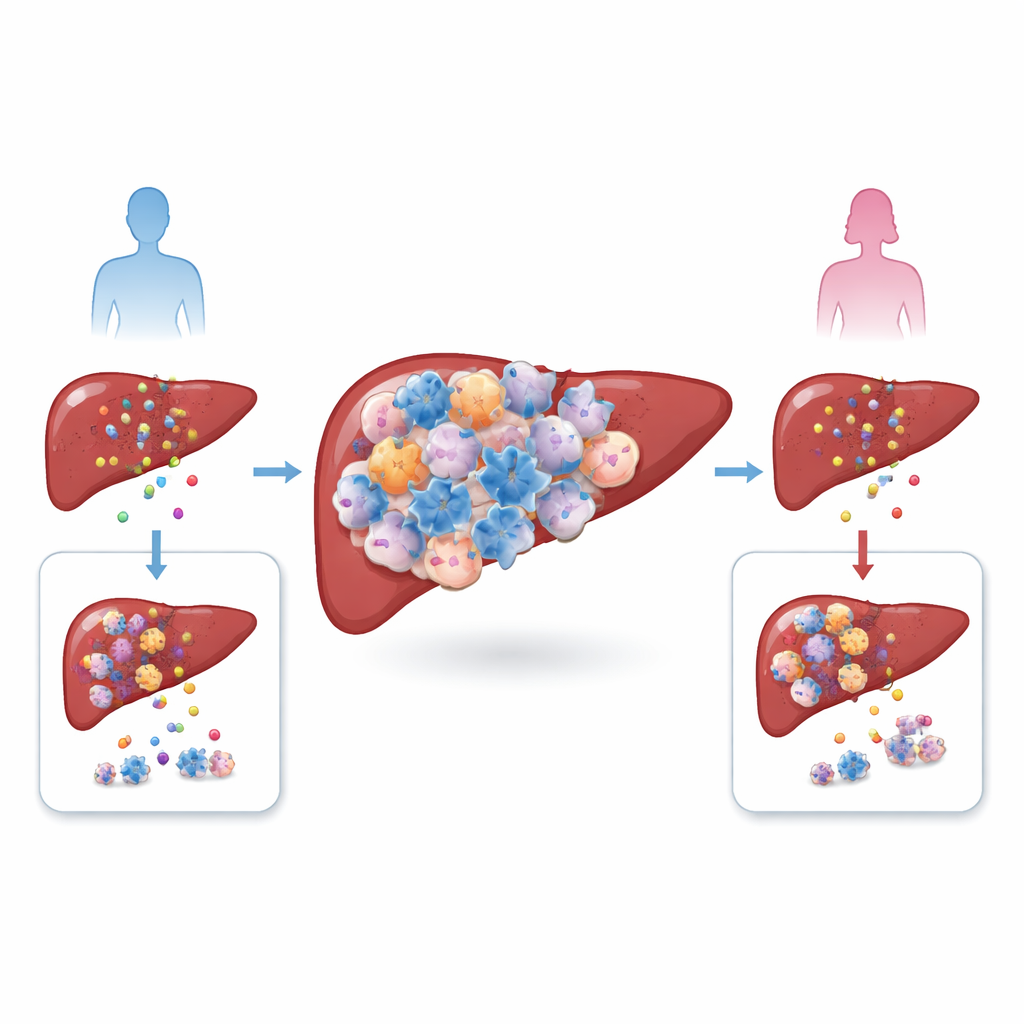
Hoe mannelijke hormonen onderdrukkende cellen binnenhalen
Om te begrijpen waarom mannelijke tumoren meer Tregs aantrekken, richtten de onderzoekers zich op chemische signalen die door kankercellen worden geproduceerd. Ze ontdekten dat mannelijke levertumoren grotere hoeveelheden van een molecuul genaamd Ccl2 produceerden, terwijl Tregs meer van de bijbehorende receptor, Ccr2, droegen. Deze koppeling werkt als een thuiszoekende baken en lokt Tregs de tumor in. Wanneer het Ccl2-signaal of de Ccr2-receptor in muizen werd verwijderd, krimpten tumoren en drongen veel minder Tregs de lever binnen, vooral bij mannelijke dieren. Het team toonde vervolgens aan dat testosteron, het belangrijkste mannelijke geslachtshormoon, dit proces aandrijft: het activeert een keten van eiwitten in leverkankercellen die het Ccl2-gen aanzet, waardoor de chemische oproep die Tregs aantrekt sterker wordt. Gecastreerde mannelijke muizen, die minder testosteron produceren, hadden lagere Ccl2-niveaus in hun tumoren en minder infiltrerende Tregs.
Waakcellen die kanker zouden kunnen bestrijden — maar worden geremd
Een ander T-celtype, bekend als gamma-delta T-cellen, kan fungeren als snelle “wachters” die tumorcellen herkennen en doden zonder het gebruikelijke antigeenpresentatiemechanisme. In een gezonde lever zijn deze cellen relatief schaars, maar in leverkanker kunnen ze krachtige tumorbestrijders zijn. De studie vond dat vrouwelijke tumoren meer van deze gamma-delta cellen bevatten en dat ze actiever waren en beter bewapend met toxische moleculen. Het verwijderen van mannelijke geslachtshormonen in muizen verhoogde het aantal en de bedrijvigheid van gamma-delta cellen in tumoren, terwijl klassieke dodelijke CD8-T-cellen grotendeels onveranderd bleven. In kweek schaadden gamma-delta cellen leverkankercellen gemakkelijk, maar dit effect werd verzwakt wanneer Tregs werden toegevoegd, wat suggereert dat Tregs deze veelbelovende antitumorpopulatie specifiek inbedden.
Hypoxie, geheime pakketjes en gesmoorde verdedigers
Dieper gravend vroegen de onderzoekers hoe Tregs erin slagen gamma-delta T-cellen te onderdrukken. Binnen tumoren is zuurstof vaak schaars, een toestand die hypoxie wordt genoemd. Onder deze lage-zuurstofomstandigheden begonnen Tregs in mannelijke tumoren grote hoeveelheden van een eiwit genaamd S100a4 te produceren. In plaats van direct als vrij molecuul te werken, werd S100a4 verpakt in kleine membraanomhulde deeltjes die bekendstaan als extracellulaire vesicles. Deze vesicles blonken af van Tregs en werden opgenomen door naburige gamma-delta T-cellen. Eenmaal binnen herschreef S100a4 de genetische regulatie van de cellen: het verminderde de openheid van DNA-regio's die sleutelgenen voor signaalgeving en doding regelen en verlaagde hun activiteit. De gamma-delta cellen werden minder in staat om te reageren via hun T-celreceptoren en minder bekwaam in het vrijgeven van toxische eiwitten en cytokinen, waardoor hun antikankerwerking effectief werd verdoofd. 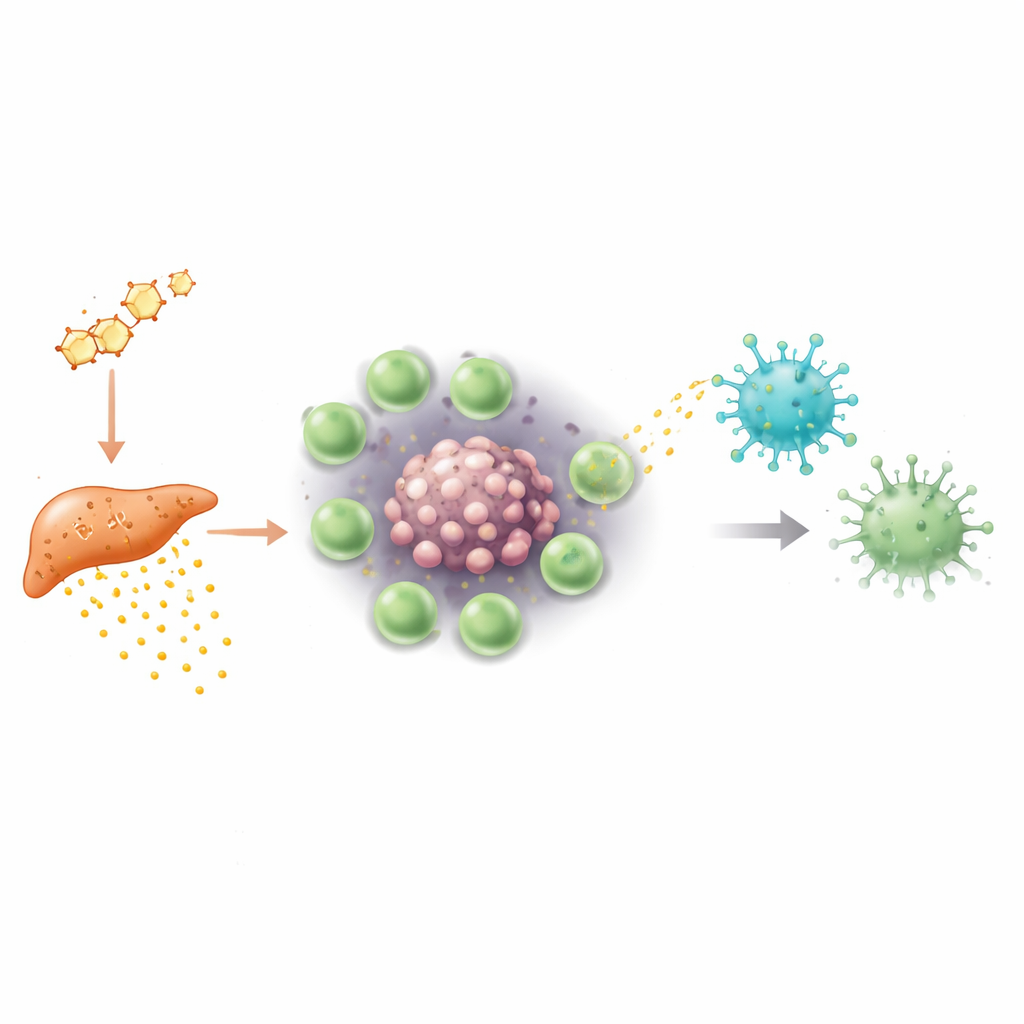
Het schadelijke circuit doorbreken
Tenslotte testte het team wat er gebeurt als deze Treg–S100a4–gamma-delta-as wordt onderbroken. In muizen die zo zijn geconstrueerd dat Tregs geen S100a4 kunnen maken, krimpten mannelijke levertumoren, daalde het totale S100a4-niveau in tumoren en werden gamma-delta T-cellen talrijker en actiever. Opmerkelijk was dat het aantal Tregs in de tumor niet daalde — alleen hun onderdrukkende effect op gamma-delta cellen werd opgeheven. Deze wijziging veegde bijna de gebruikelijke kloof in tumorernst tussen mannelijke en vrouwelijke muizen uit, wat benadrukt hoe centraal deze route is voor seksegebonden verschillen in leverkanker.
Wat dit betekent voor toekomstige behandelingen
In begrijpelijke bewoordingen laat de studie zien dat mannelijke hormonen leverkankercellen aansporen sterkere “welkomstsignalen” uit te zenden voor immuunsuppressieve Tregs. Eenmaal in de tumor — en onder de stress van lage zuurstof — verzenden deze Tregs S100a4-gevulde vesicles die stilletjes naburige gamma-delta T-cellen ontwapenen, die anders de kanker onder controle zouden kunnen houden. Door ofwel het Ccl2-signaal te blokkeren dat Tregs aantrekt, ofwel de S100a4-boodschappen te verhinderen die gamma-delta cellen stilleggen, zouden toekomstige therapieën de eigen verdedigingskracht van het lichaam kunnen herstellen, vooral bij mannen. Dit werk suggereert dat de behandeling van leverkanker baat kan hebben bij seksebewuste benaderingen en bij het benutten, in plaats van het negeren, van de unieke kwaliteiten van gamma-delta T-cellen.
Bronvermelding: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Trefwoorden: hepatocellulair carcinoom, regulatorische T-cellen, gamma-delta T-cellen, sekseverschillen, tumorimmunologie