Clear Sky Science · nl
Dubbele rekrutering van twee CCM2-moleculen naar KRIT1 onderdrukt KLF4-expressie
Waarom de bloedvaten in de hersenen zorgvuldig geregeld moeten worden
Bloedvaten in de hersenen moeten een nauwkeurig evenwicht bewaren: ze moeten stevig genoeg zijn om lekken te voorkomen, maar flexibel genoeg om op de behoeften van het lichaam te reageren. Wanneer dit evenwicht faalt, kunnen mensen cerebrale cavernomateuze malformaties ontwikkelen—clusters van kwetsbare, belachtige bloedvaten die kunnen bloeden en toevallen of beroertes veroorzaken. Deze studie onthult een eerder onbekende moleculaire handdruk tussen drie eiwitten die helpt hersenvaten stabiel te houden, en toont aan hoe het verbreken van die handdruk ziekte kan veroorzaken.
De poortwachters van vaatgezondheid
Cellen die bloedvaten bekleden vertrouwen op een reeks hoofdschakelaars, genoemd KLF2 en KLF4, om genen te reguleren die de sterkte en identiteit van vaten behouden. Als deze schakelaars te hoog worden aangezet, worden vaten abnormaal en gevoeliger voor schade. Twee andere eiwitten, KRIT1 en CCM2, staan bekend als bewakers van dit systeem. Mensen die erfelijke defecte versies van een van beide eiwitten hebben, lopen een hoog risico op cerebrale cavernomateuze malformaties. Tot nu toe begrepen wetenschappers echter niet precies hoe KRIT1 en CCM2 samenwerken om KLF4 te remmen.
Een verrassend trio
De onderzoekers gebruikten in het laboratorium gekweekte, op endotheel-achtige cellen lijkende menselijke cellen en verminderden selectief de hoeveelheid CCM2 of KRIT1 met genetische middelen. Wanneer een van beide eiwitten werd uitgeput, schoot het KLF4-niveau omhoog, in overeenstemming met wat in diermodellen en patiënten wordt gezien. Het herstellen van normale CCM2 of KRIT1 bracht KLF4 weer naar beneden—maar alleen als de herstelde eiwitten elkaar nog konden vasthouden. Door nauwkeurige wijzigingen aan te brengen in de regio’s waar CCM2 en KRIT1 op elkaar inwerken, toonde het team aan dat dit fysieke contact essentieel is om te voorkomen dat KLF4 stijgt. Deze experimenten plaatsen de KRIT1–CCM2-partnerschap stevig in het hart van het controlesysteem voor deze krachtige transcriptiefactor.
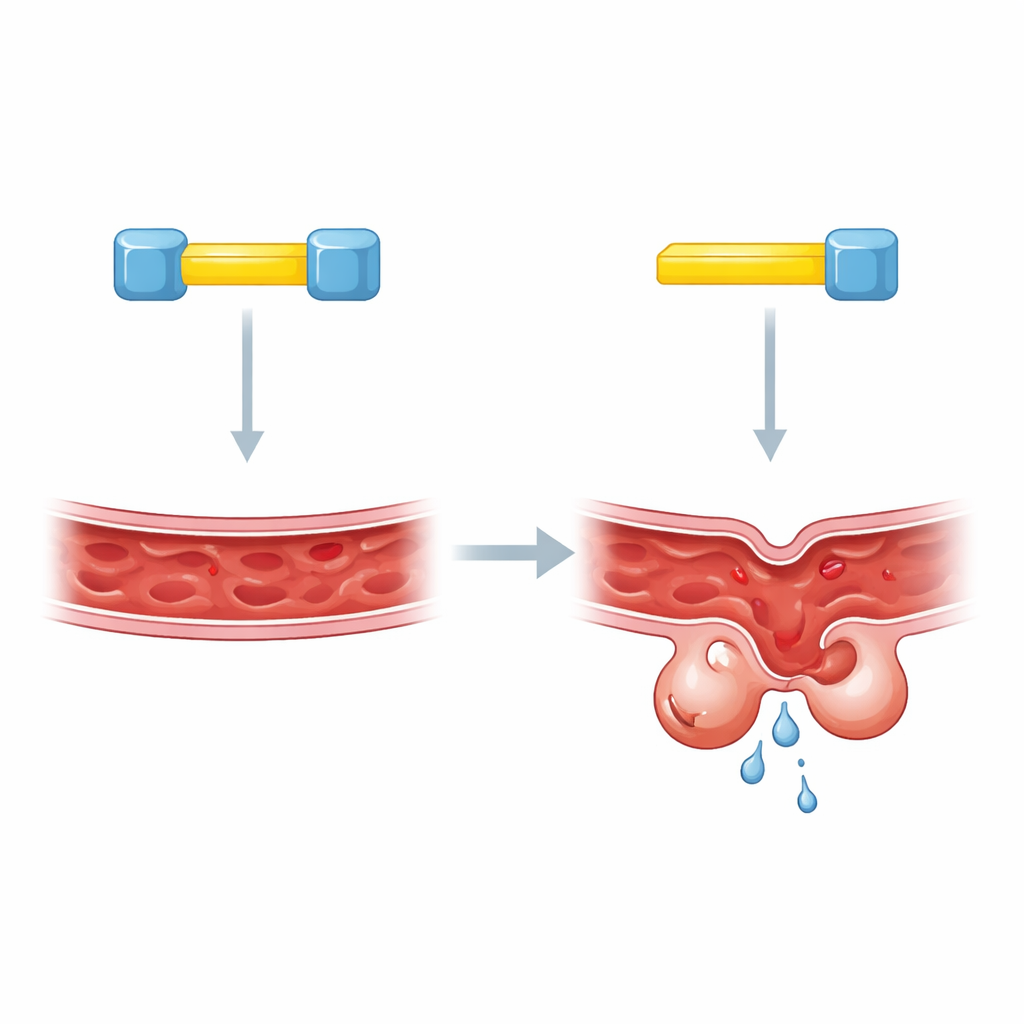
Twee sloten op één sleutel
Om dieper te graven richtten de auteurs zich op korte segmenten binnen KRIT1 die fungeren als moleculaire aanlegplaatsen. Eerder werk suggereerde dat CCM2 aan KRIT1 hecht op een van deze sites, maar verschillende methoden hadden tegenstrijdige antwoorden opgeleverd over welke dat was. De nieuwe studie laat zien dat de verwarring voortkwam uit een complexer beeld: KRIT1 draagt twee nabijgelegen aanlegplaatsen, en beide zijn nodig. Wanneer een van de segmenten werd verstoord, bleven de KLF4-waarden abnormaal hoog, alsof KRIT1 geheel ontbrak. Biochemische testen in geëngineerde cellen toonden aan dat één KRIT1-eiwit tegelijk twee afzonderlijke CCM2-moleculen kan overbruggen, wat wijst op een onverwachte driepartijenassemblage.
De moleculaire klem in detail bekijken
Het team zuiverde vervolgens de relevante delen van CCM2 en KRIT1 en onderzocht hoe ze samenkomen in oplossing en in kristallen. Metingen van de massa van het complex gaven aan dat twee kopieën van een sleutelregio van CCM2 binden aan één strook KRIT1 die de paar aanlegplaatsen draagt. Hoge-resolutie structurele snapshots bevestigden deze 2:1-structuur: een verlengd KRIT1-peptide rijgt zich tussen twee CCM2-domeinen, waarbij elke aanlegplaats in een vergelijkbare holte op een verschillend CCM2-molecuul past. Een kort helicaal segment tussen de aanlegplaatsen helpt de twee CCM2-domeinen naast elkaar te positioneren, waardoor een nauwsluitende, klemachtige structuur ontstaat. Dit type dubbele binding—twee bindingsdomeinen die zich vasthechten aan tandemplaatsen langs één partner—was voor deze familie van eiwitmodules nog niet beschreven.
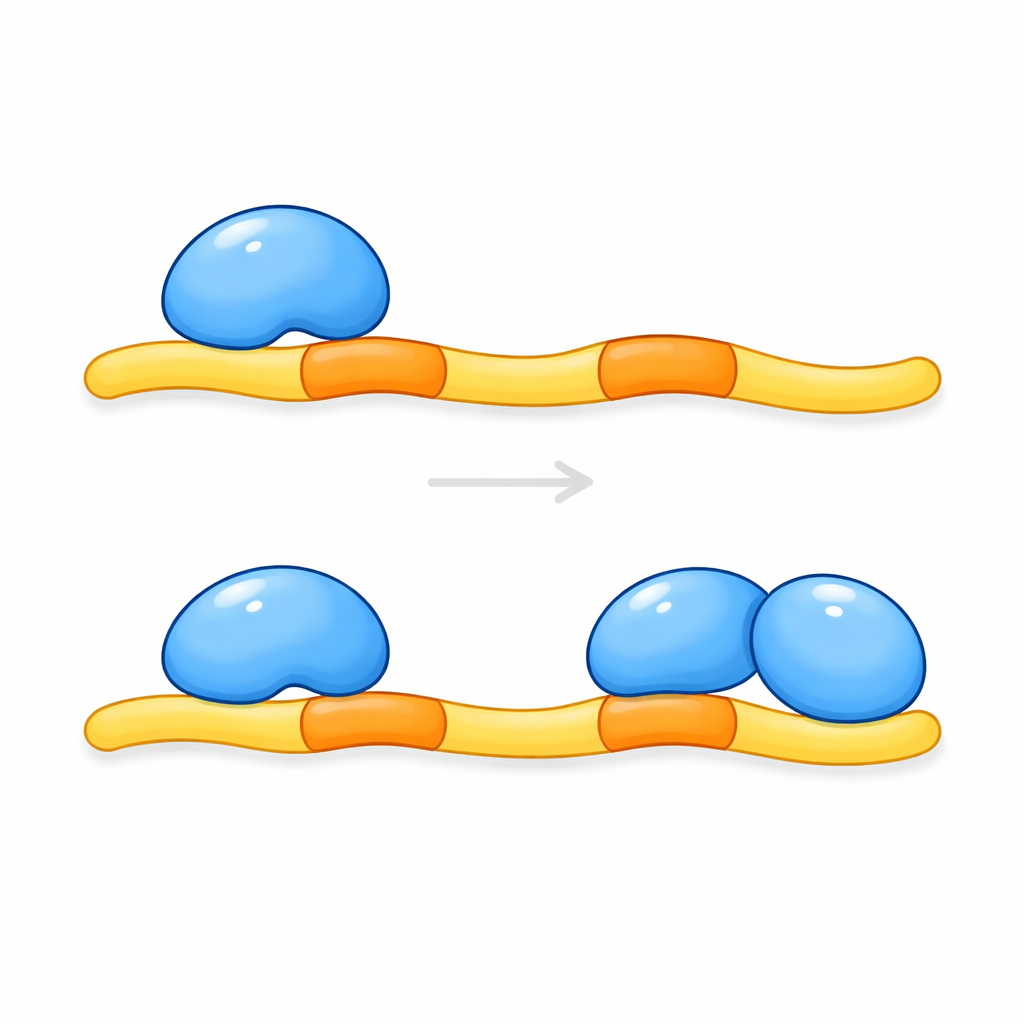
Gevolgen voor hersenziekten en verder
Deze bevindingen tonen aan dat KRIT1 niet simpelweg één CCM2-molecuul bindt; in plaats daarvan fungeert het als een scaffold dat een paar CCM2-eiwitten rekruteert. Alleen wanneer beide aanlegplaatsen op KRIT1 bezet zijn, kan het complex de productie van KLF4 adequaat onderdrukken en zo helpen fragiele vatgroei te voorkomen. Mutaties in KRIT1 die een van beide aanlegplaatsen verstoren, zullen naar verwachting deze beschermende klem verzwakken en kunnen sommige erfelijke vormen van cerebrale cavernomateuze malformaties verklaren. Omdat veel andere menselijke eiwitten vergelijkbare dubbele aanlegmotieven dragen, wijst deze studie ook op een breder principe: dubbele binding door paren van verwante domeinen kan een algemene manier zijn waarop cellen signaalnetwerken fijnregelen. Het begrijpen van deze driepartijeninteractie kan uiteindelijk strategieën sturen om bloedvaten te stabiliseren bij mensen met risico op hersenbloedingen.
Bronvermelding: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Trefwoorden: cerebrale cavernomateuze malformaties, endotheelcellen, KRIT1, CCM2, KLF4