Clear Sky Science · nl
Contrastvrije identificatie van de bloed‑hersenbarrièrestatus bij gliomen via generatieve diffusie‑AI en niet‑contrast MRI
Waarom dit belangrijk is voor hersentumorpatiënten
Mensen met hersentumoren ondergaan routinematig MRI‑scans, en veel patiënten krijgen ook geïnjecteerde contrastvloeistof zodat artsen kunnen zien of de beschermende bloed‑hersenbarrière is beschadigd. Die informatie stuurt de keuze voor operatie, bestraling en prognose—maar het contrastmiddel kan risico’s met zich meebrengen, voegt tijd en kosten toe en is niet altijd beschikbaar. Deze studie presenteert een kunstmatig‑intelligentiesysteem (AI) dat routinematige, contrastvrije MRI‑scans leest en virtueel de ontbrekende contrastbeelden reconstrueert, zodat artsen de status van de bloed‑hersenbarrière kunnen afleiden zonder enig contrastmiddel toe te dienen.
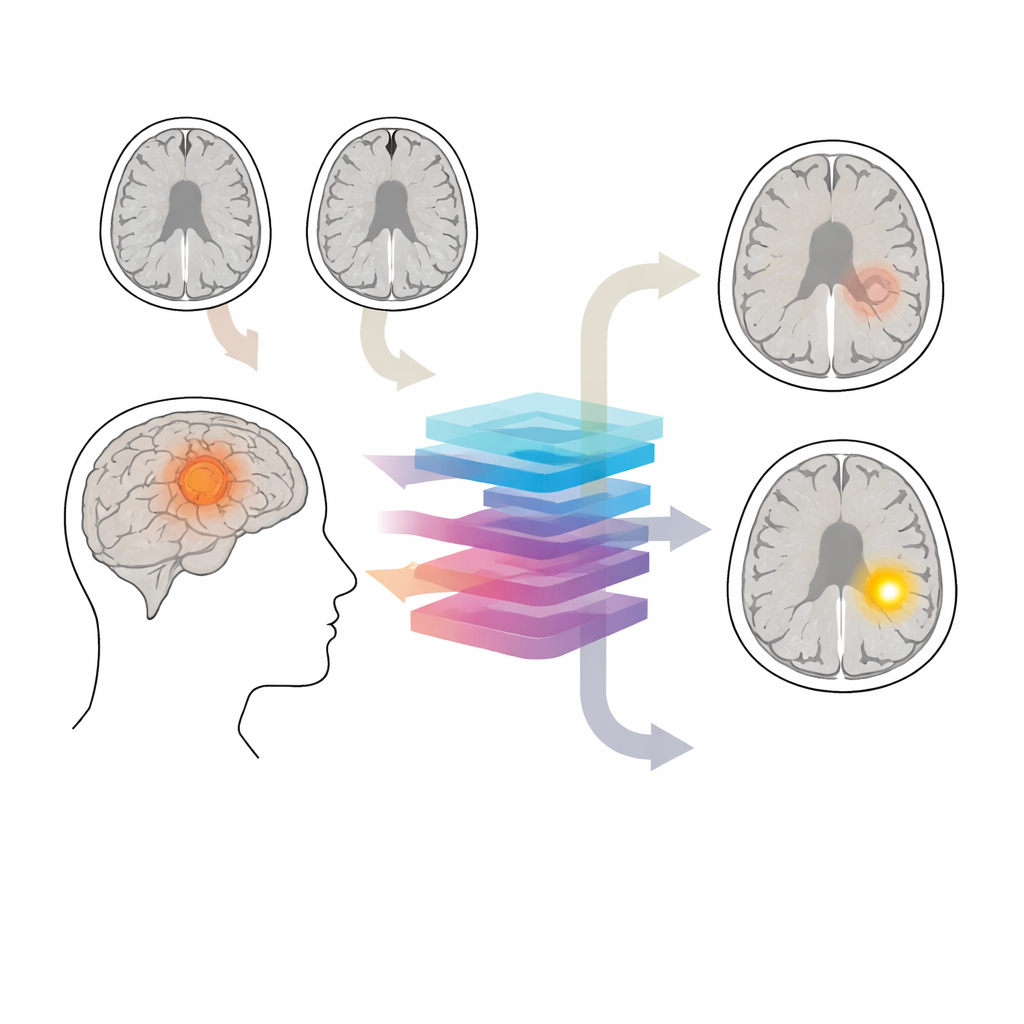
De beschermende poortwachter van de hersenen
De bloed‑hersenbarrière werkt als een microscopisch filter rond bloedvaten in de hersenen en laat alleen zeer kleine moleculen passeren. Bij veel gliomen wordt deze barrière lek. Op standaard contrast‑MRI lichten lekke gebieden op na injectie, terwijl intacte regio’s donker blijven. Deze patronen beïnvloeden hoe agressief een tumor wordt behandeld en helpen bepalen wat chirurgisch verwijderd of met bestraling bestreken moet worden. Toch worden contrastscans soms overgeslagen—bijvoorbeeld tijdens vroege onderzoeken of bij langetermijnfollow‑up van langzaam groeiende tumoren—en sommige patiënten moeten contrast vermijden vanwege nierziekte, allergische reacties of zorgen over gadoliniumafzetting in de hersenen.
Gewone scans omzetten in virtueel contrast
De auteurs vroegen zich af of niet‑contrast MRI‑scans, die al veel worden gemaakt, genoeg subtiele informatie bevatten zodat AI kan afleiden wat een contrastscan zou hebben laten zien. Ze concentreerden zich op twee veelgebruikte sequenties: T1 en T2‑FLAIR. Hoewel deze niet direct lekkage van de bloed‑hersenbarrière tonen, leggen ze tumordistributie, omliggende zwelling en weefselschade vast die vaak gepaard gaan met barrière‑afbraak. Het team bouwde een systeem genaamd CBSI dat eerst synthetische contrastversterkte beelden genereert uit deze niet‑contrastscans en die vervolgens, samen met de originele beelden, gebruikt om te bepalen of de barrière intact of verstoord is bij elk glioma.
Hoe het nieuwe AI‑systeem werkt
Centraal in CBSI staat een diffusiemodel—een type AI dat begint met ruisachtige beelden en die iteratief "denoist" tot realistische afbeeldingen. Hier leert het model niet‑contrastinput om te zetten in twee alternatieve virtuele contrastbeelden: één met de veronderstelling van een intacte barrière en één met de veronderstelling van een lekke barrière. Een begeleidingsmechanisme geeft het model aan welk patroon van versterking het moet nastreven, en een aanvullende segmentatiestap helpt het extra aandacht te geven aan het tumorgebied. In een tweede fase vergelijkt een apart netwerk voor elke patiënt de twee synthetische uitkomsten en beoordeelt welke meer zelfconsistent is met de originele MRI‑gegevens. Die beslissing wordt vervolgens vertaald naar de voorspelde status van de bloed‑hersenbarrière.
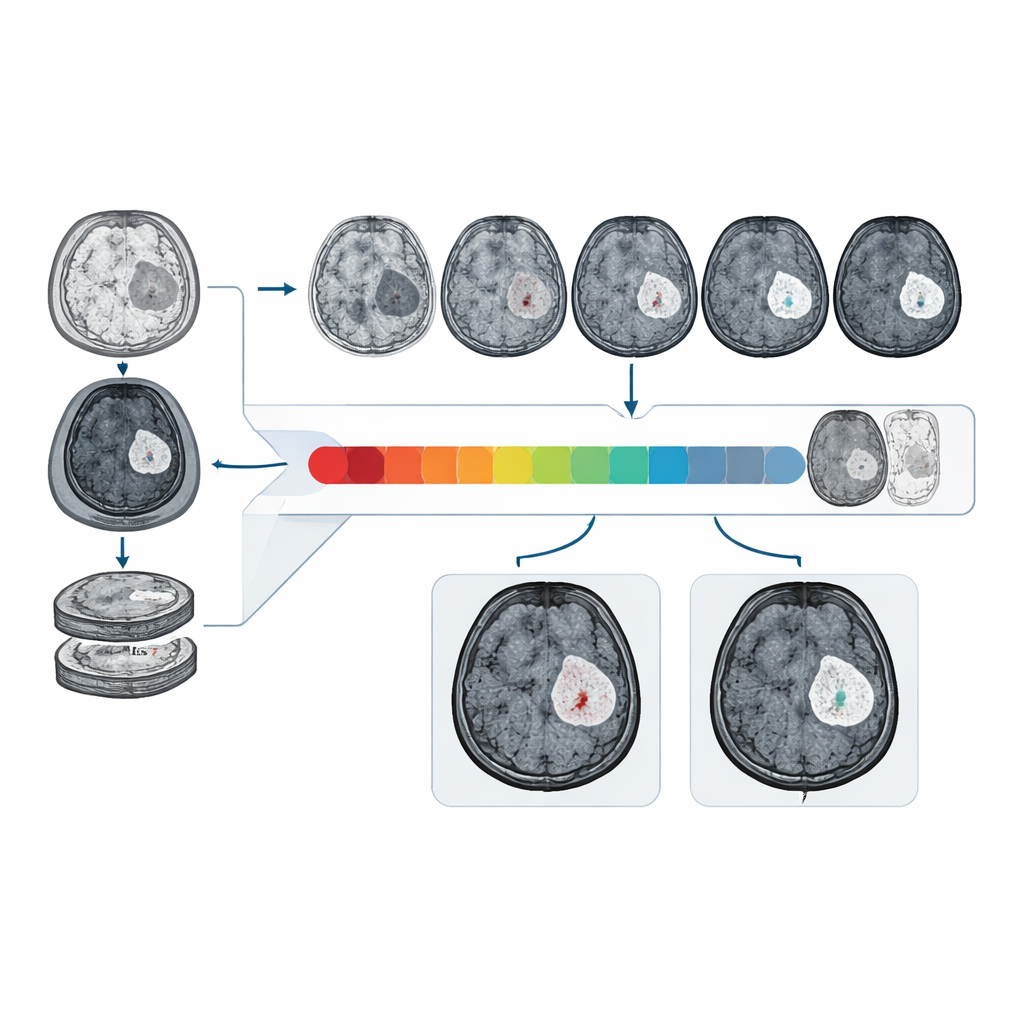
Prestaties op echte en diverse datasets
De onderzoekers trainden en testten CBSI op MRI‑gegevens van 1.535 gliomapatiënten verzameld in meerdere ziekenhuizen en uit internationale openbare datasets. Op een externe klinische testset onderscheidde CBSI intacte van verstoorde barrières met een area under the curve van ongeveer 81%, duidelijk beter dan modellen die alleen op niet‑contrastbeelden vertrouwden en in de buurt van de prestaties van modellen die echte contrastscans konden gebruiken. Radiologen beoordeelden, bij het zien van gerandomiseerde mengsels van echte en synthetische contrastbeelden van het systeem, meer dan 90% van de synthetische afbeeldingen als van hoge diagnostische kwaliteit, en hun vermogen om contrastversterking op synthetische beelden te identificeren was vergelijkbaar met hun prestaties op echte scans.
Voordelen voor behandelplanning en toekomstige zorg
Aangezien de synthetische contrastbeelden die door CBSI worden geproduceerd tumordetails en versterkingspatronen vastleggen, verbeterden ze ook downstreamtaken zoals het afbakenen van tumorgrenzen en het inschatten van tumorgraad—beide sterk afhankelijk van het gedrag van de bloed‑hersenbarrière. De methode generaliseerde goed naar verschillende scanners, beeldvormingsprotocollen en patiëntpopulaties, inclusief gegevens uit Sub‑Saharaans Afrika en grotere internationale cohorten. Hoewel de auteurs erkennen dat elk deep‑learning‑systeem een statistisch hulpmiddel blijft en geen directe kijk op de biologie biedt, suggereren hun resultaten dat virtuele contrastbeeldvorming het gebruik van geïnjecteerde middelen zou kunnen verminderen, vooral voor kwetsbare patiënten of in situaties waarin contrastscans moeilijk te verkrijgen zijn. In praktische zin zou deze AI‑benadering artsen in staat kunnen stellen belangrijke, behandelvormende informatie over de bloed‑hersenbarrière uit de scans te halen die patiënten toch al ondergaan—zonder een extra injectie.
Bronvermelding: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Trefwoorden: glioma, bloed‑hersenbarrière, hersenen MRI, medische beeldvorming AI, contrastvrije beeldvorming