Clear Sky Science · nl
Nanobody-gebaseerde IgG remmen tegelijkertijd de allergene en enzymatische activiteit van het dominante honingbijengifallergeen
Waarom bijensteken ertoe doen
Voor de meeste mensen is een steek van een honingbij pijnlijk maar van korte duur. Voor anderen kan het een levensbedreigende reactie van het hele lichaam uitlokken, anafylaxie genoemd. De belangrijkste preventieve behandeling van vandaag, venom immunotherapy, helpt veel patiënten maar duurt jaren, vereist frequente injecties en kan zelf allergische bijwerkingen veroorzaken. Deze studie onderzoekt een nieuwe, gerichtere manier om mensen die gevaarlijk allergisch zijn voor honingbijengif te beschermen door één sleutelelement van het gif uit te schakelen voordat het schade kan aanrichten.
De belangrijkste boosdoener in bijengif
Honingbijengif is een cocktail van verschillende moleculen, maar één eiwit, fosfolipase A2 (of Api m 1), steekt er bovenuit. Het is het dominante allergeen bij patiënten met een honingbijallergie en komt bijna bij iedereen voor. Api m 1 heeft een dubbele rol: het beschadigt celmembranen, wat bijdraagt aan pijn en ontsteking op de steekplaats, en het is tevens een belangrijk doelwit voor allergie-opwekkende antilichamen bekend als IgE. Wanneer Api m 1 bindt aan IgE die verankerd is op immuuncellen zoals mestcellen en basofielen, kan dat een kettingreactie veroorzaken die leidt tot de plotselinge vrijgave van ontstekingsstoffen en in ernstige gevallen tot anafylaxie.
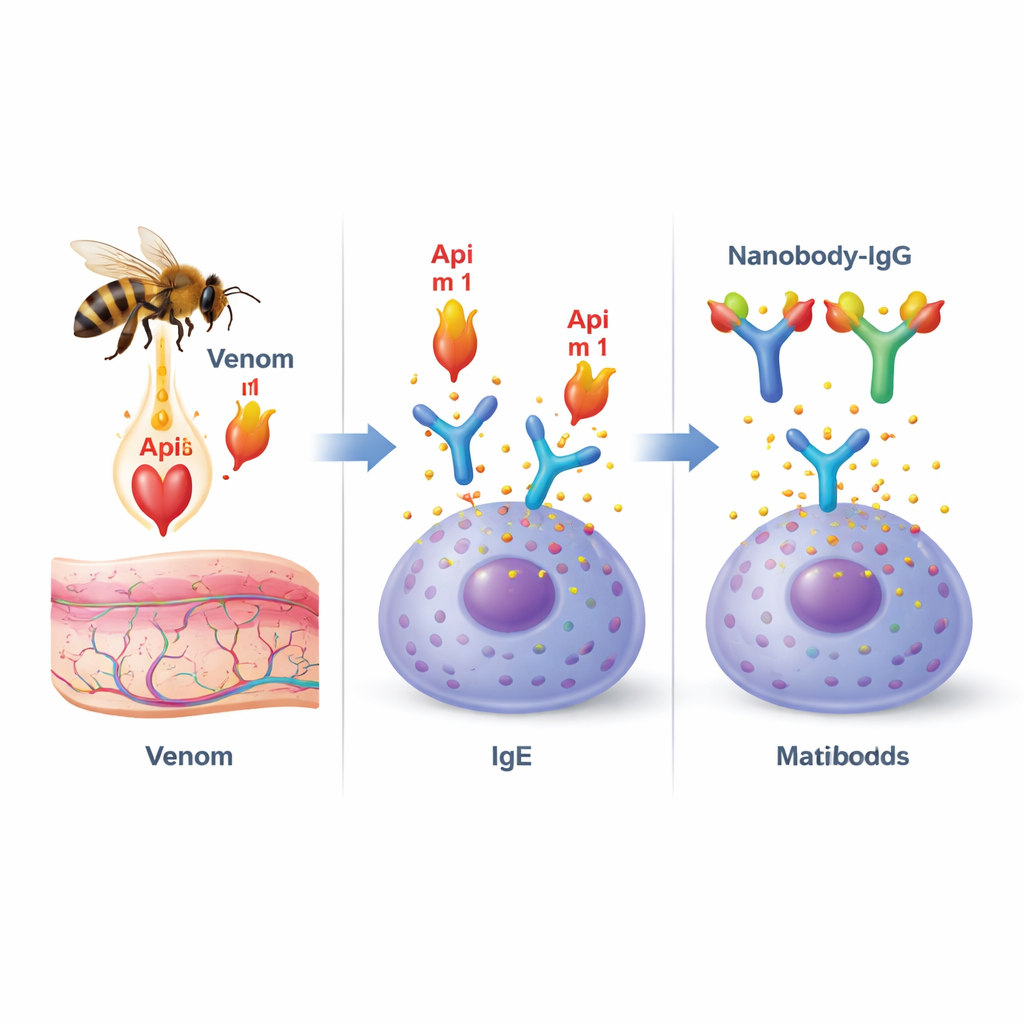
Ontwerpen van kleine antilichamen om het allergeen te blokkeren
De onderzoekers gebruikten "nanobodies", kleine, stabiele antilichaamfragmenten die oorspronkelijk werden ontdekt bij kameelachtigen. Omdat ze klein en langwerpig zijn, passen nanobodies bijzonder goed in groeven en pockets op eiwitten. Het team isoleerde Api m 1-specifieke nanobodies uit een immuunbibliotheek en selecteerde twee opvallende kandidaten, AM1-1 en AM1-4. Gedetailleerd structureel werk met röntgendiffractie toonde aan dat deze twee nanobodies zich aan tegenovergestelde zijden van Api m 1 klemmen en elkaar niet in de weg zitten. De ene nanobody, AM1-1, ligt direct over het actieve centrum van het enzym, wat suggereert dat ze de membraanschadende functie van Api m 1 kan blokkeren, terwijl AM1-4 zich in een afzonderlijk pocket op het eiwitoppervlak nestelt.
Nanobodies omzetten in krachtige blokkers
Om van deze kleine binders langdurig werkzame geneesmiddelen te maken, fuseerden de wetenschappers elke nanobody aan het staartdeel (Fc‑regio) van menselijk IgG1, waardoor grotere antilichaamachtige moleculen ontstonden met betere stabiliteit in de bloedbaan. Ze ontwikkelden ook een 'bispecifieke' variant die zowel AM1-1 als AM1-4 draagt in één IgG-achtig molecuul. Laboratoriumtests toonden aan dat deze nanobody-IgG-fusies met extreem hoge affiniteit aan Api m 1 binden en, wanneer aanwezig, de binding van IgE uit het bloed van honingbijallergische patiënten aan Api m 1 sterk kunnen verminderen. In celgebaseerde assays verminderden ze de activatie van basofielen, de immuuncellen die normaal sterk reageren bij blootstelling aan Api m 1 bij allergische personen.
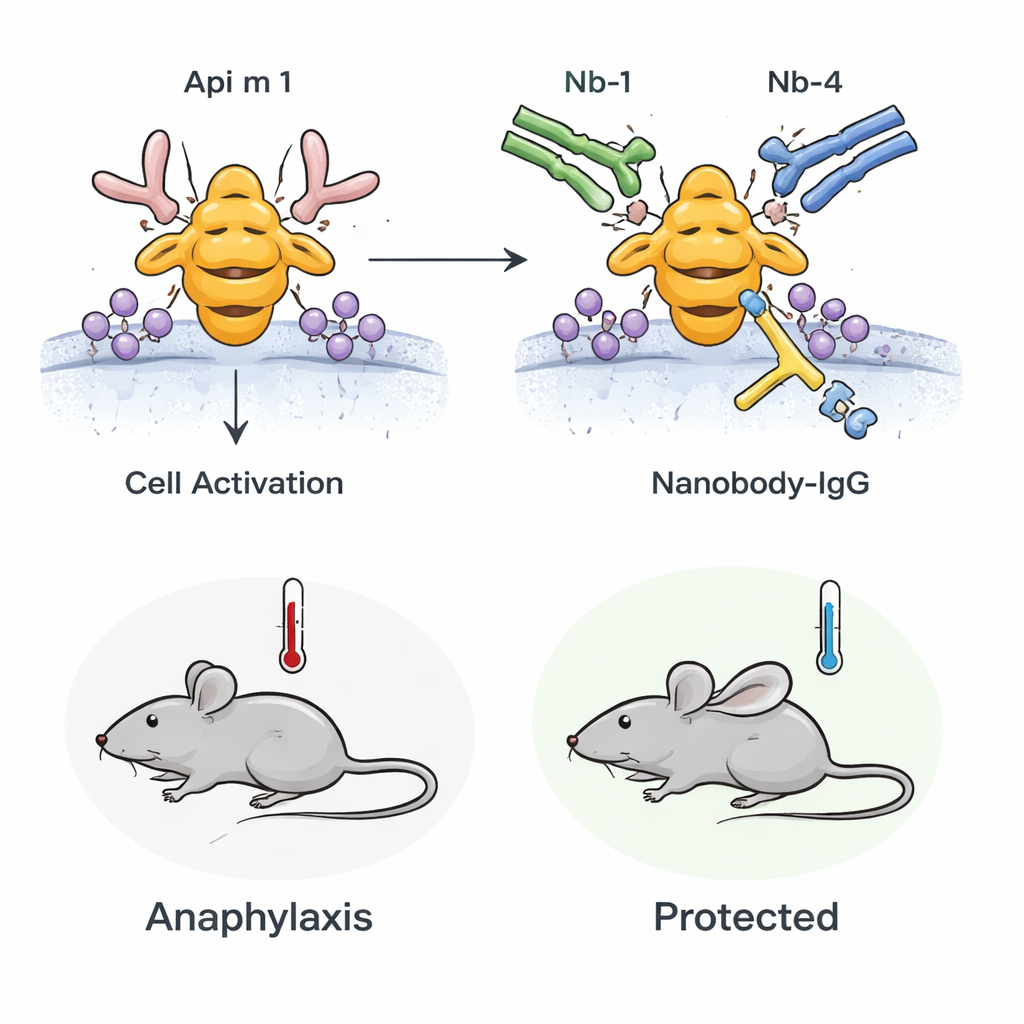
Van reageerbuis naar levende dieren
Het team vroeg zich vervolgens af of dit blokkerende effect ook in een levend organisme zou standhouden. Ze gebruikten muizen die gesensibiliseerd waren voor honingbijengif zodat hun immuunsysteem op Api m 1 reageerde op een manier die de menselijke allergie nabootst. Toen deze muizen werden blootgesteld aan Api m 1, ontwikkelden ze aanwijzingen voor anafylaxie, waaronder een daling van de lichaamstemperatuur en markers van mestcelactivatie in het bloed. Als de muizen echter vooraf werden behandeld met de bispecifieke nanobody-IgG, werden zowel de temperatuurdaling als de mestcelactivatie aanzienlijk verminderd. Dit toont aan dat vooraf aanwezige, hoogaffiene blokkerende antilichamen de systemische allergische reactie op Api m 1 in vivo kunnen temperen.
Wat dit kan betekenen voor mensen met een bijengifallergie
Samengevat laat de studie zien dat zorgvuldig ontworpen nanobody-gebaseerde IgG-moleculen tegelijkertijd de allergene en enzymatische werking van Api m 1, de belangrijkste dader bij honingbijengifallergie, kunnen blokkeren. Voor patiënten opent dit de mogelijkheid van een seizoensgebonden, passieve immunisatie: een paar injecties van zulke antilichamen tijdens de maanden waarin bijensteken het meest waarschijnlijk zijn, zou tijdelijke bescherming kunnen bieden tegen ernstige reacties, zonder de langdurige verplichting en risico's van traditionele venom immunotherapy. Hoewel er meer werk nodig is om de aanpak uit te breiden naar andere gifcomponenten en om veiligheid en werkzaamheid bij mensen te testen, biedt deze nanobody-strategie een precieze nieuwe manier om kwetsbare personen tegen gevaarlijke bijensteken te beschermen.
Bronvermelding: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
Trefwoorden: allergie voor bijengif, nanobodies, passieve immunotherapie, fosfolipase A2, preventie van anafylaxie