Clear Sky Science · nl
Coöperatieve klemgemedieerde promotorherkenning door poxvirus-RNA-polymerase en zijn TBP/TFIIB-achtige partner
Hoe een virus de genregulatie in onze cellen herschakelt
Poxvirussen, waaronder het virus dat historisch verantwoordelijk was voor pokken, voeren al hun genexpressie uit in het cytoplasma van onze cellen, ver van het DNA-controlecentrum in de kern. Om dit voor elkaar te krijgen, nemen ze hun eigen verkleinde " genetische fabriek" mee. Deze studie onthult op atomair detail hoe één van die virussen, Vaccinia, halverwege de infectie een specifieke golf van zijn genen inschakelt door een onverwacht klemachtig eiwit te gebruiken dat samenwerkt met het virale kopieermechanisme.
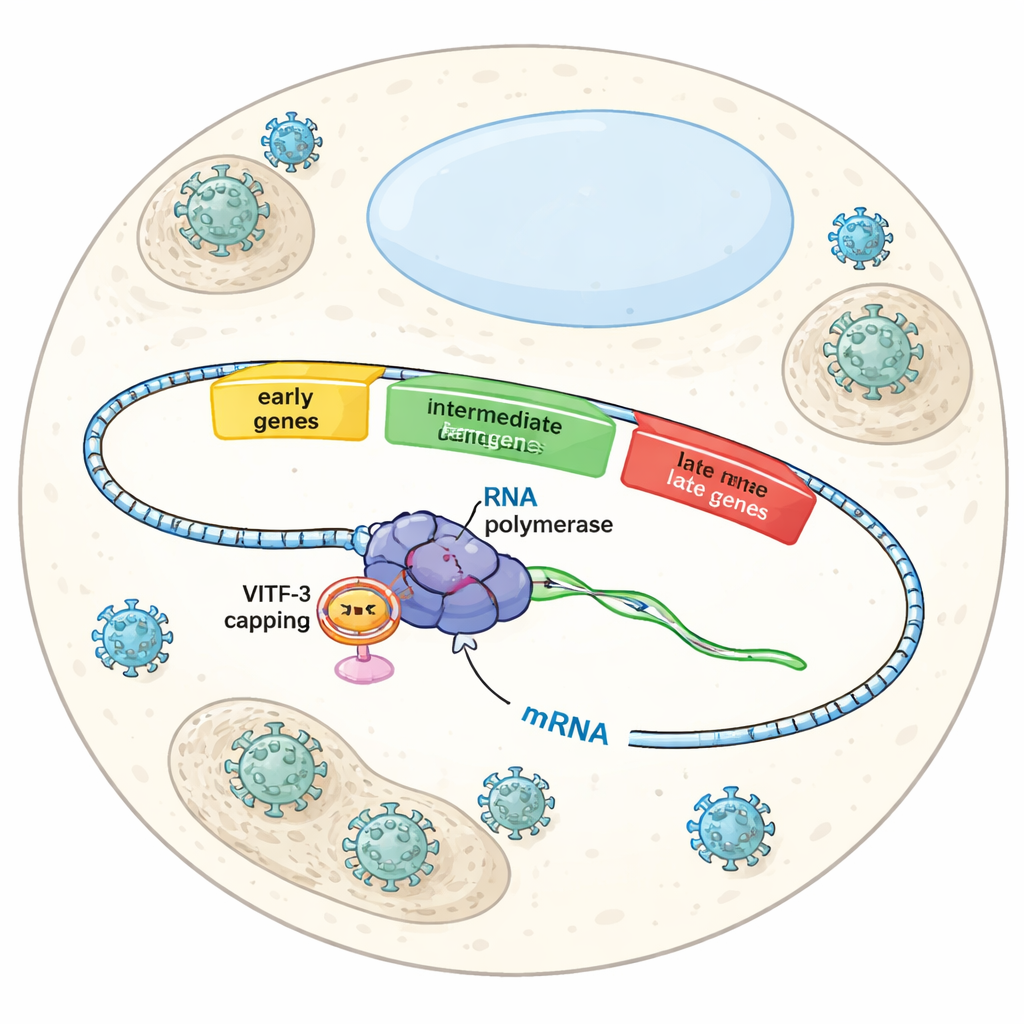
Drie golven in een virale overname
Wanneer Vaccinia een cel infecteert, zet het niet al zijn genen tegelijkertijd aan. In plaats daarvan volgt het een zorgvuldig getimede verdeling met vroege, intermediaire en late genen. Vroege genen bereiden het terrein voor virale replicatie, intermediaire genen helpen bij de opbouw van de machinerie voor het maken van nieuwe deeltjes, en late genen voltooien de montage en verpakking. Elke golf hangt af van dezelfde virale RNA-polymerase — het enzym dat DNA afleest om RNA te maken — maar verschillende hulpfactoren vertellen de polymerase welke groep genen in elke fase geactiveerd moet worden. Tot nu toe begrepen wetenschappers de controle over vroege genen redelijk goed, maar hoe het virus specifiek intermediaire genen herkende en activeerde bleef een mysterie.
Een ringvormige hulp die een partner nodig heeft
De onderzoekers richtten zich op een tweedelig eiwit genaamd VITF-3, dat nodig is voor het inschakelen van intermediaire genen. Veel organismen, inclusief mensen, gebruiken een paar eiwitten genaamd TBP en TFIIB om hun RNA-polymerase naar het juiste startpunt op het DNA te leiden. Het team toonde aan dat VITF-3 een sterk gemodificeerde versie is van datzelfde oude paar. In tegenstelling tot zijn cellulaire verwanten pakt VITF-3 op zichzelf echter niet aan het DNA. In plaats daarvan vergrendelen de twee subunits zich tot een gesloten ring die inert is tegenover DNA tenzij de virale RNA-polymerase aanwezig is. Dit was onverwacht, want in de meeste systemen bindt het TBP-achtige component eerst het promotor-DNA en rekruteert vervolgens de polymerase; hier lijkt het virus de volgorde van gebeurtenissen te hebben herschreven.
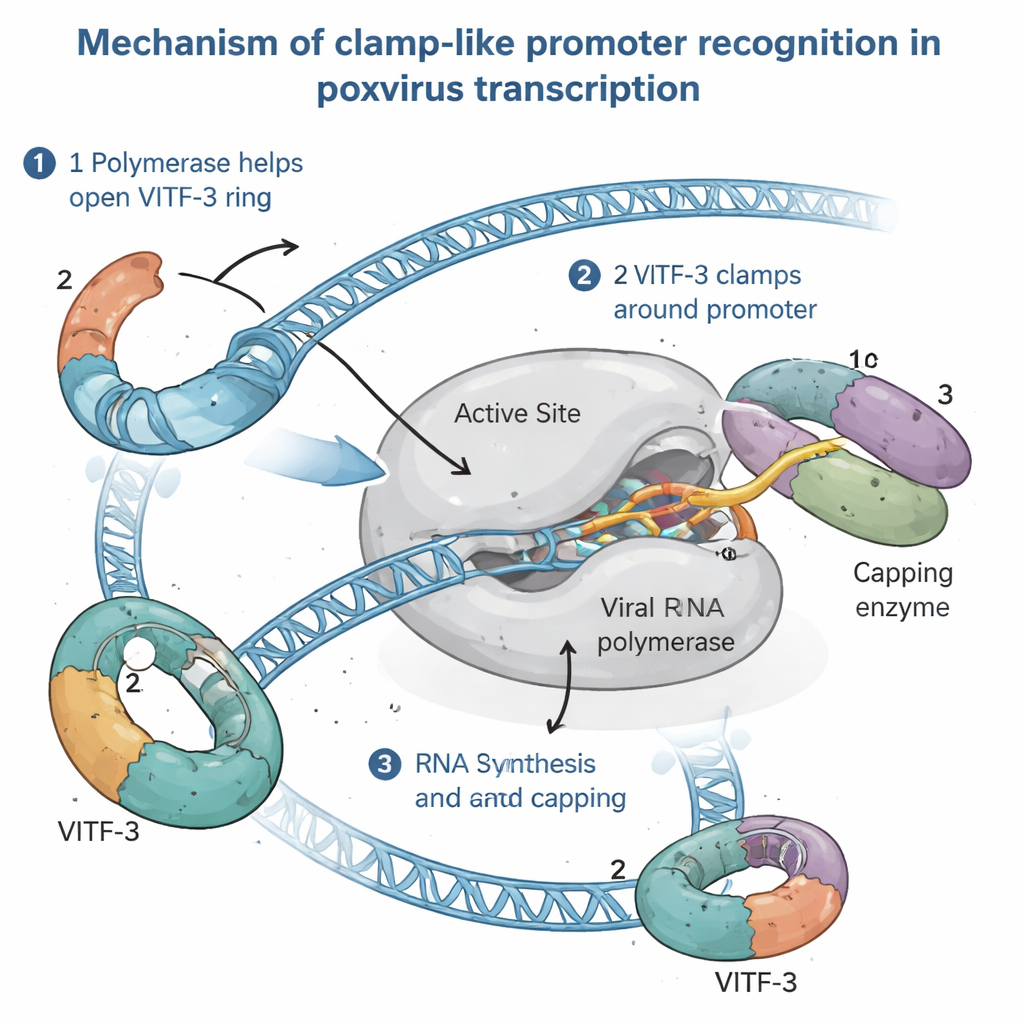
Het intermediaire transcriptieapparaat in actie zien
Om te begrijpen hoe deze ongewone opzet werkt, isoleerden de auteurs het volledige intermediaire pre-initiatiefcomplex — de assemblage klaar net voordat de RNA-synthese begint — uit geïnfecteerde menselijke cellen. Met behulp van hogeresolutie cryo-elektronmicroscopie visualiseerden ze het complex tot ongeveer 2,4 Ångström detail, scherp genoeg om zijketens van aminozuren en individuele DNA-basen te zien. De beelden toonden de virale RNA-polymerase die het promotor-DNA vasthoudt, terwijl VITF-3 een strakke ring vormt rond een AT-rijke DNA-strek net stroomopwaarts van de startplaats. Deze ring buigt het DNA scherp ongeveer 90 graden en voert het in een spleet in de polymerase. Tegelijkertijd is een viraal capping-enzym — verantwoordelijk voor het toevoegen van de beschermende cap aan het 5′-uiteinde van viraal RNA — aangehecht op de polymerase, klaar om nieuwe transcripties direct bij ontstaan te modificeren.
Een klem-laadmechanisme geleend in geest
Door structurele momentopnames te combineren met biochemische testen, stelt de studie voor dat de virale RNA-polymerase actief VITF-3 op het DNA laadt, en fungeert als een "klem-lader." Eerst bindt de polymerase aan een intermediair promotor en helpt zij om de VITF-3-ring open te wrikken. Vervolgens sluit zij, samen met het capping-enzym, de ring rond het AT-rijke gebied en klemt het complex vast op zijn plaats. Het DNA smelt nabij de startplaats en de polymerase leest rechtstreeks een korte vierletterige sequentie (een TAAA-motief) die precies aangeeft waar de RNA-synthese moet beginnen. Wanneer het RNA groeit, volgt het hetzelfde pad dat door een deel van VITF-3 in het initiële complex werd ingenomen, waardoor het oprijzende RNA waarschijnlijk VITF-3 opzij duwt, zodat de polymerase het promotor kan verlaten en langs het gen kan doorgaan terwijl VITF-3 mogelijk achterblijft om hergebruik van hetzelfde promotor te versnellen.
Wat dit betekent voor het begrijpen en richten op poxvirussen
Kort gezegd laat dit werk zien dat het Vaccinia-virus een universele genregulatiemodule heeft herbestemd tot een klem die alleen DNA vastgrijpt wanneer zijn eigen RNA-polymerase dat aangeeft. Die slimme wending stelt het virus in staat één kernenzym te gebruiken voor drie zeer verschillende transcriptieprogramma’s, simpelweg door fase-specifieke helpers te wisselen. Omdat hetzelfde soort factoren bewaard blijft in veel poxvirussen, inclusief menselijke ziekteverwekkers, bieden het nieuw onthulde klem-laadmechanisme en de unieke VITF-3-ring concrete structurele doelen voor antivirale strategieën die gericht zijn op het verstoren van het vermogen van het virus om zijn genen tijdens infectie te timen en te controleren.
Bronvermelding: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Trefwoorden: poxvirus transcriptie, Vaccinia-virus, RNA-polymerase, promotorherkenning, transcriptiefactoren