Clear Sky Science · nl
Fosfoglycerraatdehydrogenase-gemedieerde serinereprogrammering verergert macrofaaghyperinflammatie bij muizen met Pseudomonas aeruginosa-longontsteking
Als de verdedigers van het lichaam te ver gaan
Longontsteking veroorzaakt door de bacterie Pseudomonas aeruginosa is berucht moeilijk te behandelen, vooral bij mensen met kwetsbare longen. Antibiotica richten zich op de microbe, maar deze ziekte is vaak dodelijk niet alleen door de bacteriën zelf, maar doordat de eigen immuunrespons van het lichaam uit de hand loopt. Deze studie onthult hoe één metabole “schakelaar” in immuuncellen hen kan verschuiven van behulpzaam naar schadelijk — en suggereert dat bijsturing van dieet of cellulaire metabolisme levensbedreigende longontsteking zou kunnen temperen.
Een gevaarlijke dans tussen kiem en immuunsysteem
Pseudomonas aeruginosa is een veelvoorkomende gramnegatieve bacterie die de lage luchtwegen kan binnendringen en ernstige longontsteking kan veroorzaken. Normaal patrouilleren longresidentie immuuncellen, macrofagen genoemd, in de luchtzakken, waarbij ze indringers opeten en alarm slaan met chemische signalen. Maar bij een hoge bacteriële belasting werven deze cellen grote aantallen reserve-macrofagen uit de bloedbaan. Het resultaat kan een storm van inflammatoire moleculen zijn die het kwetsbare longweefsel beschadigen, herstelprocessen belemmeren en in ernstige gevallen leiden tot ademhalingsfalen en overlijden. De auteurs vroegen zich af of het interne metabolisme van deze macrofagen deze schadelijke overreactie zou kunnen aansturen.
Een metabool enzym in het heetst van de strijd
Het team concentreerde zich op een enzym genaamd fosfoglycerraatdehydrogenase (PHGDH), een belangrijk instappunt in de route waarmee cellen het aminozuur serine uit glucose maken. In muismodellen van Pseudomonas-longinfectie stegen PHGDH-niveaus en -activiteit scherp in de longen, vooral in macrofagen. Wanneer muizen werden behandeld met een kleine-molecuulremmer van PHGDH, of wanneer het gen voor PHGDH specifiek in myeloïde cellen (waaronder macrofagen) werd verwijderd, deden de dieren het beter: ze leefden langer, hadden minder longschade, droegen minder bacteriën en produceerden lagere hoeveelheden krachtige inflammatoire cytokinen zoals interleukine-6 en interleukine-1β. Op cellulair niveau verschuiven het blokkeren van PHGDH macrofagen weg van een sterk pro-inflammatoir stadium zonder de tegenovergestelde, wondhelende fenotype te versterken.
De brand aanwakkeren: serine en een overactieve signaalcircuits
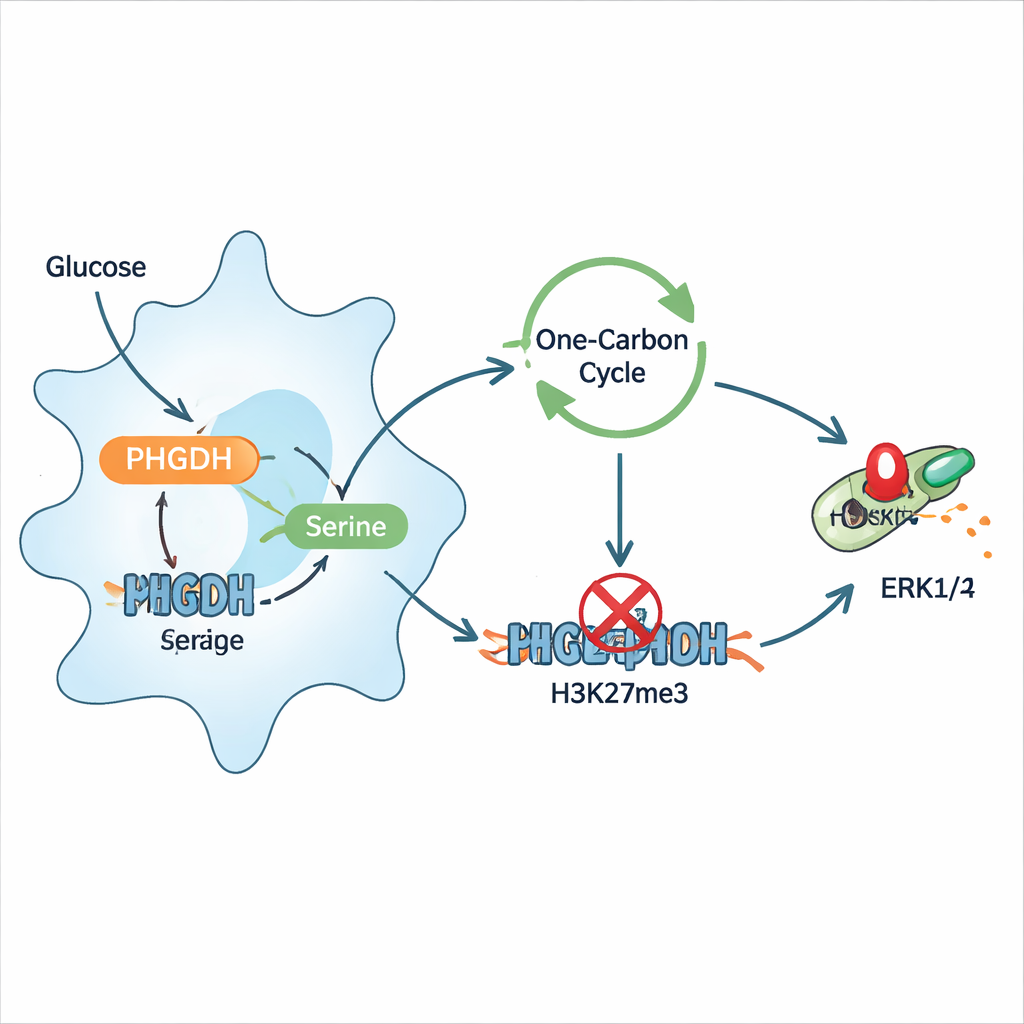
Dieper gravend toonden de onderzoekers aan dat infectie macrofagen herprogrammeert om meer glucose naar nieuwe serineproductie te leiden, en dat deze serine op haar beurt de ontsteking verergert. Extra serine deed macrofagen meer inflammatoire cytokinen afscheiden en meer oppervlaktemarkers van activatie tot expressie brengen, terwijl serine-beperkte diëten geïnfecteerde muizen beschermden en het aantal bacteriën verlaagden. Mechanistisch voedde serine een "one-carbon"-metabole cyclus die helpt bij het leveren van methylgroepen aan de cel, chemische labels die in epigenetische regulatie worden gebruikt. Dit versterkte een specifieke histonmarkering, H3K27-trimethylatie, in de buurt van het gen voor een remmend eiwit genaamd DUSP4, dat normaal helpt het ERK1/2-signaleringspad uit te schakelen. Wanneer DUSP4 werd onderdrukt, bleef ERK1/2 ingeschakeld en werden inflammatoire signalen versterkt. Het remmen van PHGDH of het verlagen van serine keerde deze keten om, herstelde DUSP4 en verminderde ERK1/2-fosforylering.
Macrofagen in balans brengen zonder de verdediging te verzwakken
Belangrijk is dat het terugschakelen van PHGDH het immuunsysteem niet simpelweg verlammde. Sterker nog, macrofagen zonder PHGDH waren beter in het insluiten en doden van Pseudomonas vroeg na infectie, terwijl ze tegelijkertijd minder schadelijke cytokinen produceerden. Het overdragen van deze PHGDH-deficiente macrofagen naar normale muizen verbeterde de uitkomst na bacteriële uitdaging, wat onderstreept dat de voordelen voortkwamen uit het herprogrammeren van de gastheerrespons in plaats van directe antimicrobiële werking. Het werk suggereert ook dat serinerijke diëten onbedoeld hyperinflammatie bij ernstige bacteriële pneumonie kunnen bevorderen, terwijl gecontroleerde serinebeperking een nieuwe manier zou kunnen bieden om overmatige longs schade te temmen.
Wat dit betekent voor de behandeling van moeilijk te genezen longontsteking
In begrijpelijke termen laat deze studie zien dat sommige macrofagen bij Pseudomonas-pneumonie suiker verbranden op een manier die extra serine produceert, en dat deze metabole omweg hun inflammatoire machine op overdrive zet. Door het enzym PHGDH te blokkeren of serine te beperken, konden de onderzoekers deze overreactie kalmeren, longweefsel beschermen en toch immuuncellen in staat stellen bacteriën te verwijderen. Hoewel het werk bij muizen is gedaan en ver van klinisch gebruik staat, wijst het op een veelbelovend idee: traditionele antibiotica combineren met geneesmiddelen of dieetinterventies die het immuuncelmetabolisme subtiel bijstellen, zou een destructief immuunvuur kunnen veranderen in een gecontroleerde, bacteriebestrijdende vlam.
Bronvermelding: Chen, R., Zeng, R., Shi, M. et al. Phosphoglycerate dehydrogenase-mediated serine reprogramming aggravates macrophage hyperinflammation in murine Pseudomonas aeruginosa pneumonia. Nat Commun 17, 1944 (2026). https://doi.org/10.1038/s41467-026-69539-1
Trefwoorden: Pseudomonas-pneumonie, macrofaagmetabolisme, serine-biosynthese, longontsteking, PHGDH