Clear Sky Science · nl
Ustilago maydis verstoort koolhydraatsignaleringsnetwerken om hypertrofie in gastheercellen te induceren
Wanneer gewasziekten cellen in ‘tumoren’ veranderen
Maïs (corn) is een van 's werelds belangrijkste voedsel- en voedervoedergewassen, en het heeft een ongebruikelijke vijand: de roestschimmel Ustilago maydis, die opgezwollen, tumorachtige aangroeiingen op bladeren en kolven veroorzaakt. Naast het opvallende uiterlijk leiden deze aangroeiingen ongemerkt de suikers van de plant weg van normale groei en afweer en in winst voor de schimmel. Deze studie onthult hoe een enkel schimmeleiwit helpt de interne energieschakelaars van de plant om te zetten, waardoor gewone bladcellen veranderen in opgezwollen, zetmeelgevulde fabrieken die de pathogeen voeden.
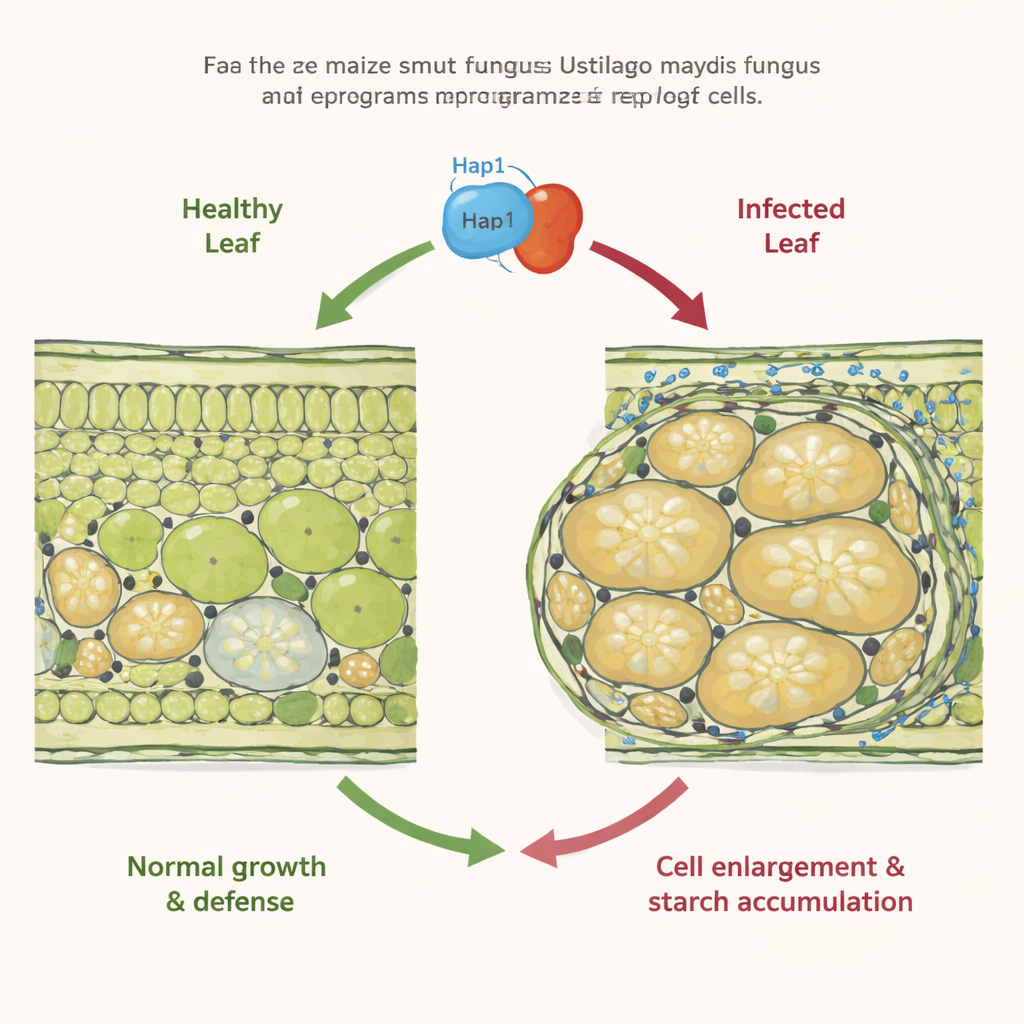
Een schimmel die plantengroei herbedraadt
De meeste schimmels die smut veroorzaken verspreiden zich geruisloos door graangewassen en vervormen voornamelijk de bloemen. Ustilago maydis is anders: hij kan plaatselijke tumoren vormen op bijna elk bovengronds deel van de maïsplant. Eerder werk toonde aan dat in geïnfecteerde bladeren sommige cellen te veel beginnen te delen (hyperplasie), terwijl aangrenzende mesofylcellen, die normaal fotosynthese uitvoeren, in plaats daarvan dramatisch opzwellen (hypertrofie) en stoppen met delen. Deze hypertrofe cellen vullen zich ook met zetmeelkorrels op plaatsen waar C4-planten zoals maïs gewoonlijk geen zetmeel opslaan. De moleculaire triggers achter deze extreme celuitzetting en suikerhamstering waren echter onbekend.
Het vinden van de schimmeltrigger voor celschijning
De onderzoekers richtten zich op schimmel-"effector"-eiwitten — moleculen die in plantweefsel worden uitgescheiden en de gastheerbiologie herschikken. Vanuit een lijst van effectors die specifiek actief zijn in hypertrofe tumorcellen gebruikten ze CRISPR-Cas9 om verschillende kandidaatgenen in U. maydis uit te schakelen. Eén gen, UMAG_02473, sprong eruit: mutanten die het misten veroorzaakten veel minder tumoren en lieten plantencellen zien met kleinere kernen en veel minder zetmeel in het bladmeseofyl. Omdat vergrote kernen kenmerkend zijn voor endoreduplicatie — cellen die hun DNA kopiëren zonder te delen — concludeerde het team dat deze effector, die ze Hap1 (hypertrofie-geassocieerd eiwit 1) noemden, cruciaal is om mesofylcellen in een groeiprogramma zonder deling te duwen en voor het stimuleren van zetmeelopbouw.
Het kapen van de energie-hoofdschakelaar van de plant
Om te begrijpen hoe Hap1 het metabolisme van maïs herschikt, zochten de wetenschappers naar zijn plantaardige doelwitten. Ze toonden aan dat Hap1 in gastheercellen wordt afgeleverd en zich ophoopt in zowel het cytoplasma als de kern. Met eiwit pull-downs en massaspectrometrie vonden ze dat Hap1 bindt aan het maïseiwit SnRK1, een centraal energiesensor die normaal reageert op stress en lage energie door suikervrijmakende paden aan te zetten, energie-intensieve synthese (zoals zetmeelvorming) terug te schakelen en afweerreacties te versterken. Verdere tests bevestigden dat Hap1 fysiek interacteert met de katalytische subeenheden van SnRK1. Wanneer Hap1 aanwezig was, veranderden de fosforyleringspatronen op SnRK1-componenten en bekende SnRK1-doeleiwitten, en een directe kinase-assay toonde dat Hap1 de capaciteit van SnRK1 om een standaard testsubstraat te fosforyleren vermindert. Kortom, Hap1 verstoort de energie-"thermostaat" van de plant en verzwakt de gebruikelijke reactie op stress en voedingsstoffentekort.
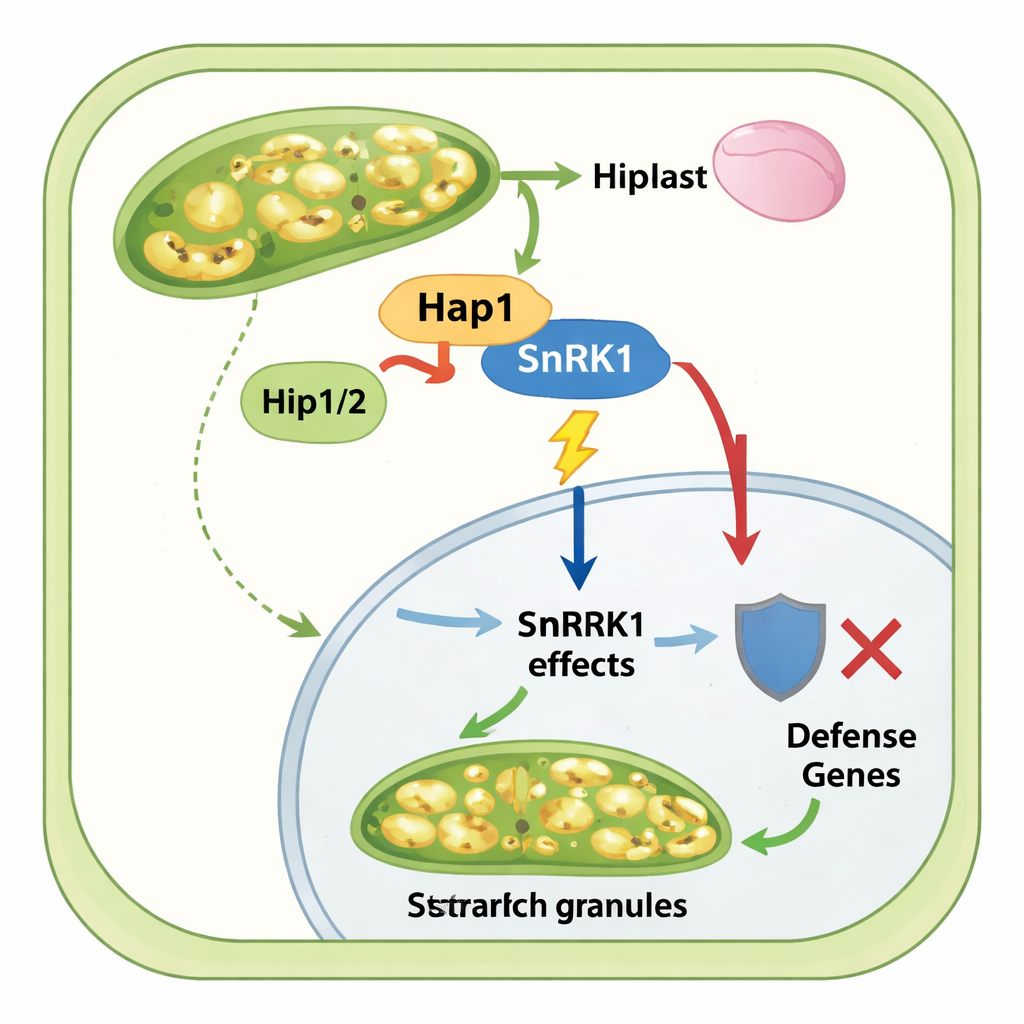
Hulp-effectors en een suikerrijk tumor-niche
Het verhaal eindigt niet met Hap1 alleen. Het team ontdekte twee aanvullende schimmeleffectors, Hip1 en Hip2, die specifiek met Hap1 interageren en ook in hypertrofe tumorcellen tot expressie komen. Hoewel het verwijderen van deze helpers beperkte invloed had op de algehele ziektevretheid, toonden biochemische experimenten aan dat Hip1 en Hip2 zowel aan Hap1 als aan het SnRK1-complex binden, helpen Hap1-eiwitniveaus te handhaven en nodig zijn voor Hap1 om efficiënt SnRK1 uit geïnfecteerd maïsweefsel te ‘pulldown’. Fosfoproteomica en genexpressiegegevens samen lieten zien dat wanneer Hap1 aanwezig is, maïstumoren genen en enzymen voor zetmeelsynthese omhoogreguleren, terwijl genen die gekoppeld zijn aan plantenafweer en normale proteïnesynthese worden onderdrukt. Zonder Hap1 daalt de zetmeelaccumulatie in mesofylcellen sterk en worden stress- en afweergerelateerde signaalroutes actiever.
Wat dit betekent voor maïs en zijn verdediging
In gewone bewoordingen laat dit werk zien dat Ustilago maydis niet alleen succes heeft door weefsels te beschadigen, maar door bedreven te knoeien met de interne energieregeling van de plant. De Hap1-effector, versterkt door zijn partners Hip1 en Hip2, lijkt de SnRK1 op "stil" te zetten — een belangrijke beschermer die normaal energie spaart en immuunverdedigingen ondersteunt. Met deze beveiliging verzwakt, stoppen maïsmesofylcellen met functioneren als normale groene fabriekjes en zwellen ze op, kopiëren hun DNA zonder te delen en hamsteren zetmeel. Deze tumorachtige cellen worden voedingsrijke eilanden die de schimmel voeden. Inzicht in deze schimmelstrategie opent de deur naar veredeling of engineering van maïsvariëteiten waarin SnRK1 of verwante paden minder kwetsbaar zijn, waardoor gewassen resistenter worden tegen tumorvormende infecties zonder groei op te offeren.
Bronvermelding: Lee, Y.J., Zhang, D., Stolze, S.C. et al. Ustilago maydis disrupts carbohydrate signaling networks to induce hypertrophy in host cells. Nat Commun 17, 1990 (2026). https://doi.org/10.1038/s41467-026-69532-8
Trefwoorden: maïs schimmel, plantenimmuniteit, schimmelige effectors, zetmeelmetabolisme, SnRK1-signaleringsweg