Clear Sky Science · nl
Een synthetische cel met geïntegreerde DNA-zelfreplicatie en lipidesynthese
Leven van nul opbouwen
Wat maakt een levende cel meer dan een zakje moleculen? Een belangrijk antwoord ligt in het vermogen om zijn genetische instructies te kopiëren en zijn eigen beschermende membraan te bouwen. Deze studie zet een grote stap richting het nabootsen van die truc in het laboratorium. De auteurs ontwerpen kleine vetbellen, liposomen genoemd, die een stukje DNA kunnen lezen, dat DNA kunnen kopiëren en nieuw membraanmateriaal kunnen maken — allemaal binnen hetzelfde miniatuurtje compartiment. Hun werk brengt ons dichter bij kunstmatige cellen die kunnen groeien, zich aanpassen en misschien op een dag zelfstandig kunnen evolueren.
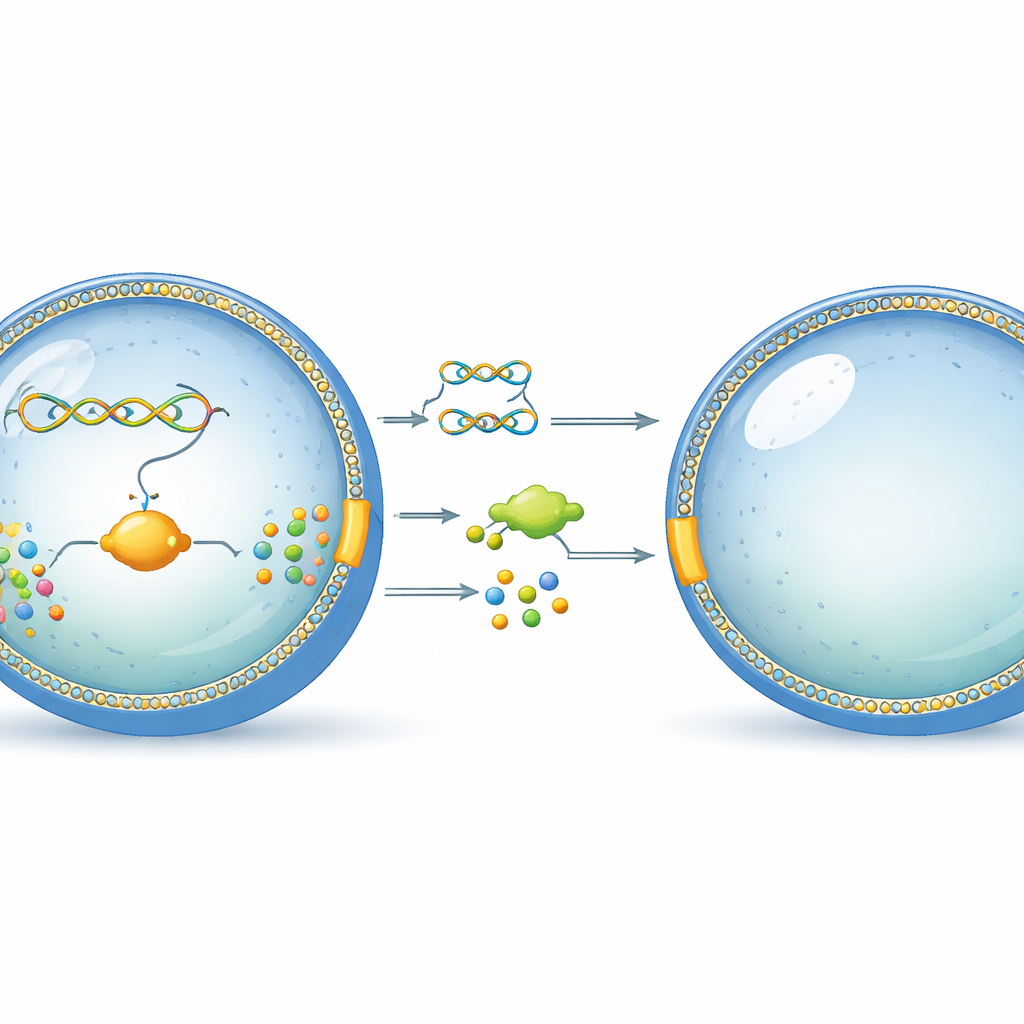
Een piepkleine bel die als een cel werkt
De onderzoekers beginnen met eenvoudige, celgrote belletjes gemaakt van fosfolipiden, hetzelfde type moleculen dat de buitenste laag van echte cellen vormt. In deze belletjes stoppen ze een zorgvuldig ontworpen DNA-streng en een set gezuiverde cellulaire machines die DNA kunnen lezen en eiwitten kunnen maken. Deze opstelling, een celvrij expressiesysteem genoemd, functioneert als de uitgeklede kern van een levende cel: hij kan genetische informatie omzetten in werkzame moleculen zonder dat er een levend organisme aan te pas komt. Het sleutelidee is om alles binnen het liposoom te plaatsen zodat het genetische programma en zijn producten bij elkaar blijven, net zoals in een natuurlijke cel.
Een op maat gemaakt DNA-programma met twee taken
In het hart van hun synthetische cel bevindt zich een op maat gemaakte DNA-molecule die de auteurs DNArep-PLsyn noemen. Dit DNA draagt instructies voor zes eiwitten. Twee ervan komen van een bacteriofaag (een virus dat bacteriën infecteert) en vormen samen een module die het DNA zelf kan kopiëren, en zo een ingebouwde zelfreplicatiemodule biedt. De andere vier stammen van de darmbacterie E. coli en vormen een keten van reacties die eenvoudige uitgangsstoffen omzet in een specifiek fosfolipide dat in membranen wordt gebruikt. Om dit ongebruikelijke genoom samen te stellen, moest het team DNA-stukken aan elkaar lijmen in reageerbuizen en in gistcellen, en het resultaat vervolgens omzetten in een lineaire DNA-streng die door de virale kopieermachinerie herkend en gerepliceerd kan worden.
Het synthetische proces maken en testen
Zodra het DNA en de eiwitmakende machinerie in de liposomen zijn verzegeld, worden de belletjes op verschillende temperaturen verwarmd en aan het werk gezet. Het team controleert wat er gebeurt met fluorescerende markers: één kleurstof licht op wanneer hij aan DNA bindt, waarmee zichtbaar wordt hoeveel DNA aanwezig is, en een andere hecht zich aan het nieuwe fosfolipide als dat geproduceerd en in het membraan ingebouwd wordt. Met flowcytometrie en hogeresolutiemicroscopie kunnen ze tienduizenden individuele vesikels analyseren. Ze vinden dat veel belletjes het genoom succesvol kopiëren, vele anderen nieuwe membraansyntheseproducten maken, en een kleinere maar significante fractie beide activiteiten tegelijk kan uitvoeren. Aanvullende tests met DNA-kwantificatie en massaspectrometrie bevestigen dat het volledige genoom wordt vermeerderd en dat nieuwe fosfolipidemoleculen daadwerkelijk gesynthetiseerd worden, zij het in bescheiden hoeveelheden.
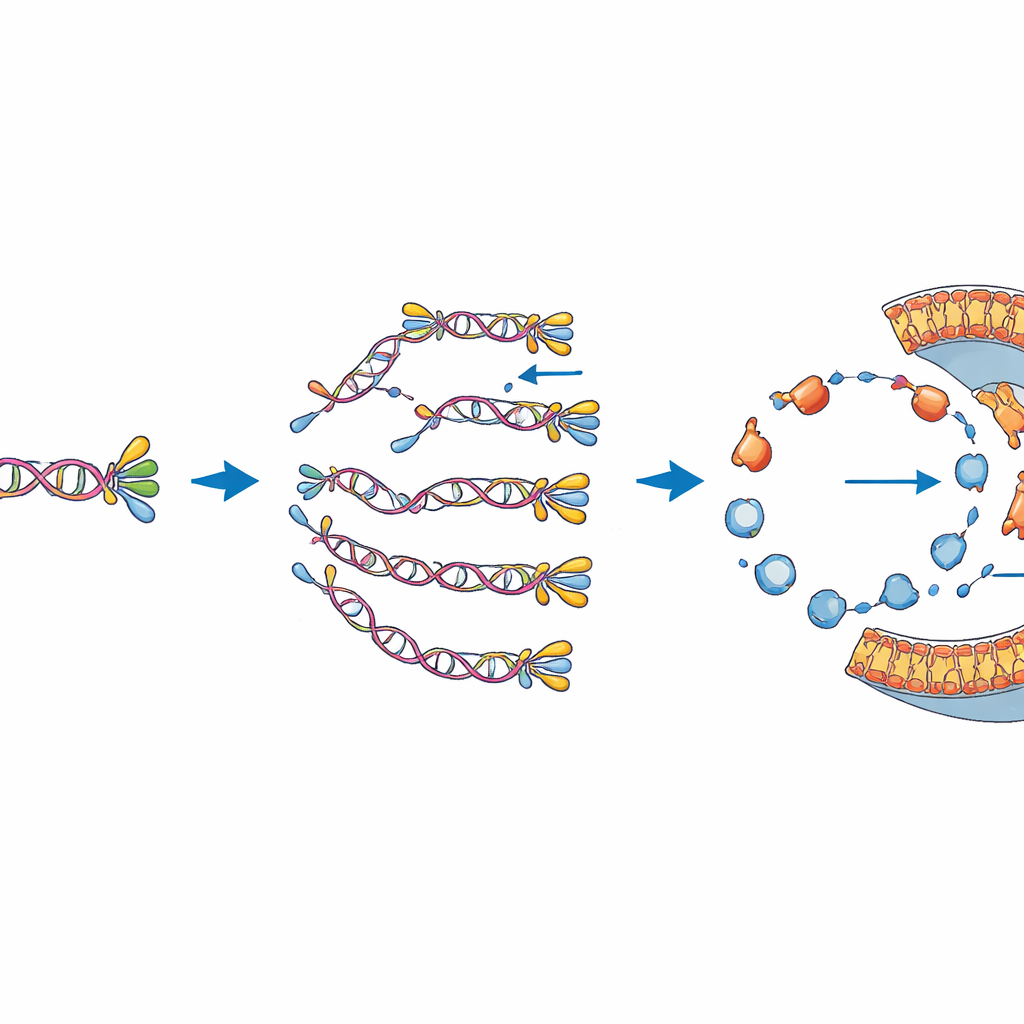
Twee essentiële taken in balans brengen
De auteurs onderzoeken vervolgens hoe deze twee functies elkaar beïnvloeden. Door de DNA-kopieer- of membraanmaken-chemie aan en uit te zetten via de benodigde ingrediënten, tonen ze aan dat elk proces grotendeels kan werken zonder de ander te verstoren. Echter, wanneer beide modules op hetzelfde DNA gecodeerd zijn, blijkt de membraansynthesekant kwetsbaarder: minder vesikels tonen deze activiteit vergeleken met vesikels die alleen de lipide-gerelateerde genen dragen. Evenzo replikeert het gecombineerde genoom niet zo efficiënt als een kleinere versie die alleen de DNA-replicatiegenen bevat. Dit suggereert dat zelfs in dit uitgeklede systeem er concurrentie is om gedeelde middelen en fysieke plaats op het DNA, wat echo’s oproept van de afwegingen die in echte cellen worden gezien.
Zich voorbereiden op evolutie in de reageerbuis
Om verder te gaan dan een eenmalige demonstratie, ontwerpen de onderzoekers hun systeem zo dat het in principe via evolutie verbeterd kan worden. Ze produceren schonere, betrouwbaardere DNA-versies met plasmiden die in gist en bacteriën zijn gekweekt, wat het aandeel volledig functionele synthetische cellen verhoogt. Ze laten ook zien dat het mogelijk is om genomen te kapselen, te selecteren en terug te winnen uit vesikels die zowel DNA-kopie als membraansynthese uitvoeren. Dit bereidt de weg voor toekomstige cycli waarin licht verschillende genomen met elkaar concurreren en diegenen die beter presteren worden verrijkt en gekopieerd.
Waarom dit belangrijk is voor ons begrip van leven
Simpel gezegd hebben de onderzoekers een microscopisch belletje gebouwd dat zijn eigen recept kan lezen, meer exemplaren van dat recept kan maken en het kan gebruiken om zijn buitenste huid te herstellen en uit te breiden. Hoewel deze synthetische cellen nog niet groot kunnen groeien of delen zoals levende organismen, laat het werk zien dat kernkenmerken van leven — informatieopslag, zelfkopiëren en basale zelfconstructie — gecombineerd kunnen worden in een eenvoudig, beheersbaar pakket. Dit vormt belangrijk fundament voor het onderzoeken hoe leven mogelijk uit niet-levende chemie is ontstaan en voor het ontwerpen van kunstmatige cellen die nuttige taken uitvoeren, van slimme geneesmiddelafgifte tot zelfvernieuwende mini-fabriekjes.
Bronvermelding: Restrepo Sierra, A.M., Ramirez Gomez, F., van Tongeren, M. et al. A synthetic cell with integrated DNA self-replication and lipid biosynthesis. Nat Commun 17, 2727 (2026). https://doi.org/10.1038/s41467-026-69531-9
Trefwoorden: synthetische cellen, DNA-zelfreplicatie, lipidesynthese, kunstmatig leven, bottom-up biologie